山东省济宁市高新区2021-2022学年九年级下学期期中化学试题
试卷更新日期:2022-10-08 类型:期中考试
一、单选题
-
1. 实验室中的药品要求分类存放。某实验室1号柜存放的是单质,2号柜存放的是酸,3号柜存放的是碱,4号柜存放的是盐。纯碱应存放的实验柜是( )A、1号柜 B、2号柜 C、3号柜 D、4号柜2. “火碱、烧碱、纯碱、苛性钠、小苏打”所代表的物质(或主要成分)共有( )A、一种 B、二种 C、三种 D、四种3. 某同学用月季花自制酸碱指示剂,并用于检验白醋的酸碱性,部分操作如下,其中错误的是( )A、研磨花瓣
 B、浸取色素
B、浸取色素 C、取用白醋
C、取用白醋 D、检验白醋
D、检验白醋 4. 下表为四种植物适宜生长的pH范围,不适宜种植在酸性土壤中的是( )
4. 下表为四种植物适宜生长的pH范围,不适宜种植在酸性土壤中的是( )选项
A
B
C
D
植物
杨梅
菠萝
甘薯
冬枣
pH
4.0--5.0
4.5--5.5
5.0--6.0
8.0--8.5
A、A B、B C、C D、D5. 对于碱,下列说法正确的是( )A、碱一定含有 H 元素 B、可使酚酞变红的都是碱溶液 C、所有非金属氧化物都可与碱溶液反应 D、酸与碱反应一定不产生沉淀6. 王亚平在中国空间站表演“五环魔术”,她往碳酸钠溶液中加入溴百里酚蓝试剂,呈现鲜亮的蓝色。若将溴百里酚蓝加入盐酸中,则会呈现黄色。下列有关说法错误的是( )A、溴百里酚蓝可作为酸碱指示剂 B、碳酸钠的化学式为Na2CO3 C、碳酸钠溶液呈碱性 D、碳酸钠属于碱7. 晾晒海水获得的粗盐中含有可溶性杂质MgCl2、CaCl2等。现要除去粗盐溶液中的MgCl2和CaCl2 , 需先依次加入足量的a和b,过滤后再加c。则a、b、c分别是( )A、Na2CO3 稀盐酸NaOH B、K2CO3NaOH稀盐酸 C、NaOHNa2CO3稀盐酸 D、KOH稀盐酸Na2CO38. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。下列说法错误的是( ) A、P点表示t2℃时,甲和乙的溶解度相等 B、t3℃时Q点表示甲的不饱和溶液 C、t3℃时,将25g乙放入50g水中,所得溶液中溶质和溶剂的质量比为2:5 D、将t3℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为丙>甲>乙9. 下列每组中的物质在溶液中能大量共存且溶液为无色的是( )A、FeCl3、NaCl、Na2SO4 B、K2CO3、NaCl、H2SO4 C、BaCl2、Na2SO4、NaOH D、MgCl2、Na2SO4、HCl10. 向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )A、
A、P点表示t2℃时,甲和乙的溶解度相等 B、t3℃时Q点表示甲的不饱和溶液 C、t3℃时,将25g乙放入50g水中,所得溶液中溶质和溶剂的质量比为2:5 D、将t3℃时甲、乙、丙的饱和溶液降温至t1℃,溶质的质量分数由大到小的顺序为丙>甲>乙9. 下列每组中的物质在溶液中能大量共存且溶液为无色的是( )A、FeCl3、NaCl、Na2SO4 B、K2CO3、NaCl、H2SO4 C、BaCl2、Na2SO4、NaOH D、MgCl2、Na2SO4、HCl10. 向盛有一定质量稀盐酸的四个烧杯中,分别逐渐加入金属镁、Fe2O3固体、Cu(OH)2固体、Na2CO3溶液至过量。下列图像能正确反映其对应变化关系的是( )A、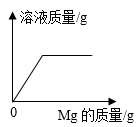 B、
B、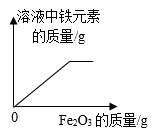 C、
C、 D、
D、
二、综合题
-
11. 如图是工业上以石灰石为原料的化工生产过程中主要物质之间的转化关系(图中部分生成物已略去)。

回答下列问题:
(1)、已知反应②的化学方程式为 , 则D物质的化学式是。(2)、写出反应④的化学方程式。(3)、实验室可利用F制备少量的氢氧化钠溶液,反应的化学方程式为 , 该反应属于(填基本反应类型)反应。(4)、F在生产和生活中用途广泛,请任举一例:。12. 金属镁被誉为“国防金属”,目前世界上60%的镁是从海水中提取的。某兴趣小组在实验室模拟海水提镁的主要流程如下: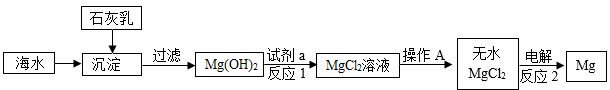 (1)、过滤后,滤液仍浑浊的原因可能是 (写出一点即可)。(2)、试剂a是 , 写出反应Ⅰ的化学方程式:。(3)、操作A的名称: , 反应2属于 (填基本反应类型)。13. 物质的溶解度不同,用途也不同。请据表回答:
(1)、过滤后,滤液仍浑浊的原因可能是 (写出一点即可)。(2)、试剂a是 , 写出反应Ⅰ的化学方程式:。(3)、操作A的名称: , 反应2属于 (填基本反应类型)。13. 物质的溶解度不同,用途也不同。请据表回答:表一 物质的溶解度(20℃)
物质
NaOH
Ca(OH)2
CaCO3
CaSO3
溶解度(克)
109
0.165
0.0014
0.0043
表二 物质在水中的溶解性等级
20℃时的溶解度(克)
>10
1-10
0.01-1
<0.01
等级
易溶
可溶
微溶
难溶
(1)、实验中一般用氢氧化钠溶液吸收二氧化碳,而不用澄清石灰水来吸收二氧化碳主要原因是氢氧化钙于水,吸收效果不好。(2)、实验中一般用澄清石灰水检验二氧化碳,但是根据上表可知能使澄清石灰水变浑浊的不一定是二氧化碳,也可能是二氧化硫,请用化学方程式说明。(3)、20℃时,饱和氢氧化钠溶液的溶质质量分数为。(精确到0.1%)14. 某化学实验小组将未经打磨的铝片放入盛有稀硫酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示,回答下列问题: (1)、AB段压强不变的原因 , 反应在点停止(填字母)。(2)、CD段容器内压强变小的原因。15. 几种固体物质的溶解度曲线如图所示,请回答下列问题。
(1)、AB段压强不变的原因 , 反应在点停止(填字母)。(2)、CD段容器内压强变小的原因。15. 几种固体物质的溶解度曲线如图所示,请回答下列问题。 (1)、在50 ℃时,硝酸钾的溶解度(填“大于”“小于”或“等于”)氯化钾的溶解度。(2)、使接近饱和的硝酸钾溶液变为饱和溶液的方法是(任写一种)。(3)、硝酸钾、氯化钾和氢氧化钙中,溶解度随温度升高而减小的是。(4)、在40 ℃时,向50 g水中加入25 g氯化钾,充分溶解后,所得溶液的溶质质量分数是(精确到0.1%)。16. 中和反应是一类重要的化学反应,化学兴趣小组做了如下实验:
(1)、在50 ℃时,硝酸钾的溶解度(填“大于”“小于”或“等于”)氯化钾的溶解度。(2)、使接近饱和的硝酸钾溶液变为饱和溶液的方法是(任写一种)。(3)、硝酸钾、氯化钾和氢氧化钙中,溶解度随温度升高而减小的是。(4)、在40 ℃时,向50 g水中加入25 g氯化钾,充分溶解后,所得溶液的溶质质量分数是(精确到0.1%)。16. 中和反应是一类重要的化学反应,化学兴趣小组做了如下实验: (1)、观察到试管①③中共同的明显现象是 , 试管②中没有明显现象。(2)、(提出问题)试管②中没有明显现象,是否发生了反应?
(1)、观察到试管①③中共同的明显现象是 , 试管②中没有明显现象。(2)、(提出问题)试管②中没有明显现象,是否发生了反应?(实验探究)
化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了(填写现象),证明了稀盐酸和氢氧化钠溶液一定发生了化学反应,为进一步探究试管②反应后溶液中溶质成分,还可以向试管b中加入下列物质中的(填字母)。
A Zn B Fe(OH)3 C FeCl3 D AgNO3
(3)、化学兴趣小组又利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和测定结果如图所示:
①该实验中,乙溶液是;
②加入甲溶液6mL时,烧瓶中的溶液溶质成分(填化学式);
③根据该实验测定结果,判断发生化学反应的依据是。
17. 泡腾片含有NaHCO3和柠檬酸等物质,放入水中时,NaHCO3完全反应产生CO2。某化学兴趣小组的同学欲测定某品牌泡腾片中NaHCO3的含量,设计实验方案如下:
按图示连接装置并加入药品,取用的泡腾片质量为4 g。打开止水夹a通入适量空气后,称量D装置,其质量为m1 g。关闭止水夹a,用注射器向B装置中注入适量水。待装置B中无气泡产生后,打开止水夹a,再次通入适量空气,第二次称量D装置,其质量为m2 g。
回答下列问题:
(1)、A装置中浓NaOH溶液的作用是 , B装置盛装泡腾片的仪器名称是。(2)、C装置中浓硫酸的作用是。(3)、碱石灰主要含CaO和NaOH,D装置中碱石灰吸收CO2质量增加,写出所涉及反应的一个化学方程式:。(4)、步骤中再次通入空气的目的是。(5)、实验测定泡腾片中所含NaHCO3的质量分数为(用含m1、m2的代数式表示)。若省略E装置,则测得NaHCO3的质量分数(填“偏大”“偏小”或“不变”)。三、计算题
-
18. 欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示:

回答下列问题:
(1)、a点溶液中的溶质是(填化学式)。(2)、计算该稀硫酸的溶质质量分数。( 写出计算过程,结果精确到0.1%)