山东省日照市2022-2023学年高二上学期8月校际联考化学试题
试卷更新日期:2022-09-26 类型:月考试卷
一、单选题
-
1. 下列文献记载的物质的提取方法涉及蒸馏操作的是( )A、《医学入门》记载提纯铜绿:“水洗净,细研水飞,去石澄清,慢火熬干” B、《本草纲目》记载提取硝酸钾:“此即地霜也,所在山泽,冬月地上有霜,扫取以水淋汁,后乃煎炼而成” C、《游宦纪闻》记载提取花露水:“锡为小瓶,实花一重,……。窍甑之傍,以泄汗液,以器贮之” D、《菽园杂记》记载提取食盐:“烧草为灰,布在滩场,然后以海水渍之,侯晒结浮白,扫而复淋”2. 下列化学用语表示正确的是( )A、质子数为92、中子数为146的铀(U)原子: B、的电子式: C、四氯化碳的球棍模型:
 D、用电子式表示HCl的形成过程:
D、用电子式表示HCl的形成过程: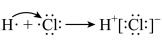 3. 下列关于常见有机物的说法错误的是( )A、正丁烷的沸点高于异丁烷 B、用燃料电池型呼气酒精检测仪检验是否“酒驾”,利用的是乙醇的还原性 C、乳酸(
3. 下列关于常见有机物的说法错误的是( )A、正丁烷的沸点高于异丁烷 B、用燃料电池型呼气酒精检测仪检验是否“酒驾”,利用的是乙醇的还原性 C、乳酸( )与乙醇、乙酸均可发生酯化反应
D、若2.6 g某烃完全燃烧,生成和 , 则该烃一定为乙炔()
4. 下列说法正确的是( )A、将某刺激性气味的气体通入品红溶液,若溶液褪色,则该气体为 B、将少量通入淀粉KI溶液,若溶液变蓝色,可证明Cl的得电子能力强于I C、制备溴苯时,将反应后的混合液用稀NaOH溶液洗涤后过滤,可得到溴苯 D、用同浓度同体积的氨水代替NaOH溶液,测得的中和反应的反应热数值偏高5. 某盐的结构如图所示,其中X、Y、Z、W是原子序数依次递增的短周期元素。下列说法正确的是( )
)与乙醇、乙酸均可发生酯化反应
D、若2.6 g某烃完全燃烧,生成和 , 则该烃一定为乙炔()
4. 下列说法正确的是( )A、将某刺激性气味的气体通入品红溶液,若溶液褪色,则该气体为 B、将少量通入淀粉KI溶液,若溶液变蓝色,可证明Cl的得电子能力强于I C、制备溴苯时,将反应后的混合液用稀NaOH溶液洗涤后过滤,可得到溴苯 D、用同浓度同体积的氨水代替NaOH溶液,测得的中和反应的反应热数值偏高5. 某盐的结构如图所示,其中X、Y、Z、W是原子序数依次递增的短周期元素。下列说法正确的是( ) A、X与Y、Z、W均可形成原子个数比为1:1的化合物 B、X、Y的氧化物的熔点:X<Y C、该盐中各元素原子的最外层均达到8电子稳定结构 D、X、Y形成的化合物均不能使酸性高锰酸钾溶液褪色6. 为阿伏加德罗常数的值,下列说法正确的是( )
A、X与Y、Z、W均可形成原子个数比为1:1的化合物 B、X、Y的氧化物的熔点:X<Y C、该盐中各元素原子的最外层均达到8电子稳定结构 D、X、Y形成的化合物均不能使酸性高锰酸钾溶液褪色6. 为阿伏加德罗常数的值,下列说法正确的是( )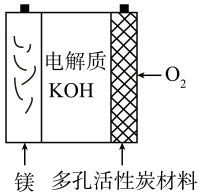 A、78 g 中含有的阴离子数为 B、标准状况下,2.24L乙醇中的碳氢键数为 C、镁-空气电池(如图所示)工作时,若外电路中有个电子通过,则负极质量增重58 g D、标准状况下的与 , 在光照下充分反应后分子总数为7. 利用太阳光在一种新型复合光催化剂表面实现高效分解水的主要过程如图所示。
A、78 g 中含有的阴离子数为 B、标准状况下,2.24L乙醇中的碳氢键数为 C、镁-空气电池(如图所示)工作时,若外电路中有个电子通过,则负极质量增重58 g D、标准状况下的与 , 在光照下充分反应后分子总数为7. 利用太阳光在一种新型复合光催化剂表面实现高效分解水的主要过程如图所示。
几种化学键的键能:
化学键
H-O
O=O
H-H
O-O
键能/()
463
496
436
138
下列说法错误的是( )
A、过程Ⅰ生成了·OH和·H B、过程Ⅱ中只有新化学键的生成 C、总反应的化学方程式为 D、若反应过程中有2 mol水分解,则过程Ⅲ放出132 kJ能量8. 铁-铬液流电池的装置如下图所示,下列说法错误的是( ) A、放电时,通过质子交换膜向Y电极移动 B、通过该原电池反应可知氧化性: C、充电时,X电极的电极反应式为 D、充电完成后,可将电解质溶液泵回储液罐,将能量储存起来9. 双酚A的结构如图所示,下列说法正确的是( )
A、放电时,通过质子交换膜向Y电极移动 B、通过该原电池反应可知氧化性: C、充电时,X电极的电极反应式为 D、充电完成后,可将电解质溶液泵回储液罐,将能量储存起来9. 双酚A的结构如图所示,下列说法正确的是( )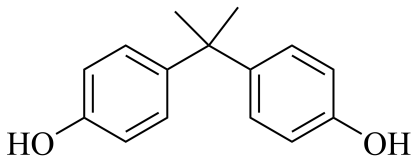 A、双酚A的分子式为 B、双酚A分子中存在6种化学环境不同的氢 C、双酚A能发生取代、加成、氧化反应 D、1 mol双酚A与足量钠反应,可产生2 mol10. 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌的作用下能被腐蚀,原理如图所示。下列说法错误的是( )
A、双酚A的分子式为 B、双酚A分子中存在6种化学环境不同的氢 C、双酚A能发生取代、加成、氧化反应 D、1 mol双酚A与足量钠反应,可产生2 mol10. 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌的作用下能被腐蚀,原理如图所示。下列说法错误的是( )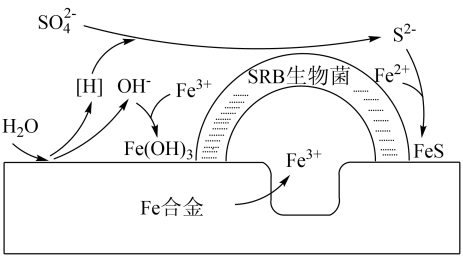 A、腐蚀过程中正极附近碱性增强 B、该腐蚀过程属于吸氧腐蚀 C、硫酸盐还原菌SRB加快了金属的腐蚀 D、可在管道上镶嵌锌块以减缓腐蚀,这种方法叫做牺牲阳极保护法11. 如图所示,将气体X、Y通入溶液乙中,不能产生浑浊的是( )
A、腐蚀过程中正极附近碱性增强 B、该腐蚀过程属于吸氧腐蚀 C、硫酸盐还原菌SRB加快了金属的腐蚀 D、可在管道上镶嵌锌块以减缓腐蚀,这种方法叫做牺牲阳极保护法11. 如图所示,将气体X、Y通入溶液乙中,不能产生浑浊的是( )气体X
气体Y
溶液乙
A
NaCl溶液
B
饱和NaCl溶液
C
HCl
溶液
D
饱和溶液
 A、A B、B C、C D、D12. 利用Hck反应在强碱和钯催化下合成二苯乙烯的方法如下,下列说法正确的是( )
A、A B、B C、C D、D12. 利用Hck反应在强碱和钯催化下合成二苯乙烯的方法如下,下列说法正确的是( )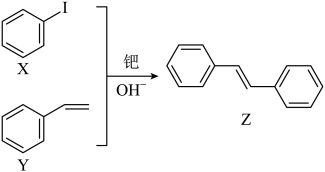 A、Heck反应属于加成反应 B、X、Y、Z三种物质均为不饱和烃 C、Z分子中处于同一平面的原子最多为26个 D、常温下,1mol物质Z最多能与7mol发生加成反应
A、Heck反应属于加成反应 B、X、Y、Z三种物质均为不饱和烃 C、Z分子中处于同一平面的原子最多为26个 D、常温下,1mol物质Z最多能与7mol发生加成反应二、多选题
-
13. Q、X、Y、Z、W是原子序数依次增大的短周期主族元素,其最外层电子数之和为26,Q与X、Y、Z、W位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍,W的一种气态氧化物是高效消毒剂。下列说法正确的是( )A、简单化物的稳定性:Z<Q B、Q与Z一定位于同一主族 C、最高价氧化物的水化物的酸性:Z>Y D、工业上常用电解X与W形成的化合物水溶液的方法制备X单质14. 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示。若使用铅蓄电池作外接电源,下列说法错误的是( )
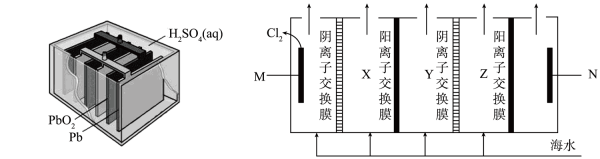 A、Y室可获得淡化的海水 B、电解时,M电极连接铅蓄电池的Pb电极 C、撤去X与Y、Y与Z之间的交换膜也可得到淡化的海水 D、理论上N电极产生11.2L(标准状况)气体时,Pb电极增重48 g15. 一定温度下,2L密闭容器中加入1 mol M,同时发生反应:
A、Y室可获得淡化的海水 B、电解时,M电极连接铅蓄电池的Pb电极 C、撤去X与Y、Y与Z之间的交换膜也可得到淡化的海水 D、理论上N电极产生11.2L(标准状况)气体时,Pb电极增重48 g15. 一定温度下,2L密闭容器中加入1 mol M,同时发生反应:① , 反应速率;
② , 反应速率
已知:、为反应速率常数,只与温度有关。M、Z的物质的量随时间变化如图所示。下列说法正确的是( )
 A、20min时,反应②一定达到化学平衡状态 B、0~20min内,Y的平均反应速率为 C、容器内气体压强不再改变时,反应①、②均达到化学平衡状态 D、反应①、②均达到化学平衡状态时,c(Y):c(Z)=1:2
A、20min时,反应②一定达到化学平衡状态 B、0~20min内,Y的平均反应速率为 C、容器内气体压强不再改变时,反应①、②均达到化学平衡状态 D、反应①、②均达到化学平衡状态时,c(Y):c(Z)=1:2三、综合题
-
16. 下表为元素周期表的一部分,表中所列的每个字母分别代表一种元素。

回答下列问题:
(1)、元素f的原子结构示意图为。(2)、c、d、e的简单离子半径由大到小的顺序为(用离子符号表示)。(3)、c与d形成的原子个数比为1:1的化合物中含有的化学键类型为。(4)、下列事实能说明d元素原子的失电子能力比e强的是____(填标号)。A、单质的熔点:d<c B、简单阳离子的氧化性:e>d C、常温下,d单质能与水剧烈反应而e不能 D、相同物质的量的d、e单质分别与足量盐酸反应,生成的的量:d<c(5)、f与g组成的化合物是一种重要的半导体材料,该化合物中得电子能力更强的元素是(填元素符号),其原因是。(6)、高温下e的氧化物可与a、b单质反应生成高导热结构陶瓷eb和一种还原性气体,该反应的化学方程式为。17. 利用加氢制甲醇是实现碳中和、碳达峰较为可行的方法。已知:
回答下列问题:
(1)、 。(2)、恒温恒容的容器中仅发生反应 , 下列说法正确的是____(填标号)。A、时,说明反应达到平䡓状念 B、时,说明反应达到平衡状态 C、的体积分数保持不变时,说明反应达到平衡状态 D、反应达到平衡后,升高温度,正反应速率增大,逆反应速率减小(3)、一定温度下,在2 L的密闭容器中按物质的量比1:5充入和 , 发生反应 , 测得和的物质的量浓度随时间变化关系如图所示。

①3min时,(填“>”“=”或“<”),0~10min,反应放出kJ的热量。
②反应达到化学平衡时,=。
(已知:)
若初始总压强为 , 平衡时总压强为P,则=。
③反应达到平衡后,下列条件可使化学平衡发生移动的是(填标号)。
A.恒容条件充入 B.升高温度
C.使用高效催化剂 D.恒容条件充入He
18. 实验室利用异丁酸( 和氯化亚砜()制备异丁酰氯(
和氯化亚砜()制备异丁酰氯( )的实验装置如图所示(夹持和加热装置已省略)。
)的实验装置如图所示(夹持和加热装置已省略)。 
实验时,先在A中放入8.8g异丁酸,再由B向A中滴入10 mL (密度为),80℃下回流45 min,生成异丁酰氨和两种常见酸性气体。D中溶液褪色,E中溶液颜色变浅。
已知:Ⅰ、易溶于:
Ⅱ、相关物理量:
物质
异丁酸
异丁酰氯
沸点/℃
153
78.8
93
相对分子质量
88
119
106.5
问答下列问题:
(1)、仪器A的名称为 , 应采用的加热方式为(填“水浴加热”“直接加热”或“油浴加热"):A中发生的化学方程式为。(2)、C装置的作用为。(3)、E中发生反应的离子方程式为。(4)、反应完成后,为制得纯净的异丁酰氯,须进行操作(填操作名称):该操作须用到的玻璃仪器与上述装置中相同的,除导气管外还有(填仪器名称)。(5)、经一系列操作,最终获得纯净异丁酰氯6.39 g,则该反应的产率为%()。19. “电化学”与人类生产、生活密不可分,下图Ⅰ甲池可实现在铁表面镀锌:下图Ⅱ可通过电解废旧锂电池中的获得锂盐和。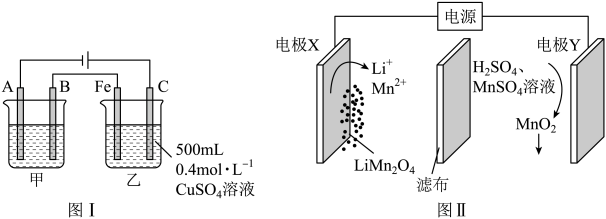
回答下列问题:
(1)、上图Ⅰ中A电极的电极材料为;乙池电解开始时发生反应的化学方程式为。(2)、上图Ⅰ,工作一段时间后,若甲池阴极增重26g,则乙池中产生气体的体积为L(标准状况)。(3)、上图Ⅱ中滤布的作用为。X电极为极,其电极反应式为。(4)、上图Ⅱ电解过程中将(填“增大”“减小”或“不变”,忽略电解过程中溶液体积的变化)。20. 肉桂酸异丙酯(G)常用于软饮料、冰制食品的调味与增香,其一种合成路线如下。
一定条件下
已知: , R为烃基。
回答下列问题:
(1)、石蜡油分解的实验中,碎瓷片的作用是。(2)、A→B的化学方程式为。(3)、E→F的反应类型为。G中所含官能团的名称为。(4)、D+F→G的化学方程式为。(5)、参照上述合成路线,写出由乙醇制备的合成路线(无机试剂任选) 。