浙教版科学九年级上学期 第二单元 物质转化与材料利用 综合卷(2)
试卷更新日期:2022-09-22 类型:单元试卷
一、单选题
-
1. 材料与人类生活密切相关,下列物品是由金属材料制成的是( )A、
 羊毛衫
B、
羊毛衫
B、 塑料盆
C、
塑料盆
C、 不锈钢餐具
D、
不锈钢餐具
D、 玻璃杯
2. 下列是表示气体微粒的示意图,图中“●”和“O”分别表示不同元素的原子,其中表示单质的是( )A、
玻璃杯
2. 下列是表示气体微粒的示意图,图中“●”和“O”分别表示不同元素的原子,其中表示单质的是( )A、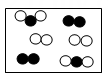 B、
B、 C、
C、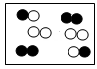 D、
D、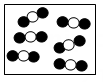 3. 84 消毒液(主要成分是NaClO)在防疫期间被很多学校广泛使用。专家特别提醒,它不能和洁厕灵(主要成分是HCl)混合使用,否则会产生有毒气体,其反应原理是NaClO+2HCl=NaCl+H2O+X。由此能做出的判断是( )A、该反应为复分解反应 B、NaClO 是一种氧化物 C、有毒气体X为氯气 D、反应中氯元素的化合价均发生改变4. 构建元化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价类二维图”。下列说法错误的是( )
3. 84 消毒液(主要成分是NaClO)在防疫期间被很多学校广泛使用。专家特别提醒,它不能和洁厕灵(主要成分是HCl)混合使用,否则会产生有毒气体,其反应原理是NaClO+2HCl=NaCl+H2O+X。由此能做出的判断是( )A、该反应为复分解反应 B、NaClO 是一种氧化物 C、有毒气体X为氯气 D、反应中氯元素的化合价均发生改变4. 构建元化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价类二维图”。下列说法错误的是( )
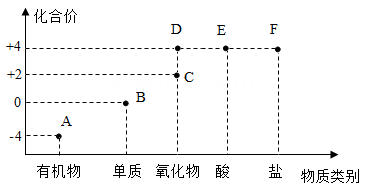 A、A点可能是CH4 B、B点对应的物质充分燃烧可得到D点对应的物质 C、某化合物的化学式为CaCO3 , 它对应的点是F D、C点对应的物质与水反应可得到E点对应的物质5. 将一定量金属M加入到ZnSO4和CuSO4的混合溶液中,充分反应后,过滤,得到固体滤渣,滤液为无色,向滤渣中滴加稀盐酸有气泡产生。下列有关M、Zn、Cu金属活动性判断一定正确的是( )A、M>Zn B、Zn>M C、M>Cu D、Cu>M6. 氢气还原氧化铜实验,反应的化学方程式为H2+CuOCu+H2O下列说法错误的是( )
A、A点可能是CH4 B、B点对应的物质充分燃烧可得到D点对应的物质 C、某化合物的化学式为CaCO3 , 它对应的点是F D、C点对应的物质与水反应可得到E点对应的物质5. 将一定量金属M加入到ZnSO4和CuSO4的混合溶液中,充分反应后,过滤,得到固体滤渣,滤液为无色,向滤渣中滴加稀盐酸有气泡产生。下列有关M、Zn、Cu金属活动性判断一定正确的是( )A、M>Zn B、Zn>M C、M>Cu D、Cu>M6. 氢气还原氧化铜实验,反应的化学方程式为H2+CuOCu+H2O下列说法错误的是( )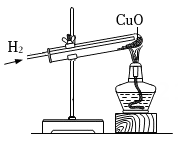 A、发生的反应属于置换反应 B、反应中氢气属于还原剂 C、实验中是先加热,后通氢气 D、可观察到氧化铜有黑丝变红色7. 某同学为探究镁、锌、铜、银的活动性顺序,设计了如下实验流程。依据该流程设计,下面对物质①、②的选择合理的是( )
A、发生的反应属于置换反应 B、反应中氢气属于还原剂 C、实验中是先加热,后通氢气 D、可观察到氧化铜有黑丝变红色7. 某同学为探究镁、锌、铜、银的活动性顺序,设计了如下实验流程。依据该流程设计,下面对物质①、②的选择合理的是( )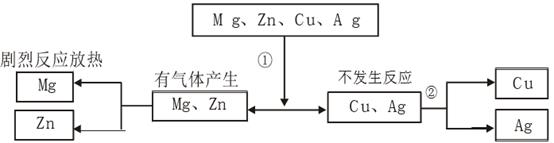 A、①稀硫酸,②硫酸铜溶液 B、①稀硫酸,②硫酸锌溶液 C、①稀盐酸,②硫酸亚铁溶液 D、①稀盐酸,②氯化镁溶液8. 检验碳酸盐的常用方法是( )。A、加入氯化钡溶液,产生白色沉淀 B、加入石灰水,产生白色沉淀 C、加入稀盐酸,产生使石灰水变浑浊的气体 D、放入水中,不溶解的是碳酸盐9. 用Zn、CuO、稀H2SO4作原料制取Cu,有两种途径:①Zn H2 Cu ②CuO CuSO4 Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )A、消耗相同质量的氧化铜 B、消耗相同质量的锌 C、消耗相同质量的稀硫酸 D、生成硫酸锌的质量相同10. 下列图像能正确反映对应变化关系的是( )A、
A、①稀硫酸,②硫酸铜溶液 B、①稀硫酸,②硫酸锌溶液 C、①稀盐酸,②硫酸亚铁溶液 D、①稀盐酸,②氯化镁溶液8. 检验碳酸盐的常用方法是( )。A、加入氯化钡溶液,产生白色沉淀 B、加入石灰水,产生白色沉淀 C、加入稀盐酸,产生使石灰水变浑浊的气体 D、放入水中,不溶解的是碳酸盐9. 用Zn、CuO、稀H2SO4作原料制取Cu,有两种途径:①Zn H2 Cu ②CuO CuSO4 Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )A、消耗相同质量的氧化铜 B、消耗相同质量的锌 C、消耗相同质量的稀硫酸 D、生成硫酸锌的质量相同10. 下列图像能正确反映对应变化关系的是( )A、 实验室中用一氧化碳还原氧化铁
B、
实验室中用一氧化碳还原氧化铁
B、 往氢氧化钙溶液中逐滴加入蒸馏水
C、
往氢氧化钙溶液中逐滴加入蒸馏水
C、 向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液
D、
向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液
D、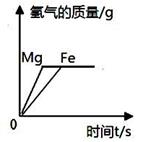 将足量粉末状金属分别与等质量、等质量分数的稀盐酸反应
11. 据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应惰性,可替代黄金做精密电子元器件。下列对该铜纳米颗粒的判断,正确的是( )A、能与盐酸反应产生氢气 B、在空气中容易锈蚀 C、能与硫酸亚铁发生置换反应 D、具有良好的导电性12. 归纳和演绎是重要的科学方法。下列归纳或演绎合理的是( )A、有机物是一类含碳化合物,所以CH4、CO2都是有机物 B、金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气 C、氧化物是由两种元素组成,其中一种是氧元素的化合物,所以水是氧化物 D、硫酸、盐酸电离时都能产生H+ , 所以电离时只要能产生H+的化合物都是酸13. 将等质量的甲、乙金属分别与足量的稀硫酸反应,产生的氢气的量与反应时间的关系如下图。则甲、乙两金属分别可能是( )
将足量粉末状金属分别与等质量、等质量分数的稀盐酸反应
11. 据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应惰性,可替代黄金做精密电子元器件。下列对该铜纳米颗粒的判断,正确的是( )A、能与盐酸反应产生氢气 B、在空气中容易锈蚀 C、能与硫酸亚铁发生置换反应 D、具有良好的导电性12. 归纳和演绎是重要的科学方法。下列归纳或演绎合理的是( )A、有机物是一类含碳化合物,所以CH4、CO2都是有机物 B、金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气 C、氧化物是由两种元素组成,其中一种是氧元素的化合物,所以水是氧化物 D、硫酸、盐酸电离时都能产生H+ , 所以电离时只要能产生H+的化合物都是酸13. 将等质量的甲、乙金属分别与足量的稀硫酸反应,产生的氢气的量与反应时间的关系如下图。则甲、乙两金属分别可能是( )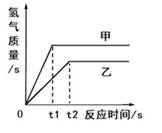 A、铁、锌 B、铁、铜 C、镁、铁 D、锌、铁14. 通过一步化学反应实现如图所示的 X、Y、Z 三种物质间转化,表格中 X、Y、Z 对应的物 质能实现这种转化的是( )
A、铁、锌 B、铁、铜 C、镁、铁 D、锌、铁14. 通过一步化学反应实现如图所示的 X、Y、Z 三种物质间转化,表格中 X、Y、Z 对应的物 质能实现这种转化的是( )
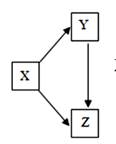
X
Y
Z
A
CO2
CaCO3
Na2CO3
B
Al
Al2O3
Al2(SO4)3
C
AgNO3
NaNO3
AgCl
D
H2SO4
CuSO4
Cu(OH)2
A、A B、B C、C D、D15. 如图所示为某化学反应的微观模拟示意图,下列说法中不正确的是( ) A、该反应不属于置换反应 B、图示中x的数值为3 C、反应前后氢元素的化合价发生了改变 D、该反应前后分子、原子的种类发生改变16. 小科将未经砂布打磨的铝条放入盛有稀盐酸的密闭容器中,用传感器测得容器内温度和压强的变化,如图所示。下列分析中正确的是( )
A、该反应不属于置换反应 B、图示中x的数值为3 C、反应前后氢元素的化合价发生了改变 D、该反应前后分子、原子的种类发生改变16. 小科将未经砂布打磨的铝条放入盛有稀盐酸的密闭容器中,用传感器测得容器内温度和压强的变化,如图所示。下列分析中正确的是( )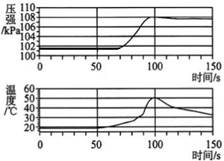 A、密闭容器内物质反应前后质量减少 B、50s时,溶液中的溶质为AlCl3 C、0~50s内,发生的反应是2Al+6HCl=2AlCl3+3H2↑ D、100s~140s内,温度降低说明反应停止并逐渐冷却,导致压强减小17. 在试管中加入一段纯净的镁条,再加入硝酸银溶液,观察到如下现象:①镁条表面迅速覆盖了一层疏松的固体物质;②镁条表面有明显的气泡。经检验,疏松的固体物质中有单质银,气泡中有氢气。对于上述实验现象,分析错误的是( )A、镁投入硝酸银溶液中,只发生:2AgNO3+Mg=Mg(NO3)2+2Ag B、镁跟硝酸银溶液反应会生成氢气 C、镁能从硝酸银溶液中置换出银 D、根据该实验可判断镁比银化学活动性强18. 现有铁、氧化铁、稀硫酸、氢氧化钙、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“﹣”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系)。下列判断合理的是( )
A、密闭容器内物质反应前后质量减少 B、50s时,溶液中的溶质为AlCl3 C、0~50s内,发生的反应是2Al+6HCl=2AlCl3+3H2↑ D、100s~140s内,温度降低说明反应停止并逐渐冷却,导致压强减小17. 在试管中加入一段纯净的镁条,再加入硝酸银溶液,观察到如下现象:①镁条表面迅速覆盖了一层疏松的固体物质;②镁条表面有明显的气泡。经检验,疏松的固体物质中有单质银,气泡中有氢气。对于上述实验现象,分析错误的是( )A、镁投入硝酸银溶液中,只发生:2AgNO3+Mg=Mg(NO3)2+2Ag B、镁跟硝酸银溶液反应会生成氢气 C、镁能从硝酸银溶液中置换出银 D、根据该实验可判断镁比银化学活动性强18. 现有铁、氧化铁、稀硫酸、氢氧化钙、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“﹣”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系)。下列判断合理的是( ) A、丙可能是碳酸钠溶液 B、丁可能是氢氧化钙溶液 C、乙必须通过置换反应转化为铁 D、甲和丁的反应一定是中和反应19. 现有a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液、盐酸中的一种。根据下表中它们两两间相互反应的实验记录,推断a、b、c、d的顺序正确的是( )
A、丙可能是碳酸钠溶液 B、丁可能是氢氧化钙溶液 C、乙必须通过置换反应转化为铁 D、甲和丁的反应一定是中和反应19. 现有a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液、盐酸中的一种。根据下表中它们两两间相互反应的实验记录,推断a、b、c、d的顺序正确的是( )a
b
c
d
b
无明显现象
——
有气体生成
有沉淀生成
c
有气体生成
有气体生成
——
有沉淀生成
A、H2SO4、Na2CO3、BaCl2、HCl B、HCl、H2SO4、Na2CO3、BaCl2 C、Na2CO3、H2SO4、HCl、BaCl2 D、BaCl2、Na2CO3、HCl、H2SO420. 现有一混合物的水溶液,只可能含有Na+、Ba2+、Cl-、 、 中的若干种。现取100mL此溶液进行如下实验:①加足量BaCl2溶液后,过滤,得干燥沉淀6.27g;
②在沉淀中加足量盐酸,过滤、洗涤、干燥后,称得沉淀质量为2.33g;
③在滤液中滴加AgNO3溶液,产生白色沉淀。
根据上述实验,下列推测中,正确的是( )
A、一定含 、 和Na+ , 一定不含Ba2+ B、一定含 、 和Na+ , 一定不含Ba2+ , 可能含Cl- C、一定含 和 ,一定不含Ba2+ , 可能含Na+和Cl- D、一定含 ,一定不含Ba2+和CO,可能含Cl-和Na+二、填空题
-
21. 废液中含有ZnCl2、FeCl2和CuCl2。要全部回收金属铜,某同学先向其中加入稍过量的铁粉,充分反应后过滤,(1)、滤渣中含有。(2)、要得到纯净的金属铜,这位同学需要继续完成的实验是(用化学方程式表示)22.
已知A、B为两种黑色粉末,D为红色单质.A﹣﹣E五种物质之间的转化关系如如图所示.
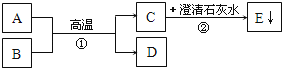
(1)C的化学式为 ;
(2)反应①的化学方程式为 .
23. 在一根用细绳吊着的长玻璃棒左端绕上光亮的粗制丝,并使玻璃棒保持水平(如图)。用酒精灯给铜丝加热数分钟,停止加热后冷却,发现玻璃棒左端下降。 (1)、用酒精灯加热时,可观察到铜丝表面变色。(2)、将玻璃棒连同细绳取下,铜丝端浸入稀硫酸中,充分反应后取出,洗涤、干燥后再重新挂起(细绳系在玻璃棒的位置不变),玻璃棒 (填“能”或“不能”)再次保持水平。请写出涉及的化学方程式: 。24. 小婷和小彤在帮助老师整理药品时,发现有四瓶失去标签的溶液,只知道它们分别是氢氧化钙溶液、硫酸铜溶液、碳酸钠溶液和稀盐酸。小婷很快就判断出其中一瓶是硫酸铜溶液。小彤把其他三种溶液分别编号成A、B、C,然后两两混合进行如下实验:
(1)、用酒精灯加热时,可观察到铜丝表面变色。(2)、将玻璃棒连同细绳取下,铜丝端浸入稀硫酸中,充分反应后取出,洗涤、干燥后再重新挂起(细绳系在玻璃棒的位置不变),玻璃棒 (填“能”或“不能”)再次保持水平。请写出涉及的化学方程式: 。24. 小婷和小彤在帮助老师整理药品时,发现有四瓶失去标签的溶液,只知道它们分别是氢氧化钙溶液、硫酸铜溶液、碳酸钠溶液和稀盐酸。小婷很快就判断出其中一瓶是硫酸铜溶液。小彤把其他三种溶液分别编号成A、B、C,然后两两混合进行如下实验:实验
A+B
B+C
A+C
现象
无明显现象
有白色沉淀产生
有气体产生
据此,小彤很快就分辨出了三种未知溶液。回答下列问题:
(1)、小婷判断出硫酸铜溶液的依据是。(2)、C溶液中溶质的化学式是。(3)、A与B反应的基本类型是。(4)、B与C反应的化学方程式是。25. 将稀盐酸逐滴加入盛氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入氢氧化钠溶液的质量变化如图所示。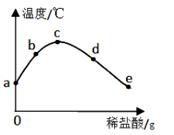 (1)、该反应的实质是。(2)、从a到c的过程中,溶液的pH值。(填“升高”“降低”或“不变”)(3)、图中各点中溶质种类完全相同的两点是。(填字母)26. 小科同学取了适量实验室制二氧化碳发生装置中的剩余溶液。逐滴滴加纯碱溶液,绘制产生沉淀的图象如甲图所示。
(1)、该反应的实质是。(2)、从a到c的过程中,溶液的pH值。(填“升高”“降低”或“不变”)(3)、图中各点中溶质种类完全相同的两点是。(填字母)26. 小科同学取了适量实验室制二氧化碳发生装置中的剩余溶液。逐滴滴加纯碱溶液,绘制产生沉淀的图象如甲图所示。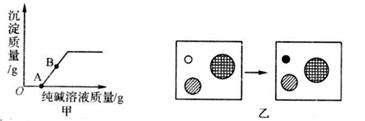 (1)、请写出B点对应溶液的溶质是(写化学式)。(2)、乙图是甲图中O点到A点的反应微观实质模型图。则“o”表示 (写化学符号)。(3)、写出OA之间发生的化学方程式。27. 某固体由 Ba2+、Cu2+、Na+、Cl-、 、 中的几种离子构成,取一定质量的该固体样品,进行如下实验:
(1)、请写出B点对应溶液的溶质是(写化学式)。(2)、乙图是甲图中O点到A点的反应微观实质模型图。则“o”表示 (写化学符号)。(3)、写出OA之间发生的化学方程式。27. 某固体由 Ba2+、Cu2+、Na+、Cl-、 、 中的几种离子构成,取一定质量的该固体样品,进行如下实验:①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。
则
(1)、该固体中一定含有的离子 ,(2)、请设计简单实验证明可能存在的离子。三、实验探究题
-
28. 一种制备氢氧化镁的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。
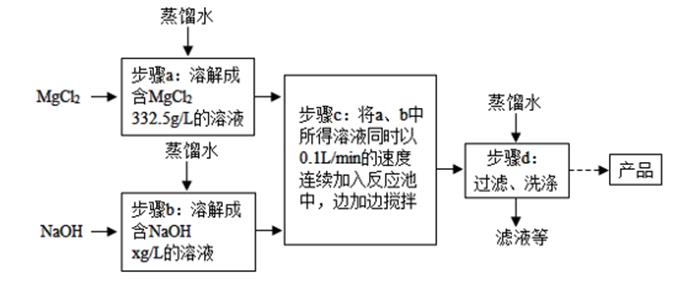 (1)、写出步骤c中发生反应的化学方程式:。(2)、x=。(3)、过滤得到的粗产品还要经过洗涤,检验洗涤是否完成的方案:。29. 小毛在做木炭还原氧化铜实验时,发现试管中的澄清石灰水变浑浊,且有气泡不断冒出。于是对“木炭和氧化铜反应生成铜和二氧化碳”这一结论提出质疑:①木炭在高温下与试管内空气中的氧气反应也能产生二氧化碳,那么,澄清的石灰水变浑浊,不能说明二氧化碳一定 是木炭和氧化铜反应产生的。
(1)、写出步骤c中发生反应的化学方程式:。(2)、x=。(3)、过滤得到的粗产品还要经过洗涤,检验洗涤是否完成的方案:。29. 小毛在做木炭还原氧化铜实验时,发现试管中的澄清石灰水变浑浊,且有气泡不断冒出。于是对“木炭和氧化铜反应生成铜和二氧化碳”这一结论提出质疑:①木炭在高温下与试管内空气中的氧气反应也能产生二氧化碳,那么,澄清的石灰水变浑浊,不能说明二氧化碳一定 是木炭和氧化铜反应产生的。②石灰水中不断有气泡冒出,不应该是二氧化碳。针对小毛的质疑,同学们进行了如下探究:
[建立假设]石灰水中不断冒出的气体是CO。
[查阅资料]CO气体能使湿润的黄色氯化钯试纸变蓝色。
[设计实验并操作]
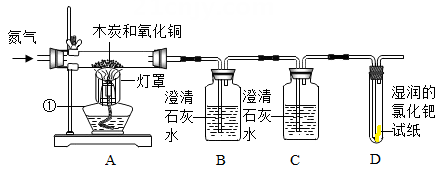
⑴组装仪器,如图所示,检查装置的气密性;
⑵在硬质玻璃管中装入一定比例氧化铜和木炭粉的混合物;
⑶在B、C中均放入澄清的石灰水,且B.中石灰水保证足量,D中放入湿润的氯化钯试纸
⑷先通入一会儿氮气,目的是;
[现象记录]A.中的黑色固体逐渐变成光亮的红色;B.中澄清的石灰水变浑浊,D.中湿润的黄色氯化钯试纸变成蓝色。
[得出结论]碳能与氧化铜反应产生二氧化碳的同时有一氧化碳生成。
[反思]同学们对CO产生的原因进行了分析:原因一是木炭和氧化铜在高温条件下直接发生反应产生CO;原因二是反应C+2CuO 2Cu+CO2↑ 中的一种产物和反应物木炭又发生了化学反应,产生了CO;
[评价]从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理:。由此,同学们想到如图装置设计中存在缺陷,改进方法是 。
30. 鉴别 5 瓶失去标签的溶液:稀盐酸、稀硫酸、NaOH 溶液、CuSO4 溶液和 BaCl2 溶液。(1)、观察 5 溶液的颜色,溶液呈色的是 CuSO4 溶液。(2)、取少量四种无色溶液分别放入四支试管中,再分别滴加 CuSO4 溶液,可鉴别出 NaOH溶液和 BaCl2 溶液。写出 CuSO4 和 NaOH 溶液反应的化学方程式。(3)、对剩余两瓶溶液如何进行鉴别,请简要写出鉴别方法:。(4)、实验结束后,将所有试管中的物质充分混合,过滤除去沉淀,得到无色滤液;取少量无色滤液滴加 Na2SO4 溶液,无明显现象,另取少量无色滤液分别与下列物质混合时,一定无明显现象的是 。A、酚酞溶液 B、Mg C、CuO D、Ba(OH)2 溶液 E、AgNO3 溶液四、解答题
-
31. 实验室模拟炼铁的实验装置如图所示。
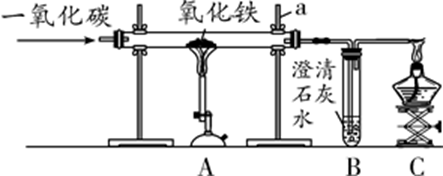 (1)、实验中看到的现象:玻璃管中的粉末。(2)、用600吨含氧化铁质量分数为80%的赤铁矿,可以炼出含杂质4%的生铁多少吨?(反应的化学方程式为3CO+Fe2O3 2Fe+3CO2)32. 钢铁的使用是人类文明和进步的重要标志。某钢铁公司用500吨含氧化铁(Fe2O3)64%的赤铁矿石进行炼铁,高炉炼铁的原理为3CO+Fe2O3 2Fe+3CO2。计算(1)、铁矿石中氧化铁的质量为吨;(2)、这些矿石理论上能炼得铁多少吨?(写出简明的计算过程)33. Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:
(1)、实验中看到的现象:玻璃管中的粉末。(2)、用600吨含氧化铁质量分数为80%的赤铁矿,可以炼出含杂质4%的生铁多少吨?(反应的化学方程式为3CO+Fe2O3 2Fe+3CO2)32. 钢铁的使用是人类文明和进步的重要标志。某钢铁公司用500吨含氧化铁(Fe2O3)64%的赤铁矿石进行炼铁,高炉炼铁的原理为3CO+Fe2O3 2Fe+3CO2。计算(1)、铁矿石中氧化铁的质量为吨;(2)、这些矿石理论上能炼得铁多少吨?(写出简明的计算过程)33. Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:加入稀硫酸的质量(g)
充分反应后剩余固体的质量(g)
第 1 次
40
m
第 2 次
40
14.8
第 3 次
40
12.2
第 4 次
40
11.2
第 5 次
40
11.2
试回答下列问题:
(1)、从以上数据可知,最后剩余的11.2g固体的成分是;表格中,m= .(2)、黄铜样品中锌的质量分数为 .(3)、计算所用稀硫酸中硫酸的质量分数是多少?34. 某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。回答下列问题: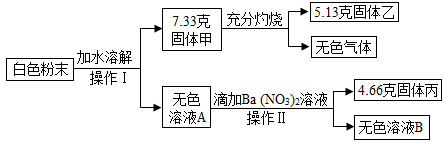 (1)、固体甲的成分是。(2)、无色气体的质量是多少克?(3)、白色粉末中肯定含有的物质总质量。
(1)、固体甲的成分是。(2)、无色气体的质量是多少克?(3)、白色粉末中肯定含有的物质总质量。