浙教版科学 八年级上册 第1章溶液计算
试卷更新日期:2022-09-21 类型:同步测试
一、单选题
-
1. 将80℃时的硝酸钾饱和溶液降温至20℃,析出晶体后得到的液体( )A、是水 B、是不饱和溶液 C、仍是饱和溶液 D、可能是饱和溶液2. 将20 ℃时某硝酸钾溶液均分为两份,第一份恒温蒸发掉10 g水,析出a g晶体;第二份恒温蒸发掉20 g水,析出晶体b g。则a与b的关系正确的是( )A、2a=b B、2a≤b C、2a≥b D、2a<b3. t℃时,将一定质量的某物质的不饱和溶液分成三等份,分别加热蒸发溶剂。然后把温度降至t ℃。已知从三份溶液中蒸发溶剂的质量分别为10 g、20 g、30 g,析出晶体(不含结晶水)的质量分别为a g、b g、c g,则a、b、c三者的关系是( )A、c=2b-a B、c=a+b C、c=a+2b D、c=2a+b4. 硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
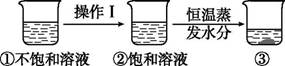 A、操作Ⅰ一定是降温,溶剂质量不变 B、②到③的操作也可以是降温 C、①与②的溶质质量分数相比,②一定比①大 D、②与③的溶质质量可能相等5. 如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态。分析实验过程,判断下列说法正确的是( )
A、操作Ⅰ一定是降温,溶剂质量不变 B、②到③的操作也可以是降温 C、①与②的溶质质量分数相比,②一定比①大 D、②与③的溶质质量可能相等5. 如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态。分析实验过程,判断下列说法正确的是( )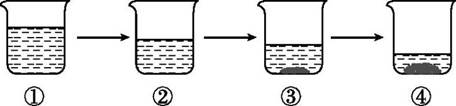 A、①→②过程中,氯化钠的质量分数保持不变 B、②→③过程中,氯化钠的溶解度不断增大 C、③→④过程中,水的质量分数不断增大 D、②→④过程中,氯化钠的质量分数先不变后增大6. 下列氯化钠溶液的溶质质量分数不是15%的是( )A、100 g水中溶解15 g氯化钠 B、氯化钠与水按15∶85的质量比形成的溶液 C、100 g溶液中含15 g氯化钠 D、30 g氯化钠溶解于170 g水中所形成的溶液7. 在一定的温度下,某物质的溶解度为S g,饱和溶液的溶质质量分数为A%,则S与A在数值上的关系是( )A、S=A B、S<A C、S>A D、无法确定8. 从10 g质量分数为10%的硝酸钾溶液中取出5 g,那么剩下的5 g硝酸钾溶液的质量分数为( )A、1% B、90% C、10% D、11.1%9. 向200 g溶质质量分数为10%的蔗糖溶液中加入200 g水,搅拌后把所得溶液倒出一半,剩余溶液的溶质质量分数为 ( )A、10% B、5% C、2.5% D、20%10. 在20 ℃时,可根据物质在100 g水中溶解的质量,将物质分为易溶、可溶、微溶、难溶四个等级,易溶物质是指( )A、小于0.01 g B、小于1 g C、大于1 g D、大于10 g11. 在一定温度下,若将某不饱和溶液蒸发15 g 水(部分)后,会析出2 g晶体(不含结晶水);若向原溶液投入5 g溶质晶体后,溶液中会剩下1 g固体溶质,则此温度下该溶质的溶解度为( )A、13.3 g B、26.7 g C、33.3 g D、40 g12. 将氢氧化钠固体加入到一定量蒸馏水中,不断搅拌,用温度传感器记录溶解过程中的温度变化,结果如图所示。图中a、c两点观察到溶液中有固体存在,b点固体完全消失。以下分析错误的是( )
A、①→②过程中,氯化钠的质量分数保持不变 B、②→③过程中,氯化钠的溶解度不断增大 C、③→④过程中,水的质量分数不断增大 D、②→④过程中,氯化钠的质量分数先不变后增大6. 下列氯化钠溶液的溶质质量分数不是15%的是( )A、100 g水中溶解15 g氯化钠 B、氯化钠与水按15∶85的质量比形成的溶液 C、100 g溶液中含15 g氯化钠 D、30 g氯化钠溶解于170 g水中所形成的溶液7. 在一定的温度下,某物质的溶解度为S g,饱和溶液的溶质质量分数为A%,则S与A在数值上的关系是( )A、S=A B、S<A C、S>A D、无法确定8. 从10 g质量分数为10%的硝酸钾溶液中取出5 g,那么剩下的5 g硝酸钾溶液的质量分数为( )A、1% B、90% C、10% D、11.1%9. 向200 g溶质质量分数为10%的蔗糖溶液中加入200 g水,搅拌后把所得溶液倒出一半,剩余溶液的溶质质量分数为 ( )A、10% B、5% C、2.5% D、20%10. 在20 ℃时,可根据物质在100 g水中溶解的质量,将物质分为易溶、可溶、微溶、难溶四个等级,易溶物质是指( )A、小于0.01 g B、小于1 g C、大于1 g D、大于10 g11. 在一定温度下,若将某不饱和溶液蒸发15 g 水(部分)后,会析出2 g晶体(不含结晶水);若向原溶液投入5 g溶质晶体后,溶液中会剩下1 g固体溶质,则此温度下该溶质的溶解度为( )A、13.3 g B、26.7 g C、33.3 g D、40 g12. 将氢氧化钠固体加入到一定量蒸馏水中,不断搅拌,用温度传感器记录溶解过程中的温度变化,结果如图所示。图中a、c两点观察到溶液中有固体存在,b点固体完全消失。以下分析错误的是( )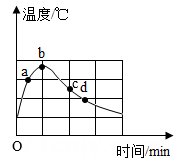 A、氢氧化钠固体溶于水会放热 B、a点时溶液质量分数比b点小 C、b点的溶液一定是饱和溶液 D、d点时的溶解度比c点小
A、氢氧化钠固体溶于水会放热 B、a点时溶液质量分数比b点小 C、b点的溶液一定是饱和溶液 D、d点时的溶解度比c点小二、填空题
-
13. 某温度下,将40 g食盐放到100 g水中,充分搅拌后溶解了36 g食盐,得到136 g食盐水。据此回答下列问题。(1)、食盐水中的溶质是 , 溶剂是。(2)、得到的溶液中,溶质质量为g,溶剂质量为g。(3)、将上述溶液分为四等份,每一份溶液中溶质质量为g,溶剂质量为g。14. 已知医用碘酒中碘的质量分数为2%,10 g碘可配制这种碘酒g,156.8 g酒精可配制这种碘酒g。15. t ℃时将12 g某物质溶于30 g水中,恰好配制成该温度下的饱和溶液,则t ℃时该物质的溶解度为g;现有该温度下该物质的饱和溶液210 g,则含溶质g,溶剂g。16. 将80克固体物质放入盛有50克水的烧杯中充分溶解,测得其溶液质量随温度变化的曲线如图所示。
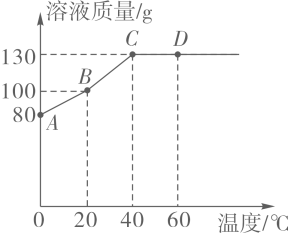 (1)、该固体物质的溶解度是随着温度的升高而 (选填“增大”或“减小”)。(2)、A点所对应的溶液中溶质与溶剂的质量之比是。(3)、从40℃到60℃的过程中,溶液的溶质质量分数 (选填“变大”、“不变”或“变小”)。
(1)、该固体物质的溶解度是随着温度的升高而 (选填“增大”或“减小”)。(2)、A点所对应的溶液中溶质与溶剂的质量之比是。(3)、从40℃到60℃的过程中,溶液的溶质质量分数 (选填“变大”、“不变”或“变小”)。三、实验探究题
-
17. 已知:氯化钠和硝酸钾在不同温度下的溶解度如下表。据表回答下列问题。
温度
10 ℃
20 ℃
30 ℃
40 ℃
50 ℃
60 ℃
70 ℃
80 ℃
氯化钠溶解度/g
35.8
36.0
36.3
36.6
37.0
37.3
37.8
38.4
硝酸钾溶解度/g
20.9
31.6
45.8
63.9
85.5
110
138
169
(1)、20 ℃时,将100 g氯化钠加入200 g水中,所得溶液的溶质与溶剂的质量比为(填最简整数比)。(2)、氯化钠中含有少量硝酸钾,要得到比较纯净的氯化钠,可以采用的方法是。(3)、20 ℃时将含有不溶性杂质的硝酸钾加入一定量的水中,充分搅拌后仍有100 g固体没有溶解。继续升高温度至60 ℃,充分搅拌后仍有60.8 g固体没有溶解。然后将混合物升温至80 ℃,再充分搅拌,恒温过滤,得到滤渣34.74 g则这一定量水的质量是g,原固体混合物中硝酸钾的质量分数为。四、解答题
-
18. 某温度下,将440 g A物质(不含结晶水)的水溶液分成等质量的2份。向第一份溶液中加入9 g A物质,充分搅拌,还有1 g固体不能溶解;将第二份溶液蒸发40 g水,并恢复到原温度,溶液恰好饱和(无A析出),则A物质在该温度下的溶解度是多少?原溶液的溶质质量分数是多少?(保留小数点后2位)19. 一定温度下,将425 g含有B物质的溶液蒸发300 g水后,溶液恰好饱和;若另取85 g原溶液,加入25 g B物质和40 g水充分搅拌后,溶液也恰好饱和。求该温度下B物质饱和溶液中溶质的质量分数是多少?20. 现有100 g溶质质量分数为15%的硝酸钾溶液,欲使其溶质质量分数增大到30%,当分别采取下列措施时,试计算:(1)、需向此溶液中加入多少克硝酸钾?(结果保留一位小数)(2)、需蒸发掉多少克水?(3)、需向此溶液中加入溶质质量分数为50%的硝酸钾溶液多少克?21. 将20 ℃时,100 g某硝酸钾不饱和溶液均分为两份,第一份恒温蒸发10 g水,析出5 g晶体;第二份恒温蒸发20 g水,析出15 g晶体。则原溶液的溶质质量是多少?22. 舟山海鲜闻名全国,但是有一些不法商贩为了获取暴利,会用福尔马林浸泡海鲜,以延长其保鲜时间,这对食用者的健康有很大损害。查阅资料发现福尔马林是浓度为35%-40%的甲醛溶液。在医学上,常用来浸泡病理切片及生物标本,请根据要求回答下列问题:(1)、实验室中,如果要配制100g质量分数为40%的福尔马林溶液,需要甲醛的质量方多少?(2)、如果将该溶液稀释为35%的溶液,需要加入多少毫升的水?(结果保留一位小数)23. 用氯化镁溶液喷洒路面可融雪、防尘。已知20℃时,氯化镁的溶解度为54.6g,在该温度下按下表数据配制溶液。
序号
①
②
③
④
氯化镁的质量/g
30
40
50
60
水的质量/g
100
100
100
100
(1)、所得溶液中,溶质与溶剂的质量比为1:2的是;(选填序号,下同)(2)、所得溶液中,属于饱和溶液的是;(3)、求序号为①所得溶液中溶质的质量分数。(结果保留到0.1%)五、综合题
-