2022-2023初中化学上学期第五单元化学方程式 课题1 质量守恒定律课堂训练
试卷更新日期:2022-09-15 类型:同步测试
一、单选题
-
1. 保护环境人人有责。一种廉价环保的新能源二甲醚,它完全燃烧时发生如下反应:X+3O22CO2+3H2O,则二甲醚(X)的化学式是( )A、C2H6O B、C2H6O2 C、C2H4O D、CH4O2. 一定条件下,在密闭容器内发生某一化学反应,测得反应前后各物质的质量如下表所示。
物质
甲
乙
丙
丁
反应前的质量/g
3.2
16.8
0.8
0.1
反应后的质量/g
x
8.4
3.0
1.0
下列说法不正确的是( )
A、x=8.5 B、反应中生成丙与丁的质量比为3:1 C、乙一定是化合物 D、丙和丁的相对分子质量之比可能为22:93. 如图是某密闭容器中物质变化过程的微观示意图,下列说法不正确的是( ) A、变化Ⅰ发生的反应是化合反应 B、变化Ⅰ过程中分子种类发生了变化 C、变化Ⅰ、Ⅱ、Ⅲ都是化学变化 D、反应中各物质都由分子构成4. 一氧化碳在充满氧气的密闭容器中燃烧,容器内有关的量随时间变化的图象正确的是( )A、
A、变化Ⅰ发生的反应是化合反应 B、变化Ⅰ过程中分子种类发生了变化 C、变化Ⅰ、Ⅱ、Ⅲ都是化学变化 D、反应中各物质都由分子构成4. 一氧化碳在充满氧气的密闭容器中燃烧,容器内有关的量随时间变化的图象正确的是( )A、 B、
B、 C、
C、 D、
D、 5. 最早的皮蛋制作方法用到炭灰(主要成分碳酸钾)和石灰(主要成分氧化钙)等原料,其中的反应为 , X可用于实验室制备二氧化碳,则m的数值是( )A、4 B、3 C、2 D、16. 化学反应前后,下列各项中肯定没有变化的是( )
5. 最早的皮蛋制作方法用到炭灰(主要成分碳酸钾)和石灰(主要成分氧化钙)等原料,其中的反应为 , X可用于实验室制备二氧化碳,则m的数值是( )A、4 B、3 C、2 D、16. 化学反应前后,下列各项中肯定没有变化的是( )①原子的数目 ②分子的数目 ③元素的种类 ④物质的总质量 ⑤物质的种类 ⑥原子的种类
A、①③⑤⑥ B、①②③⑤ C、①②④⑥ D、①③④⑥7. 在某H2O2溶液中,氢元素与氧元素的质量比为1:9,现向20g该H2O2溶液中加入少量氧化锰,充分反应后,生成氧气的质量为( )A、2 g B、4 g C、1.6g D、3.2g8. 用下列装置进行实验,不能用于验证质量守恒定律的是( )A、 B、
B、 C、
C、 D、
D、 9. 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,具有强氧化性,可与NH3发生化学反应:6ClO2+16NH3═5N2+6NH4Cl+12X。下列说法错误的是( )A、X的化学式是H2O B、NH3中氮元素的化合价为﹣3 C、NH4Cl中氯元素的质量分数最大 D、ClO2中氯、氧元素的质量比为71:3210. 化学变化遵守质量守恒定律。完成下面小题。(1)、下列燃料在O2中燃烧时,不会产生CO2的是( )A、天然气 B、煤 C、肼(N2H4) D、乙醇(C2H5OH)(2)、硅是重要的半导体材料。工业上制硅的生产流程中,其中一步反应的化学方程式为SiO2 + 2CSi + 2X,则X为( )A、SiC B、CO C、CO2 D、O2(3)、下列关于2CO + O2 2CO2的说法错误的是( )A、化学反应前后均含有碳元素和氧元素 B、化学反应前后碳原子个数不变 C、表示一氧化碳在氧气中燃烧生成二氧化碳 D、化学反应前后分子个数不变
9. 二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,具有强氧化性,可与NH3发生化学反应:6ClO2+16NH3═5N2+6NH4Cl+12X。下列说法错误的是( )A、X的化学式是H2O B、NH3中氮元素的化合价为﹣3 C、NH4Cl中氯元素的质量分数最大 D、ClO2中氯、氧元素的质量比为71:3210. 化学变化遵守质量守恒定律。完成下面小题。(1)、下列燃料在O2中燃烧时,不会产生CO2的是( )A、天然气 B、煤 C、肼(N2H4) D、乙醇(C2H5OH)(2)、硅是重要的半导体材料。工业上制硅的生产流程中,其中一步反应的化学方程式为SiO2 + 2CSi + 2X,则X为( )A、SiC B、CO C、CO2 D、O2(3)、下列关于2CO + O2 2CO2的说法错误的是( )A、化学反应前后均含有碳元素和氧元素 B、化学反应前后碳原子个数不变 C、表示一氧化碳在氧气中燃烧生成二氧化碳 D、化学反应前后分子个数不变二、填空题
-
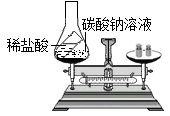
11. 某同学按图装置探究质量守恒定律,当稀盐酸与碳酸钠溶液混合后重新放回天平,观察到天平不平衡,请问天平指针向哪侧倾斜(“左侧”,“右侧”)?根据质量守恒定律解释原因?
 12. 化学反应 , 5.6gA和7.3gB恰好完全反应,生成12.7gC,则生成D的质量为g,现在要得到0.4gD,所需A的质量为g。13. 下图是某化学反应的微观示意图:
12. 化学反应 , 5.6gA和7.3gB恰好完全反应,生成12.7gC,则生成D的质量为g,现在要得到0.4gD,所需A的质量为g。13. 下图是某化学反应的微观示意图:
该反应中发生变化的粒子是(填“分子”或“原子”);写出该反应的化学方程式。
14. 氢气是理想的清洁高能燃料,以水为原料生产氢气的方法有多种。方法I:电解水法。写出电解水的化学方程式:。
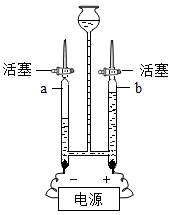
用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸以增强导电性;②a、b两试管内收集到的气体的体积比约为2︰1;③a试管内产生的气体能燃烧;④b试管内产生的气体具有可燃性。以上描述中正确的是(填序号)。
方法II:光解水法。我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“○”表示氢原子,“●”表示氧原子,“
 ”表示催化剂)
”表示催化剂)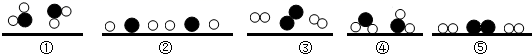 则水分解微观过程的正确顺序是(填序号)。上述过程中,不能再分的粒子是(填元素符号)。15. 质量守恒定律的发现,对科学的发展作出了重要贡献。
则水分解微观过程的正确顺序是(填序号)。上述过程中,不能再分的粒子是(填元素符号)。15. 质量守恒定律的发现,对科学的发展作出了重要贡献。①为了验证质量守恒定律,实验小组分别选取以下三组药品,通过称量比较各组物质在密闭容器内混合前后的总质量,能达到目的有。
A碘和酒精 B生石灰和水 C大理石和稀盐酸
②在一定条件下,A和B反应生成C,微粒种类变化如图所示(“
 ”、“
”、“  ”表示不同原子):
”表示不同原子):
则参加反应的A、B物质的分子数之比为 , A、B、C中属于化合物的是 , 对反应前后的分析错误的是。
a.元素种类没有改变 b.原子种类没有改变
c.原子个数没有改变 d.分子种类没有改变
三、简答题
-
16. 用质量守恒定律解释:铁丝在氧气中生成物的质量比参加铁丝的质量大。17. 请设计实验证明甲烷中含有碳元素和氢元素;乙醇的燃烧产物也是二氧化碳和水,是否可以由此说明甲烷和乙醇都是由碳元素和氢元素组成的碳氢化合物?为什么?
四、综合题
-
18. 回答问题(1)、如图是几种元素的粒子结构示意图及元素周期表的一部分。


①2021年2月27日,嫦娥五号采集的月壤样品在中国国家博物馆正式展出。月壤中存在着大量的氦﹣3(氦﹣3是含有2个质子和1个中子的氦原子),其原子结构示意图为图甲中的(选填字母编号)。
②硒是人体必需微量元素,具有防癌、抗癌作用,其原子结构示意图如图甲中的E,该元素处于元素周期表中第周期,它与图乙中(填元素名称)的化学性质相似。
③原子序数为13的元素与图甲中D元素组成化合物的化学式是。
(2)、石油中的氮元素在一定条件下转化为汽车尾气污染物的氨气(NH3)和一氧化氮(NO),这两种气体混合后能发生如图丙所示的反应。该反应中参加反应的氨气和一氧化氮的质量比为 , 此反应可以用于汽车尾气处理,其优点是(写出一条即可)。
五、实验探究题
-
19. 在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
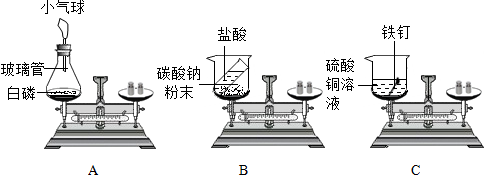 (1)、A实验;白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡,结论是:①质量不守恒。等锥形瓶冷却后,重新放在天平上称量,天平平衡,结论是:②质量守恒。你认为结论正确的是(填“①”或“②”),导致另一种结论不正确的原因是。(2)、B实验:乙组同学反应前调节天平平衡,然后将稀盐酸倒入烧杯中与碳酸钙充分反应后,再称量,观察到反应后天平不平衡,天平指针向(填“左”或“右”)偏转。同学们得到的结论是“实验B说明质量不守恒”,老师引导同学们分析了原因。你认为B实验天平不平衡的原因是。若要得到正确结论,该实验应该在装置中进行。(3)、由质量守恒定律可知,化学反应前后,一定不变的是(填序号)
(1)、A实验;白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡,结论是:①质量不守恒。等锥形瓶冷却后,重新放在天平上称量,天平平衡,结论是:②质量守恒。你认为结论正确的是(填“①”或“②”),导致另一种结论不正确的原因是。(2)、B实验:乙组同学反应前调节天平平衡,然后将稀盐酸倒入烧杯中与碳酸钙充分反应后,再称量,观察到反应后天平不平衡,天平指针向(填“左”或“右”)偏转。同学们得到的结论是“实验B说明质量不守恒”,老师引导同学们分析了原因。你认为B实验天平不平衡的原因是。若要得到正确结论,该实验应该在装置中进行。(3)、由质量守恒定律可知,化学反应前后,一定不变的是(填序号)①原子种类 ②原子数目 ③物质种类 ④原子质量 ⑤分子数目
20. 在“质量守恒定律”的课堂教学中,老师引导学生们进行“化学反应中,反应物与生成物的质量关系”实验探究。他们使用的实验装置和药品如下图所示,现分别以A、B、C表示。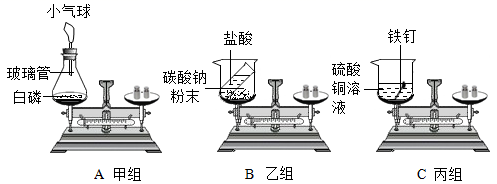 (1)、(实验验证)A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
(1)、(实验验证)A、B、C三个实验分别由甲、乙、丙三个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。A实验装置中小气球的作用是。
(2)、B实验反应后天平不平衡,指针向(填“左”或“右”)偏转,反应后天平不平衡的原因是。(3)、C实验反应前物质总质量反应后物质总质量(填“>”、“<”或“=”)。(4)、(反思与评价)上述实验A、B、C中能用来验证质量守恒定律的是(选填字母编号)。
(5)、在探究化学变化中反应物和生成物的质量关系时,若是有气体参加或有气体生成的反应,应采用容器。(6)、(拓展应用)下列事实遵守质量守恒定律的是(选填字母编号)。A.10g水受热变成10g水蒸气 B.蜡烛燃烧变短
C.酒精久置变轻 D.在一定条件下,石墨转化为金刚石
-