四川省宜宾市江安县2022年中考一模化学试题
试卷更新日期:2022-09-14 类型:中考模拟
一、单选题
-
1. 2022年2月4日20点,万众瞩目的第二十四届冬奥会在北京隆重开幕。在冬奥会开幕盛典中发生的化学变化是( )A、LED屏幕发光 B、点燃火炬 C、雕刻会徽 D、洒水制冰2. 北京冬奥会餐厅共配备了120台制餐机器人,预备了678道世界特色菜品,例如西湖牛肉羹。其主要原料牛肉富含的营养素为( )A、蛋白质 B、糖类 C、油脂 D、维生素3. 下列实验操作正确的是( )A、稀释浓硫酸
 B、测某溶液的pH
B、测某溶液的pH C、吸取稀盐酸
C、吸取稀盐酸 D、检查装置气密性
D、检查装置气密性 4. 化学用语是学习化学的基本工具,下列化学用语与含义相符的是( )A、2Fe2+:2个铁离子 B、小苏打:Na2CO3 C、2Ag:2个银原子 D、Mg+2:一个镁离子带2个单位正电荷5.
4. 化学用语是学习化学的基本工具,下列化学用语与含义相符的是( )A、2Fe2+:2个铁离子 B、小苏打:Na2CO3 C、2Ag:2个银原子 D、Mg+2:一个镁离子带2个单位正电荷5.化学思想方法是化学实验探究的重要方法,其中之一为控制变量法.如图探究影响反应速率的因素是( )
 A、温度 B、盐酸浓度 C、催化剂 D、固体质量6. 下列符合“安全、健康、绿色、环保”的生产生活理念的是( )A、煤气泄漏,开灯检查 B、福尔马林浸泡肉类,延长保质期 C、植树造林,防沙降尘 D、大力提倡焚烧秸秆,增肥环保7. “微观-宏观-符号”三重表征是化学独特的表示物质及其变化的方法。某反应的微观过程如图所示,其中“
A、温度 B、盐酸浓度 C、催化剂 D、固体质量6. 下列符合“安全、健康、绿色、环保”的生产生活理念的是( )A、煤气泄漏,开灯检查 B、福尔马林浸泡肉类,延长保质期 C、植树造林,防沙降尘 D、大力提倡焚烧秸秆,增肥环保7. “微观-宏观-符号”三重表征是化学独特的表示物质及其变化的方法。某反应的微观过程如图所示,其中“ ”代表一个碳原子,“
”代表一个碳原子,“ ”代表一个氧原子,“
”代表一个氧原子,“ ”代表一个氢原子。下列说法正确的是( )
”代表一个氢原子。下列说法正确的是( ) A、二氧化碳由1个碳原子和2个氧原子构成 B、反应前后原子种类、数目没有改变 C、参加反应的二氧化碳和氢气的分子个数比为1:1 D、反应中氢气和水的质量比为1:98. 下列排序正确的是( )A、空气中气体体积分数:
A、二氧化碳由1个碳原子和2个氧原子构成 B、反应前后原子种类、数目没有改变 C、参加反应的二氧化碳和氢气的分子个数比为1:1 D、反应中氢气和水的质量比为1:98. 下列排序正确的是( )A、空气中气体体积分数: B、地壳中元素含量:
B、地壳中元素含量: C、金属活动性:
C、金属活动性: D、将等量物质溶解在等量的20℃的水中,溶液温度:
D、将等量物质溶解在等量的20℃的水中,溶液温度: 9. 构建元素化合价和物质类别的二维图是学习化学的一种重要方法。下图是硫元素的类价二维图。下列认识错误的是( )
9. 构建元素化合价和物质类别的二维图是学习化学的一种重要方法。下图是硫元素的类价二维图。下列认识错误的是( ) A、物质X在氧气中燃烧产生微弱的淡蓝色火焰 B、物质Y是造成酸雨的气体之一 C、物质Z可用于金属除锈 D、由图可知:同种元素在不同物质中的化合价可能不同10. 比利时化学家研发了一种将木质素低聚物通过镍作催化剂除去甲基,从而生产苯酚、丙烯和乙烯等化工产品的工艺。如图是镍元素在元素周期表中的信息以及原子结构示意图。下列说法错误的是( )
A、物质X在氧气中燃烧产生微弱的淡蓝色火焰 B、物质Y是造成酸雨的气体之一 C、物质Z可用于金属除锈 D、由图可知:同种元素在不同物质中的化合价可能不同10. 比利时化学家研发了一种将木质素低聚物通过镍作催化剂除去甲基,从而生产苯酚、丙烯和乙烯等化工产品的工艺。如图是镍元素在元素周期表中的信息以及原子结构示意图。下列说法错误的是( ) A、镍的质子数是28 B、图中X的数值是2 C、镍元素位于元素周期表中第四周期 D、镍的相对原子质量为58.69g11. 已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法错误的是( )
A、镍的质子数是28 B、图中X的数值是2 C、镍元素位于元素周期表中第四周期 D、镍的相对原子质量为58.69g11. 已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法错误的是( )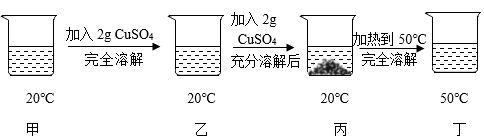 A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大12. 我国古代将炉甘石(ZnCO3)和木炭粉混合后,加热到约800℃可得到锌。主要发生的化学反应:① , ② , 下列说法正确的是( )A、X的化学式为CO B、反应①是分解反应,反应②是置换反应 C、反应前后固体的质量均不变 D、反应②可证明木炭具有氧化性13. 下列实验操作不能达到实验目的的是( )
A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大12. 我国古代将炉甘石(ZnCO3)和木炭粉混合后,加热到约800℃可得到锌。主要发生的化学反应:① , ② , 下列说法正确的是( )A、X的化学式为CO B、反应①是分解反应,反应②是置换反应 C、反应前后固体的质量均不变 D、反应②可证明木炭具有氧化性13. 下列实验操作不能达到实验目的的是( )选项
物质
目的
主要实验操作
A
硬水和软水
鉴别
取样,分别加适量肥皂水振荡,观察现象
B
二氧化碳
检验
将气体通入澄清石灰水,观察现象
C
CO2(CO)
除杂
将气体点燃
D
铁粉和氧化铜粉末
分离
用磁铁吸引
A、A B、B C、C D、D14. 人类常利用化学反应得到所需要的物质,如图是X、Y、Z、W四种物质的转化关系(都能通过一步反应实现),则X、Y、Z、W依次可能是( ) A、C、CO、CO2、H2CO3 B、H2O2、O2、H2O、H2 C、CaO、Ca(OH)2、CaCl2、CaCO3 D、Cu、CuO、Cu(OH)2、CuSO4
A、C、CO、CO2、H2CO3 B、H2O2、O2、H2O、H2 C、CaO、Ca(OH)2、CaCl2、CaCO3 D、Cu、CuO、Cu(OH)2、CuSO4二、填空题
-
15. “变化观念与平衡思想”是化学核心素养之一,这要求我们多角度认识物质,以全面了解物质世界,下图以盐酸为例,回答下列问题。
 (1)、认识物质的组成:稀盐酸中的溶质是(填化学式)(2)、认识物质的性质:打开浓盐酸的瓶盖,观察到瓶口有产生,说明浓盐酸具有挥发性。(3)、认识物质的变化:
(1)、认识物质的组成:稀盐酸中的溶质是(填化学式)(2)、认识物质的性质:打开浓盐酸的瓶盖,观察到瓶口有产生,说明浓盐酸具有挥发性。(3)、认识物质的变化:①盐酸使某指示剂变成了红色,该指示剂为(填字母)。
a、无色酚酞溶液 b、紫色石蕊溶液
②将金属甲、乙放入足量的稀盐酸中,观察到的现象如下:
甲表面有气泡产生且溶液变为浅绿色,乙无明显现象。由此推断金属甲、乙活动性顺序为(由强到弱)。写出金属甲与盐酸反应的化学方程式:。
③当胃酸过多时,可服用氢氧化铝中和胃酸,氢氧化铝属于(氧化物、酸、碱、盐)
④盐酸能与某些盐反应,请例举一种能与盐酸反应且产生气体的盐(填化学式)
(4)、认识物质的用途:盐酸可用于除铁锈,反应的化学方程式为:。三、科普阅读题
-
16. 阅读下面科普短文。
2022年2月4日晚,北京冬奥会开幕式在北京国家体育馆“鸟巢”盛大举行,其精彩绝伦,未来感十足的呈现,震撼刷屏,惊艳全球。北京作为全世界唯一的“双奥之城”被载入史册。
材料(一):“水立方”变成“冰立方”,千余辆氢能大巴穿梭于赛场,3大赛区26场馆实现100%绿电供应……中国以实际行动兑现了“绿色办奥”的庄严承诺,从能源、场馆、交通、碳汇四方面入手,推出了18项碳减排、4项碳中和措施,使北京冬奥会成为迄今为止首个“碳中和”的冬奥会。
材料(二):走进国家速滑馆“冰丝带”,映入眼帘的是一整块1.2万平方米的冰面,这是目前世界上采用二氧化碳跨临界直冷制冰技术打造的最大的多功能全冰面。常温常压下的二氧化碳是气态,施加一定压力后,可以液化成液体甚至凝华为固体,压力降低后,液态或固态的二氧化碳又能快速汽化(或升华)为气体,并大量吸热,从而达到降低环境温度的目的,被誉为是“最快的冰”。
材料(三):冬奥火炬“飞扬”外形极具动感和活力,象征冰火相约,激情飞扬,照亮冰雪,温暖世界”。它是由碳纤维与高性能树脂结合制作而成,质量只有钢的1/4左右,但是强度是钢的7-9倍,通过将碳纤维丝立体三维编织,最终像“织毛衣”一样织成了火炬外壳。“飞扬”采用氢气作为燃料,不但保证了火炬能在极寒天气中使用而且环保。高压储氢技术、大比例氢减压技术以及氢燃烧技术,完美地诠释了绿色奥运、科技
奥运的理念。回答下列问题:
(1)、上述材料中的“碳减排”“碳中和”中的“碳”是指(填物质名称)。氢能大巴采用“氢腾”系列燃料电池发动机将能转化为电能为氢能大巴车提供动力。(2)、材料(二)中固态二氧化碳的俗称。二氧化碳加压液化时,分子间隔(选填“变大”“不变“变小”)。(3)、材料(三)中冬奥火炬“飞扬”由碳纤维与高性能树脂结合制作而成,该材料属于____。A、塑料 B、金属材料 C、复合材料(4)、“飞扬”以氢气作为燃料,下图是制取与贮存氢气的一种方法。回答下列问题:
①ZnFe2O4中Fe的化合价为。ZnFe2O4中铁、氧元素的质量比为。
②反应3中氩气作保护气,目的是防止。
③反应3是Mg2Cu合金贮氢过程,其反应的化学方程式。
四、综合题
-
17. 以黄铁矿(主要成分为FeS2 , 含有少量SiO2杂质)为原料制备氯化铁晶体(FeCl3·6H2O),焙烧产生的SO2可用于工业制备硫酸。工艺流程分别如图1、图2所示:


已知:①SiO2难溶于水和酸;②HI在常态下是一种有刺激性气味的无色气体;回答下列问题
(1)、配平黄铁矿焙烧的化学方程式。(2)、试剂a是。操作I的名称为。(3)、制备硫酸的工业流程中,可循环利用的物质是。分离器中发生的变化属于变化(“化学”“物理”)。反应器中发生反应的化学方程式为。(4)、膜反应器中发生的反应为分解反应,其化学方程式为。(5)、制备硫酸的工业流程中会产生的废气SO2 , 废水中含有硫酸。以下想法不妥的是____(填序号)。A、废气可以回收再利用 B、废气可以点燃后排放 C、废水用熟石灰中和后排放 D、改进工艺,减少废气废水的排放18. 实验室常用溶质质量分数为6%的H2O2溶液(MnO2作催化剂)制取少量氧气。(1)、配制6%的H2O2稀溶液:①计算:市售H2O2溶液质量分数通常为30%。配制100g6%的H2O2溶液,需要向30%的H2O2溶液中加入水的质量为g。
②配制:量取所需H2O2溶液和水于烧杯中,用(填仪器名称)搅拌,充分混合。
(2)、制取氧气(可能用到的部分装置如图)
①实验室用H2O2制取氧气的化学方程式为 , 可选择的发生装置为(填字母)。
②若用C装置干燥氧气,则C中盛放的试剂为。(填试剂名称)
③若用D装置收集氧气,则气体应从导管(填“a”或“b”)端通入。
(3)、拓展延伸:若直接用30%的H2O2溶液制取氧气,反应速率太快。为获得平稳的气流,如图所示发生装置能达到最佳效果的是(填字母)。
 19. 某实验小组发现老师实验篮中有瓶标签受损、久置的某溶液,受损标签如下图所示。该小组同学对这瓶溶液进行了如下探究:
19. 某实验小组发现老师实验篮中有瓶标签受损、久置的某溶液,受损标签如下图所示。该小组同学对这瓶溶液进行了如下探究:
【提出问题】这瓶溶液是什么物质的溶液呢?
【猜想与假设】老师提示:原溶液只可能是下列三种溶液中的一种:
①氢氧化钠溶液 ②碳酸钠溶液 ③硫酸钠溶液
【查阅资料】Na2SO4溶液和BaCl2溶液均呈中性
(1)、【实验探究一】同学
实验操作
实验现象
实验结论
同学相互评价
甲

图1
溶液变红
甲同学得出:
样品溶液呈性;猜想①成立
乙同学认为此方案结论不正确,他的理由是。乙同学设计了如图2的实验
乙

图2
乙同学观察到试管中。
乙同学得出:猜想②成立
丙同学认为:猜想①的溶液久置可能变质,加足量稀盐酸也能观察到此现象,并设计了【实验探究二】继续探究
(2)、【实验探究二】丙同学设计的实验方案如下:实验操作
实验现象
实验结论或结果
步骤一:取少量样品溶液于试管中,加入过量BaCl2溶液,振荡
。
猜想①正确,且已部分变质。步骤二完毕后,溶液中除酚酞外,还含有的溶质有(填化学式)。
步骤二:静置,取少量上层清液于另一支试管中,滴加2-3滴酚酞溶液
。
(3)、【交流与讨论】大家认为丙同学的实验方案仍然存在缺陷,如果氢氧化钠溶液已完全变质,则无法得出正确结论。
【实验反思】
①甲同学:碱性溶液碱溶液(“一定是”“不一定是”“一定不是”)
②乙同学:氢氧化钠溶液必须要保存,其变质的化学方程式为。
三丙同学:为避免标签腐蚀,倾倒液体试剂时应注意。
五、计算题
-
20. 某炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐滴加入质量分数为9.8%的稀硫酸,测出溶液的pH随加入稀硫酸的质量变化关系如图所示。(提示:炉具清洁剂中的其余成分不与稀硫酸反应,且呈中性)请完成下列问题。
 (1)、当恰好反应时,消耗稀硫酸的质量为g。(2)、当pH=13时,溶液中所含的溶质是(填化学式,不考虑清洁剂中的其余成分)。(3)、计算该炉具清洁剂中氢氧化钠的质量分数。(写出计算过程)
(1)、当恰好反应时,消耗稀硫酸的质量为g。(2)、当pH=13时,溶液中所含的溶质是(填化学式,不考虑清洁剂中的其余成分)。(3)、计算该炉具清洁剂中氢氧化钠的质量分数。(写出计算过程)
-
-