青海省西宁市2022年中考一模化学试题
试卷更新日期:2022-09-08 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、雪糕融化 B、木炭燃烧 C、湿衣服晾干 D、矿石粉碎2. 下列物质加入足量的水中能形成紫红色溶液的是( )A、酒精 B、植物油 C、高锰酸钾 D、大理石3. 化学的学习离不开实验,而实验成功的关键在于操作。下列实验操作正确的是( )A、
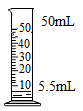 量取5.5mL液体
B、
量取5.5mL液体
B、 称量NaCl的质量
C、
称量NaCl的质量
C、 稀释浓硫酸
D、
稀释浓硫酸
D、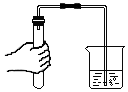 检查装置气密性
4. 空气的成分中,体积分数约占78%的是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体5. 在太空舱里,常用NiFe2O4 作催化剂将宇航员呼出的 CO2转化为 O2 , NiFe2O4中 Fe 的化合价为+3,则 Ni的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列对相关实验现象的描述完全正确的是( )A、向澄清石灰水中滴加无色酚酞试液,溶液变红 B、电解水实验中正极与负极产生的气体体积之比为8:1 C、把银片浸入硫酸铜溶液一段时间,银片表面有红色物质析出 D、镁条在空气中燃烧,发出耀眼的白光,生成一种黑色固体,放出热量7. 下列物质存放在烧杯中一段时间后,质量变小且不变质的是( )A、烧碱 B、浓硫酸 C、浓盐酸 D、生石灰8. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
检查装置气密性
4. 空气的成分中,体积分数约占78%的是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体5. 在太空舱里,常用NiFe2O4 作催化剂将宇航员呼出的 CO2转化为 O2 , NiFe2O4中 Fe 的化合价为+3,则 Ni的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列对相关实验现象的描述完全正确的是( )A、向澄清石灰水中滴加无色酚酞试液,溶液变红 B、电解水实验中正极与负极产生的气体体积之比为8:1 C、把银片浸入硫酸铜溶液一段时间,银片表面有红色物质析出 D、镁条在空气中燃烧,发出耀眼的白光,生成一种黑色固体,放出热量7. 下列物质存放在烧杯中一段时间后,质量变小且不变质的是( )A、烧碱 B、浓硫酸 C、浓盐酸 D、生石灰8. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A、X、Y、Z B、Z、Y、X C、Y、X、Z D、X、Z、Y9. 传统中药“金银花”的有效成分中含有一种名为绿原酸(C16H18O9)的物质,下列说法正确的是( )A、绿原酸由三种元素组成 B、绿原酸的相对分子质量为354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成10. 近年来科学家在“甲烷-二氧化碳重整和Ni基催化剂”的研究方面取得突破。下图是甲烷与二氧化碳反应的微观示意图,下列说法错误的是( ) A、丙物质是CO B、反应前后各元素的化合价均不变 C、参加反应的甲和乙的质量比为4:11 D、生成物中的两种分子的个数比为1:111. 如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH4NO3固体后,甲中未观察到明显现象。下列说法正确的是( )
A、丙物质是CO B、反应前后各元素的化合价均不变 C、参加反应的甲和乙的质量比为4:11 D、生成物中的两种分子的个数比为1:111. 如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH4NO3固体后,甲中未观察到明显现象。下列说法正确的是( ) A、乙中溶液一定变浑浊 B、甲中溶液一定变成饱和溶液 C、乙中溶液溶质的质量分数一定变小 D、甲、乙中溶液质量一定相等12. 归纳推理是化学学习中常用的思维方法,下列推理正确的是( )A、铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀 B、置换反应中有元素化合价改变,凡有元素化合价改变的反应一定是置换反应 C、常温下,pH<7的溶液显酸性,因此pH<7的雨水一定都是酸雨 D、化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物13. 化学实验的设计能力是化学学习的关键能力之一。下列实验方案可行的是( )
A、乙中溶液一定变浑浊 B、甲中溶液一定变成饱和溶液 C、乙中溶液溶质的质量分数一定变小 D、甲、乙中溶液质量一定相等12. 归纳推理是化学学习中常用的思维方法,下列推理正确的是( )A、铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀 B、置换反应中有元素化合价改变,凡有元素化合价改变的反应一定是置换反应 C、常温下,pH<7的溶液显酸性,因此pH<7的雨水一定都是酸雨 D、化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物13. 化学实验的设计能力是化学学习的关键能力之一。下列实验方案可行的是( )选项
实验设计
实验目的
A
用pH试纸测试肥皂水的pH
测定肥皂水的酸碱度
B
将带火星的木条伸入气体中
检验二氧化碳中混有少量氧气
C
将气体通过灼热铜丝网
除去CO2中混有的少量CO
D
将固体加水溶解,然后过滤
提纯混有少量硝酸钾的氯化钠固体
A、A B、B C、C D、D二、填空题
-
14. 按要求写出相应的化学符号(1)、两个氯原子;(2)、碱溶液中的阴离子;(3)、5个亚铁离子;(4)、标出硝酸铜中铜元素的化合价。15. 下图是A、B、C、D四种粒子的结构示意图。
 (1)、A,B,C,D共表示种元素;D中x=。(2)、由A,C两种元素组成的化合物的化学式为。16. 如图是a、b、c三种物质的溶解度曲线,回答下列问题:
(1)、A,B,C,D共表示种元素;D中x=。(2)、由A,C两种元素组成的化合物的化学式为。16. 如图是a、b、c三种物质的溶解度曲线,回答下列问题: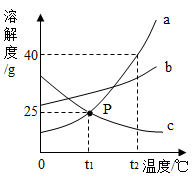 (1)、P点的含义是。(2)、t2℃时,将50克a物质加入到100克水中,充分溶解后,所得溶液的质量是克。(3)、t2℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为。17. 请用化学知识回答下列问题。(1)、用盐酸可除去铁表面的铁锈,反应的化学方程式是。(2)、长期饮用硬水对人体健康不利,要降低水的硬度,在家庭里通常采用的方法。(3)、为了防止家中常用的铁锅生锈,你的做法是。(4)、人们通常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有作用。18. 从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
(1)、P点的含义是。(2)、t2℃时,将50克a物质加入到100克水中,充分溶解后,所得溶液的质量是克。(3)、t2℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为。17. 请用化学知识回答下列问题。(1)、用盐酸可除去铁表面的铁锈,反应的化学方程式是。(2)、长期饮用硬水对人体健康不利,要降低水的硬度,在家庭里通常采用的方法。(3)、为了防止家中常用的铁锅生锈,你的做法是。(4)、人们通常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有作用。18. 从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。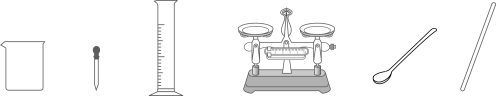 (1)、需要称量NaCl的质量为g。(2)、量取水用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。
(1)、需要称量NaCl的质量为g。(2)、量取水用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。三、综合题
-
19. A~H都是初中化学中常见的物质,已知A、B为黑色固体,D为红色固体单质,F为红色粉末,它们的转化关系如图所示.请回答:
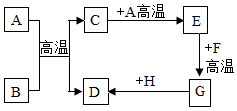 (1)、写出E+F→G的化学方程式;(2)、写出一个能实现G生成D的化学方程式 , 该反应属于反应(填基本反应类型)。20. 如图所示,某实验小组的同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
(1)、写出E+F→G的化学方程式;(2)、写出一个能实现G生成D的化学方程式 , 该反应属于反应(填基本反应类型)。20. 如图所示,某实验小组的同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。 (1)、Ⅰ、从微观角度分析,中和反应的实质是。(2)、Ⅱ、探究烧杯内溶液中溶质的成分:
(1)、Ⅰ、从微观角度分析,中和反应的实质是。(2)、Ⅱ、探究烧杯内溶液中溶质的成分:【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想①:可能是NaCl和NaOH;
猜想②:可能只有NaCl;
猜想③:可能是。
(3)、【查阅资料】氯化钠溶液呈中性。【进行实验】
实验方案
实验操作
实验现象
实验结论
方案一
取少量烧杯内溶液于试管,滴入几滴酚酞溶液,振荡
溶液色
猜想①不正确
方案二
取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
猜想②不正确,猜想③正确
(4)、【反思与拓展】①在分析化学反应后所得物质成分时,除考虑生成物外还需考虑。
②根据所学化学知识,验证烧杯内溶液中溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?(填序号)。
A pH试纸B 铜C 紫色石蕊溶液
21. 根据下列仪器装置,回答问题:
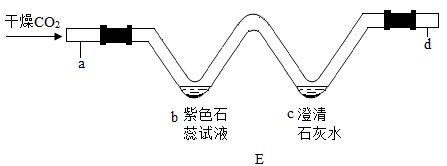 (1)、写出仪器e的名称。(2)、实验室用MnO2和双氧水制取O2 , 反应的化学方程式为;装入药品前必须进行的操作是;实验室制取并收集H2可选用的装置(填字母序号)。(3)、实验室可用(填物质名称)干燥CO2。用装置E进行CO2的部分性质实验:将干燥的紫色石蕊试纸放在(选填“a”“d”)处,并与b处现象对比,可说明CO2能与水反应;c处发生反应的化学方程式为。
(1)、写出仪器e的名称。(2)、实验室用MnO2和双氧水制取O2 , 反应的化学方程式为;装入药品前必须进行的操作是;实验室制取并收集H2可选用的装置(填字母序号)。(3)、实验室可用(填物质名称)干燥CO2。用装置E进行CO2的部分性质实验:将干燥的紫色石蕊试纸放在(选填“a”“d”)处,并与b处现象对比,可说明CO2能与水反应;c处发生反应的化学方程式为。四、计算题
-
22. 某化验室为了测定工厂废液中残余硫酸的含量,取该废液100g,向其中滴加10%的氢氧化钠溶液40g后,溶液恰好呈中性(废液中除硫酸外其它成分不与氢氧化钠反应)。该废液中残余硫酸的质量分数是多少?