四川省巴中市2022年中考化学真题
试卷更新日期:2022-09-08 类型:中考真卷
一、单选题
-
1. 以下巴中特产制作过程中涉及到化学变化的是( )A、制作腊肉时将成品切块包装 B、酿造白酒的发酵过程 C、制作中草药时晾干水分 D、制作豆腐时用纱布滤浆2. 下列食物中蛋白质含量最高的是( )A、大米 B、西红柿 C、大豆 D、菜籽油3. 为了推进垃圾分类工作,把生活垃圾按图示进行科学分类处理,实行“定时、定点”投放。手机废旧电池属于( )A、
 可回收物
B、
可回收物
B、 其他垃圾
C、
其他垃圾
C、 有害垃圾
D、
有害垃圾
D、 厨余垃圾
4. 为了防止天然气漏造成危险,可在家中安装报警器,如图安装位置最合理的是( )
厨余垃圾
4. 为了防止天然气漏造成危险,可在家中安装报警器,如图安装位置最合理的是( ) A、a处 B、b处 C、c处 D、以上各处都可以5. 下列说法错误的是( )A、家中使用的保鲜膜属于有机合成材料 B、自制简易净水器中活性炭的主要作用是杀菌、消毒 C、“大漠孤烟直”中的“烟,是固体小颗粒悬浮在空气中形成的现象 D、车用乙醇汽油中乙醇属于可再生能源6. 下列判断正确的是( )A、含氧元素的化合物一定是氧化物 B、生成盐和水的反应都是中和反应 C、只含一种元素的物质一定是单质 D、含碳元素的化合物不一定是有机物7. 规范的实验操作是实验成功的保证,下列实验操作不规范的是( )A、
A、a处 B、b处 C、c处 D、以上各处都可以5. 下列说法错误的是( )A、家中使用的保鲜膜属于有机合成材料 B、自制简易净水器中活性炭的主要作用是杀菌、消毒 C、“大漠孤烟直”中的“烟,是固体小颗粒悬浮在空气中形成的现象 D、车用乙醇汽油中乙醇属于可再生能源6. 下列判断正确的是( )A、含氧元素的化合物一定是氧化物 B、生成盐和水的反应都是中和反应 C、只含一种元素的物质一定是单质 D、含碳元素的化合物不一定是有机物7. 规范的实验操作是实验成功的保证,下列实验操作不规范的是( )A、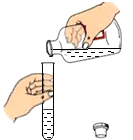 倾倒液体
B、
倾倒液体
B、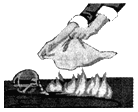 酒精灯失火用湿抹布扑盖
C、
酒精灯失火用湿抹布扑盖
C、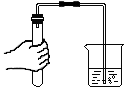 气密性检查
D、
气密性检查
D、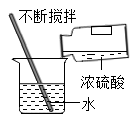 稀释浓硫酸
8. “丹砂烧之成水银”中的“丹砂”指的是硫化汞。该反应的微观示意图如图,有关说法正确的是( )
稀释浓硫酸
8. “丹砂烧之成水银”中的“丹砂”指的是硫化汞。该反应的微观示意图如图,有关说法正确的是( ) A、“
A、“ ”代表非金属单质汞
B、反应前后的原子种类发生了改变
C、此反应属于置换反应
D、反应前后各元素的化合价都不变
9. 如图为KNO3、NaCl两种物质的溶解度曲线,下列说法正确的是( )
”代表非金属单质汞
B、反应前后的原子种类发生了改变
C、此反应属于置换反应
D、反应前后各元素的化合价都不变
9. 如图为KNO3、NaCl两种物质的溶解度曲线,下列说法正确的是( ) A、a1℃时,向100g水中加入20gKNO3 , 充分溶解后所得溶液是饱和溶液 B、KNO3和NaCl的溶解度相等 C、当KNO3中含有少量NaCl时,可以用蒸发结晶的方法提纯KNO3 D、将a2℃时等质量的NaCl与KNO3的饱和溶液降温到a1℃,所得溶液中溶质质量NaCl大于KNO310. 常温下取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明稀盐酸和氢氧化钠恰好完全反应的是( )A、加入碳酸钙粉末,有气泡产生 B、加入AgNO3溶液,有白色沉淀产生 C、加入酚酞溶液,溶液显红色 D、测定溶液的pH,pH=711. 下列实验方案不合理的是( )A、除去CO2中少量的HCl气体,通过足量的NaOH溶液 B、除去CaO中少量的CaCO3 , 高温煅烧至质量不变 C、鉴别NaCl固体和NH4NO3固体,加水溶解,感知温度变化 D、鉴别羊毛线和棉线,灼烧、闻气味12. 取少量实验室制取CO2后的废液,向其中加入紫色石蕊溶液变成红色。现另取一定质量的废液于烧杯中,向其中逐渐加入碳酸钠粉末,如图:横坐标表示加入的碳酸钠粉末的质量,根据图像判断,纵坐标可能表示( )
A、a1℃时,向100g水中加入20gKNO3 , 充分溶解后所得溶液是饱和溶液 B、KNO3和NaCl的溶解度相等 C、当KNO3中含有少量NaCl时,可以用蒸发结晶的方法提纯KNO3 D、将a2℃时等质量的NaCl与KNO3的饱和溶液降温到a1℃,所得溶液中溶质质量NaCl大于KNO310. 常温下取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明稀盐酸和氢氧化钠恰好完全反应的是( )A、加入碳酸钙粉末,有气泡产生 B、加入AgNO3溶液,有白色沉淀产生 C、加入酚酞溶液,溶液显红色 D、测定溶液的pH,pH=711. 下列实验方案不合理的是( )A、除去CO2中少量的HCl气体,通过足量的NaOH溶液 B、除去CaO中少量的CaCO3 , 高温煅烧至质量不变 C、鉴别NaCl固体和NH4NO3固体,加水溶解,感知温度变化 D、鉴别羊毛线和棉线,灼烧、闻气味12. 取少量实验室制取CO2后的废液,向其中加入紫色石蕊溶液变成红色。现另取一定质量的废液于烧杯中,向其中逐渐加入碳酸钠粉末,如图:横坐标表示加入的碳酸钠粉末的质量,根据图像判断,纵坐标可能表示( ) A、溶液中溶剂的质量 B、烧杯中固体的质量 C、溶液的pH D、溶液中溶质的质量
A、溶液中溶剂的质量 B、烧杯中固体的质量 C、溶液的pH D、溶液中溶质的质量二、填空题
-
13. 我国著名的化工专家侯德榜,为纯碱和氮肥工业的发展作出了杰出的贡献。侯氏制碱法的原理为:
NaCl+NH3+CO2+H2O═NH4Cl+NaHCO3↓
2NaHCO3Na2CO3+CO2↑+H2O
(1)、Na2CO3属于(选填“酸”“碱”或“盐”),溶于水形成的溶液显性,其用途(任写一条)。(2)、NH3中氮元素的化合价是价。(3)、写出碳酸钠溶液与澄清石灰水反应的化学方程式。(4)、NaHCO3是发酵粉的主要成分,它与厨房中食醋的主要成分反应如下: NaHCO3+CH3COOH═CH3COONa+X+CO2↑,则X为(填化学式)。(5)、请设计实验方案鉴别NaCl固体和NH4Cl固体。(写出操作、现象、结论)14. 现有A、B、C、D、E、F六种元素。其中A元素原子的原子核中没有中子;B是地壳中含量最多的元素;C元素原子的核电荷数为17;D元素组成的单质是目前世界上年产量最高的金属;E是“司母戊鼎”中的一种金属元素,其单质呈紫红色;F元素形成的单质在空气中燃烧、发出耀眼的白光。(1)、下列属于B元素的原子结构示意图是。 (2)、写出由A、B两种元素形成的常见阴离子的符号。(3)、D元素的单质与A、C元素形成化合物的水溶液反应的化学方程式。(4)、人体缺D元素可能会引起。(5)、为了判断D、E、F元素形成的三种单质的活动性强弱,设计了如下实验方案(方案中的单质经过打磨处理)、其中合理的是。
(2)、写出由A、B两种元素形成的常见阴离子的符号。(3)、D元素的单质与A、C元素形成化合物的水溶液反应的化学方程式。(4)、人体缺D元素可能会引起。(5)、为了判断D、E、F元素形成的三种单质的活动性强弱,设计了如下实验方案(方案中的单质经过打磨处理)、其中合理的是。①把形状、大小相同的D、E、F元素形成的单质分别放入同浓度同体积的稀硫酸中
②把F元素形成的单质分别放入含D的低价盐溶液和E的盐溶液中
③把D元素形成的单质分别放入含E、F的盐溶液中
④把E、F元素形成的两种单质分别放入含D的低价盐溶液中
三、综合题
-
15. 某兴趣小组用氯酸钾和二氧化锰制取氧气。可能用到实验装置如图所示:

请回答下列问题:
(1)、a仪器的名称。(2)、写出用该方法制取氧气的化学方程式 , 其中二氧化锰的作用是 , 制取并收集干燥的氧气应选用(填实验装置图字母序号)。(3)、氯酸钾完全分解后,为了回收二氧化锰和氯化钾,又进行了如下实验操作:
实验操作中,操作①的名称是;实验操作②应选择上述图中的(填实验装置图字母序号)。
(4)、实验结束后,同学们在拆卸装置时闻到刺激性气味。他们将回收得到的MnO2称量,发现其质量小于加热前MnO2的质量。查阅资料后发现,加热KClO3和MnO2混合物的反应过程如下:第一步:2MnO2+2KClO32KMnO4+Cl2↑+O2↑
第二步:2KMnO4K2MnO4+MnO2+O2↑
第三步:K2MnO4+Cl22KCl+MnO2+O2↑
拆卸装置时闻到刺激性气味的气体是 , 根据以上信息写出加热后剩余固体中MnO2质量小于加热前MnO2质量的原因。
16. 天然气的主要成分为甲烷,燃烧可能会产生CO,为了检验天然气燃烧后的气体产物成分,进行如下实验: (1)、实验开始时,点燃D处酒精灯之前,先通一会儿N2 , 其目的是。(2)、A中无水CuSO4变蓝,说明气体产物中含有水;B中澄清石灰水变浑浊,证明气体产物中含有(填化学式)。(3)、C装置中发生反应的化学方程式为。(4)、实验中观察到D装置中 , E装置中 , 说明气体产物中还有CO。(5)、F处为尾气处理装置,下列装置中合理的是。
(1)、实验开始时,点燃D处酒精灯之前,先通一会儿N2 , 其目的是。(2)、A中无水CuSO4变蓝,说明气体产物中含有水;B中澄清石灰水变浑浊,证明气体产物中含有(填化学式)。(3)、C装置中发生反应的化学方程式为。(4)、实验中观察到D装置中 , E装置中 , 说明气体产物中还有CO。(5)、F处为尾气处理装置,下列装置中合理的是。
四、计算题
-
17. 粮食安全是国家安全的重要基础,化肥对提高粮食产量有重要作用。尿素【CO(NH2)2】是常用的氮肥之一,可促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量。已知:2NH3+CO2CO(NH2)2+H2O(1)、尿素中氮元素的质量分数为(结果精确到0.1%)。(2)、巴中某农业合作社需要12吨尿素,请计算合成这些尿素需要CO2的质量是多少吨。(写出计算过程)