湖南省株洲市2022年初中学业水平模拟化学试题
试卷更新日期:2022-08-31 类型:中考模拟
一、单选题
-
1. 下列过程中发生了化学变化的是( )A、轮胎爆炸 B、油污乳化 C、石油的炼制 D、生石灰吸水2. 下列实验操作正确的是( )A、
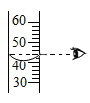 量筒读数
B、
量筒读数
B、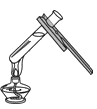 加热液体
C、
加热液体
C、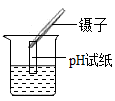 测定溶液的酸碱度
D、
测定溶液的酸碱度
D、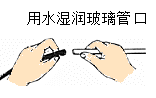 连接仪器
3. 认识物质是学习化学的基础,下列物质属于化合物的是( )A、空气 B、干冰 C、液氧 D、生铁4. 空气是一种宝贵的自然资源。下列有关空气的说法中错误的是( )A、植树造林、种草,可以保护空气 B、氧气在空气中的体积分数为78% C、氮气在焊接金属时常用作保护气 D、空气中二氧化碳的含量是相对稳定的5. 在太空舱里,常用NiFe2O4 作催化剂将宇航员呼出的 CO2转化为 O2 , NiFe2O4中 Fe 的化合价为+3,则 Ni的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列用微粒观点解释错误的是( )A、氮原子和磷原子属于不同种元素——质子数不同 B、端午时节,粽叶飘香——分子总是在不断运动着 C、酸有相似的化学性质——酸溶液中都含有H+ D、压瘪的乒乓球放入热水中重新鼓起——分子的体积增大7. 初中我们学过四种基本反应类型,下列选项中属于化合反应的是( )A、赤铁矿石炼铁的原理 B、工业制取二氧化碳 C、小苏打治疗胃酸过多 D、铝制品表面形成薄膜8. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
连接仪器
3. 认识物质是学习化学的基础,下列物质属于化合物的是( )A、空气 B、干冰 C、液氧 D、生铁4. 空气是一种宝贵的自然资源。下列有关空气的说法中错误的是( )A、植树造林、种草,可以保护空气 B、氧气在空气中的体积分数为78% C、氮气在焊接金属时常用作保护气 D、空气中二氧化碳的含量是相对稳定的5. 在太空舱里,常用NiFe2O4 作催化剂将宇航员呼出的 CO2转化为 O2 , NiFe2O4中 Fe 的化合价为+3,则 Ni的化合价为( )A、+4 B、+3 C、+2 D、+16. 下列用微粒观点解释错误的是( )A、氮原子和磷原子属于不同种元素——质子数不同 B、端午时节,粽叶飘香——分子总是在不断运动着 C、酸有相似的化学性质——酸溶液中都含有H+ D、压瘪的乒乓球放入热水中重新鼓起——分子的体积增大7. 初中我们学过四种基本反应类型,下列选项中属于化合反应的是( )A、赤铁矿石炼铁的原理 B、工业制取二氧化碳 C、小苏打治疗胃酸过多 D、铝制品表面形成薄膜8. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下: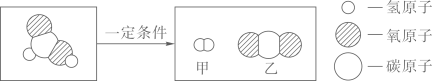
下列说法正确的是( )
A、甲酸分子中氢、氧原子个数比为1:2 B、乙中碳、氧元素质量比为1:2 C、46g甲酸中氢元素质量为2g D、生成甲与乙的分子个数比为2:19. 科学家利用“基因剪刀”技术降低了水稻中砷的含量。结合图示,有关砷的说法正确的是 ( )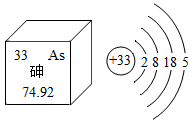 A、属于金属元素 B、中子数为 33 C、原子质量为 74.92 g D、砷元素位于元素周期表中第Ⅳ周期10. 火的使用标志着人类文明的伟大进步。下列说法错误的是( )A、图书馆失火可用二氧化碳灭火器扑灭 B、炒菜时油锅着火,立即盖上锅盖,使可燃物隔绝氧气而灭火 C、燃气灶火焰出现黄色,锅底出现黑色时,可增大灶具进风口 D、当可燃物的温度达到着火点时即可燃烧11. 家庭中一些常见物质的 pH 如下表所示:夏天我们被蚊虫叮咬后,蚊虫会在人的皮肤内分泌蚁酸(一种酸),从而使皮肤肿痛。要减轻痛痒,可在叮咬处涂抹下列物质中的( )
A、属于金属元素 B、中子数为 33 C、原子质量为 74.92 g D、砷元素位于元素周期表中第Ⅳ周期10. 火的使用标志着人类文明的伟大进步。下列说法错误的是( )A、图书馆失火可用二氧化碳灭火器扑灭 B、炒菜时油锅着火,立即盖上锅盖,使可燃物隔绝氧气而灭火 C、燃气灶火焰出现黄色,锅底出现黑色时,可增大灶具进风口 D、当可燃物的温度达到着火点时即可燃烧11. 家庭中一些常见物质的 pH 如下表所示:夏天我们被蚊虫叮咬后,蚊虫会在人的皮肤内分泌蚁酸(一种酸),从而使皮肤肿痛。要减轻痛痒,可在叮咬处涂抹下列物质中的( )物质
食醋
酱油
食盐水
氢氧化钠
肥皂水
pH
2~3
4~5
7
10~13
9~10
A、食醋 B、酱油 C、肥皂水 D、食盐水12. 化学与日常生活有着密切的联系,下列说法错误的是( )A、生活中通过煮沸可以降低水的硬度 B、农业上可以利用熟石灰来改良酸性土壤 C、在金属表面刷漆可以防止金属的锈蚀 D、人类获得能量都是通过化学变化13. 化肥对提高农作物的产量具有重要作用。下列不属于复合肥料的是( )A、(NH4)2HPO4 B、KH2PO4 C、KNO3 D、NH4NO314. 下列实验现象的描述正确的是( )A、木炭在氧气中燃烧生成二氧化碳 B、打开盛有浓盐酸的瓶盖,瓶口出现大量白雾 C、点燃塑料和羊毛都产生烧焦羽毛的气味 D、红磷燃烧时发出蓝紫色火焰,产生白色固体15. 将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:物质
a
b
c
d
反应前的质量/g
6.4
14.0
3.2
1.0
反应一段时间后的质量/g
10.0
7.2
X
1.0
下列有关说法正确的是( )
A、a和b是反应物 B、X=3.2 C、该反应属于分解反应 D、d一定是催化剂16. 已知某无色溶液中大量共存的物质有 KNO3、NaOH、X、Ba(NO3)2 , 其中 X 可能是( )A、CuCl2 B、K2CO3 C、NaNO3 D、MgSO417. 下列各组物质的反应,需要加入酸碱指示剂才能判断反应是否发生的是( )A、Fe和硫酸铜溶液 B、Zn和稀硫酸 C、氢氧化钠溶液和稀盐酸 D、澄清石灰水和二氧化碳18. 向182.5g一定浓度的盐酸中加入足量的锌粉,反应后最终溶液质量为214g,盐酸的溶质质量分数为( )A、10% B、37% C、20% D、36.5%二、多选题
-
19. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中错误的是( )
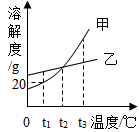 A、t1℃时,50g甲的饱和溶液中溶解了10g 的甲 B、将 t2℃时的甲、乙两种物质的饱和溶液升温至 t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 C、t2℃时,要使接近饱和的乙溶液达到饱和状态,可以采用蒸发溶剂的方法 D、甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法提纯乙20. 为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )
A、t1℃时,50g甲的饱和溶液中溶解了10g 的甲 B、将 t2℃时的甲、乙两种物质的饱和溶液升温至 t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 C、t2℃时,要使接近饱和的乙溶液达到饱和状态,可以采用蒸发溶剂的方法 D、甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法提纯乙20. 为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )选项
物质(杂质)
操作方式
A
CO2(水蒸气)
通过装有浓硫酸的洗气瓶
B
O2(N2)
缓慢通过灼热铜网
C
NaOH 溶液(Na2CO3)
滴加适量的氯化钡溶液,过滤
D
BaCl2 溶液(HCl)
加入足量 BaCO3 固体充分反应后过滤
A、A B、B C、C D、D三、填空题
-
21. 请用化学符号填空。(1)、任意一种制取氧气的盐;(2)、任意一种气体单质;(3)、任意一种酸根离子。22. 下图为 A、B、C、D、E 五种粒子的结构示意图,请按要求填空:
 (1)、x的值是。(2)、微粒 D 和 E 形成化合物的化学式为。(3)、A,B,C,D,E五种粒子对应的元素有种。23. 如图是甲、乙两种物质的溶解度曲线如图。
(1)、x的值是。(2)、微粒 D 和 E 形成化合物的化学式为。(3)、A,B,C,D,E五种粒子对应的元素有种。23. 如图是甲、乙两种物质的溶解度曲线如图。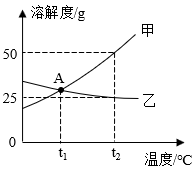 (1)、A 点的含义是。(2)、t2℃时,甲、乙两种固体各 8 g 分别投入 25 g 水中,充分搅拌。(填 “甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质g 可使其达到饱和。24. 我国自行研发的大型客机 C919 于去年 5 月成功试飞,请根据所学知识回答问题。(1)、选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度(填“大于”或“小于”)纯铝。(2)、飞机上所用的下列材料属于金属材料的是____(填序号)A、真皮座套 B、陶瓷坐便器 C、塑料扶手 D、铜制扣件(3)、飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与接触。25. 在探究金属活动性顺序时,华雪同学把两根绕成螺旋状的洁净铜丝分别浸入硫酸铝溶液、硝酸银溶液中,过一会儿取出:(1)、铜丝浸入硝酸银溶液中,可观察到铜丝上有色物质生成,溶液逐渐变成色。(2)、铜丝浸入硝酸银溶液中,离子数目减少的是 , 离子数目增加的是。26. 华为公司作为我国高科技的代表,一直致力于核心技术的开发。华为公司推出了 5G 商用芯片。制造芯片需要用到高纯硅,工业上利用二氧化硅制备高纯硅的工艺流程如下图:
(1)、A 点的含义是。(2)、t2℃时,甲、乙两种固体各 8 g 分别投入 25 g 水中,充分搅拌。(填 “甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入溶质g 可使其达到饱和。24. 我国自行研发的大型客机 C919 于去年 5 月成功试飞,请根据所学知识回答问题。(1)、选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度(填“大于”或“小于”)纯铝。(2)、飞机上所用的下列材料属于金属材料的是____(填序号)A、真皮座套 B、陶瓷坐便器 C、塑料扶手 D、铜制扣件(3)、飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与接触。25. 在探究金属活动性顺序时,华雪同学把两根绕成螺旋状的洁净铜丝分别浸入硫酸铝溶液、硝酸银溶液中,过一会儿取出:(1)、铜丝浸入硝酸银溶液中,可观察到铜丝上有色物质生成,溶液逐渐变成色。(2)、铜丝浸入硝酸银溶液中,离子数目减少的是 , 离子数目增加的是。26. 华为公司作为我国高科技的代表,一直致力于核心技术的开发。华为公司推出了 5G 商用芯片。制造芯片需要用到高纯硅,工业上利用二氧化硅制备高纯硅的工艺流程如下图: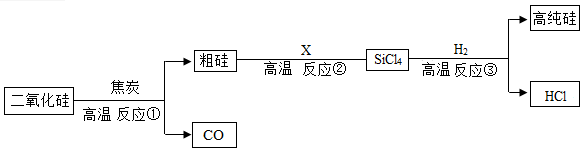 (1)、写出反应③的化学方程式 , 该反应属于 (填基本反应类型)反应。(2)、玻璃的主要成分是二氧化硅,二氧化硅(SiO2)与氢氧化钠溶液反应类似于二氧化碳与氢氧化钠溶液的 反应。请写出二氧化硅与氢氧化钠溶液反应的化学方程式。27. 在抗击新冠病毒时 84 消毒液”可作环境消毒剂,其有效成分为次氯酸钠(NaClO)。如图为一种制取“84 消毒液”的简化流程:
(1)、写出反应③的化学方程式 , 该反应属于 (填基本反应类型)反应。(2)、玻璃的主要成分是二氧化硅,二氧化硅(SiO2)与氢氧化钠溶液反应类似于二氧化碳与氢氧化钠溶液的 反应。请写出二氧化硅与氢氧化钠溶液反应的化学方程式。27. 在抗击新冠病毒时 84 消毒液”可作环境消毒剂,其有效成分为次氯酸钠(NaClO)。如图为一种制取“84 消毒液”的简化流程: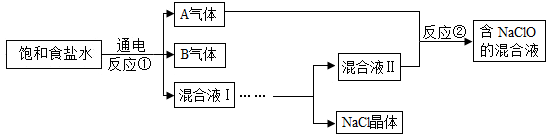
图中 A,B 气体均为单质,混合液Ⅰ、Ⅱ的溶质均为 NaOH 和 NaCl。回答下列问题:
(1)、B 气体是一种新型能源,也可作燃料。与其它燃料相比,其优点有(写一点即可)。(2)、反应①的化学方程式为。(3)、混合液Ⅰ经蒸发浓缩、冷却结晶、后得到混合液Ⅱ和 NaCl 晶体。(4)、混合液Ⅱ中 NaOH 与 A 气体发生反应②,产生 NaClO、NaCl 和 H2O,该反应的化学方程式为。(5)、“84 消毒液”与洁厕灵混用时会产生有毒的 Cl2 , 其化学方程式为:NaClO+2HCl=NaCl+Cl2↑+ H2O,对该反应的分析正确的是 (填选填序号)。a. NaClO、H2O 均为氧化物
b.不属于任何基本反应类型
c.只有氯元素的化合价发生了改变
28. 请用所学的知识回答下列问题:(1)、用石灰浆粉刷墙壁,干燥后墙面就变硬了,请用化学原理解释该现象。(2)、现有一瓶蒸馏水和氯化钾溶液,请用两种方法把它们鉴别开。29. 在实验室,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选用的装置如图所示: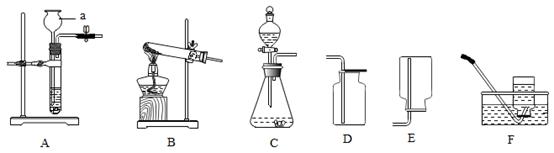 (1)、写出仪器a的名称为。(2)、若要制取并收集一瓶CO2 , 不可以选择的装置是(填图中装置对应的字母)。(3)、CO2是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO2确实能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。请回答下列问题:
(1)、写出仪器a的名称为。(2)、若要制取并收集一瓶CO2 , 不可以选择的装置是(填图中装置对应的字母)。(3)、CO2是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO2确实能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。请回答下列问题: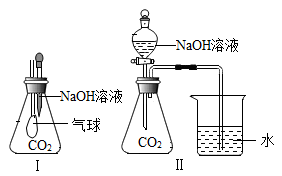
①选择装置I时,可观察到的实验现象为:。
②选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是:。
③CO2和NaOH溶液反应的化学方程式为。
30. CuSO4是一种常见的重要的化合物,多角度看物质可以提高对该物质的认识。(1)、从类别看,CuSO4属于(填“酸”或“碱”或“盐”或“氧化物”).(2)、从用途看,CuSO4可配制一种农业上常用的杀菌剂波尔多液;从组成看,CuSO4、Na2SO4均属同一系列化合物,已知 Na2SO4溶于水显中性,那 CuSO4 溶于水显什么性呢?在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个 “意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式;
(3)、【提出问题】该气体是什么呢?【猜想与假设】猜想一:O2猜想二:H2猜想三:CO2猜想四:SO2
同学们经过讨论,一致认为猜想不成立,理由是。
(4)、【实验验证】1有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是。
2将产生的气体经后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰。
【实验结论】该气体是 H2。
(5)、【反思与交流】CuSO4溶液可能显性(填“酸”或“碱”或“中”);要使由硫酸和硫酸铜组成的混合溶液中的溶质只有硫酸铜,可向其中加入过量的物质有多种,例如(用化学方程式表示)。(6)、宏观辨识与微观探析是重要的化学学科核心素养之一,请你从微观上探析CuSO4溶液的酸碱性的初步原因:实验步骤
实验现象
实验结论
取适量 Na2SO4 溶液于试管中, 滴加石蕊试液,振荡
Na+和与溶液的酸碱性无关,说明CuSO4 溶液的酸碱性与(写离子符号)有关。
四、计算题