河南省新乡市新乡县2022年中考模拟化学试题
试卷更新日期:2022-08-31 类型:中考模拟
一、单选题
-
1. 嫦娥五号带回月壤成功后,实验中学举办多种以“嫦娥五号”为主题的活动庆贺,下列活动中,属于化学变化的是( )A、主题班会 B、主题制陶 C、主题板报 D、主题作文2. 悠久的历史造就了河南异常丰富的特产。下列特产中富含维生素的是( )A、开封花生 B、汴梁西瓜 C、郑州烩面 D、道口烧鸡3. 下列各组物质中,都由分子构成的一组是()A、铁、汞 B、氨、干冰 C、水、金刚石 D、硫酸铜、氯化钠4. 工业上用CH4和CO2制取合成气会产生积碳,如图是抗积碳示意图。有关说法错误的是( )
 A、Ni基双金属催化剂可重复使用 B、反应前后元素的化合价均改变 C、反应前后原子种类和数目不变 D、合成气可合成多种化工产品,价值大5. “民以食为天,食以安为先”。下列关于农药、化肥的说法正确的是( )A、农药施用后,会通过农作物、农产品等发生转移 B、为增强肥效,应将硫酸铵与熟石灰混合施用 C、尿素( )是一种常用的复合肥料 D、农药有毒、应禁止施用农药6. 下列化学方程式的书写和对反应类型的判断,都正确的是( )A、 化合反应 B、 分解反应 C、 置换反应 D、 复分解反应7. 科学家设计了“人造树叶”模拟光合作用,其装置和反应的微观示意图如图。下列说法错误的是( )
A、Ni基双金属催化剂可重复使用 B、反应前后元素的化合价均改变 C、反应前后原子种类和数目不变 D、合成气可合成多种化工产品,价值大5. “民以食为天,食以安为先”。下列关于农药、化肥的说法正确的是( )A、农药施用后,会通过农作物、农产品等发生转移 B、为增强肥效,应将硫酸铵与熟石灰混合施用 C、尿素( )是一种常用的复合肥料 D、农药有毒、应禁止施用农药6. 下列化学方程式的书写和对反应类型的判断,都正确的是( )A、 化合反应 B、 分解反应 C、 置换反应 D、 复分解反应7. 科学家设计了“人造树叶”模拟光合作用,其装置和反应的微观示意图如图。下列说法错误的是( ) A、反应最终生成两种分子 B、该过程实现了能量的转化 C、反应前后催化剂的化学性质不变 D、该设计为缓解温室效应提供了新途径8. 自来水厂净水过程示意图如下,下列说法正确的是( )
A、反应最终生成两种分子 B、该过程实现了能量的转化 C、反应前后催化剂的化学性质不变 D、该设计为缓解温室效应提供了新途径8. 自来水厂净水过程示意图如下,下列说法正确的是( )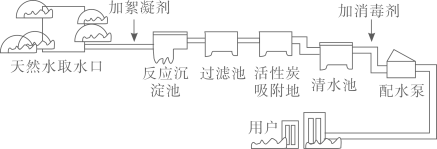 A、明矾是一种常用的絮凝剂 B、过滤可除去水中杂质离子 C、活性炭可长期使用无需更换 D、经该净水过程得到的是( )纯水9. 下列化肥属于含磷复合肥料的是( )A、KNO3 B、CO(NH2)2 C、K2HPO4 D、Ca(H2PO4)210. 下列物质分类正确的是( )A、石油、煤、甲烷﹣﹣化石燃料 B、过氧化氢、二氧化硅、铁锈﹣﹣氧化物 C、碳酸钙、葡萄糖、蛋白质﹣﹣有机物 D、HNO3、H2SO4、CH3COOH﹣﹣酸11. 某物质的溶解度曲线如图所示,下列说法正确的是( )
A、明矾是一种常用的絮凝剂 B、过滤可除去水中杂质离子 C、活性炭可长期使用无需更换 D、经该净水过程得到的是( )纯水9. 下列化肥属于含磷复合肥料的是( )A、KNO3 B、CO(NH2)2 C、K2HPO4 D、Ca(H2PO4)210. 下列物质分类正确的是( )A、石油、煤、甲烷﹣﹣化石燃料 B、过氧化氢、二氧化硅、铁锈﹣﹣氧化物 C、碳酸钙、葡萄糖、蛋白质﹣﹣有机物 D、HNO3、H2SO4、CH3COOH﹣﹣酸11. 某物质的溶解度曲线如图所示,下列说法正确的是( ) A、该物质在热水中的溶解度比在冷水中的小 B、20℃时,该物质的饱和溶液中溶质质量分数为28.6% C、20℃时,将该物质的溶液升高温度,溶质的质量分数一定增大 D、将70℃时该物质的不饱和溶液转化为饱和溶液,采用升温或降温的方法都不一定有效12. 按图所示进行实验。当观察到热水大面积变成红色时,冷水中只有品红周围变成红色。对该现象的微观解释合理的是( )
A、该物质在热水中的溶解度比在冷水中的小 B、20℃时,该物质的饱和溶液中溶质质量分数为28.6% C、20℃时,将该物质的溶液升高温度,溶质的质量分数一定增大 D、将70℃时该物质的不饱和溶液转化为饱和溶液,采用升温或降温的方法都不一定有效12. 按图所示进行实验。当观察到热水大面积变成红色时,冷水中只有品红周围变成红色。对该现象的微观解释合理的是( ) A、温度越高,分子质量越小 B、温度越高,分子体积越大 C、温度越高,分子间隔越小 D、温度越高,分子运动越快13. 下列图像能正确反应其对应关系的是( )A、
A、温度越高,分子质量越小 B、温度越高,分子体积越大 C、温度越高,分子间隔越小 D、温度越高,分子运动越快13. 下列图像能正确反应其对应关系的是( )A、 表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
B、
表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
B、 表示发生的反应为:
C、
表示发生的反应为:
C、 表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
D、
表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
D、 表示向盛有MnO2的烧杯中加入H2O2溶液
14. 某兴趣小组在研究Fe﹣Al合金、Fe﹣Cu合金、Zn﹣Cu合金、Zn﹣Fe合金时,发现其中一种合金2.5g与足量稀盐酸充分反应产生了0.2g气体,该合金可能是( )A、Fe﹣Al合金 B、Fe﹣Cu合金 C、Zn﹣Cu合金 D、Zn﹣Fe合金
表示向盛有MnO2的烧杯中加入H2O2溶液
14. 某兴趣小组在研究Fe﹣Al合金、Fe﹣Cu合金、Zn﹣Cu合金、Zn﹣Fe合金时,发现其中一种合金2.5g与足量稀盐酸充分反应产生了0.2g气体,该合金可能是( )A、Fe﹣Al合金 B、Fe﹣Cu合金 C、Zn﹣Cu合金 D、Zn﹣Fe合金二、计算题
-
15. 在一定质量的某BaCl2溶液中加入足量的Na2SO4溶液,所得BaSO4 , 沉淀质量等于原BaCl2溶液质量的1/4。则原BaCl2溶液中溶质的质量分数约为(保留到0.1%)。
三、填空题
-
16. 一定条件下,4.8g CH4与16.0g O2恰好完全反应,生成10.8g H2O、4.4g CO2和物质X.则X的质量为 g;该反应方程式中O2与X化学计量数之比为 .17. 牛尊是目前殷墟发现的唯一一件牛形青铜器。如图所示是铜元素在元素周期表中的部分信息。铜的相对原子质量为;比较铜与青铜的硬度,可采用的方法为。
 18. 二氧化氯(ClO2)是安全消毒剂,杀菌能力优于氯气(Cl2),可由NaClO2与Cl2反应制得。(1)、配平化学方程式:2NaClO2+Cl2═2ClO2+aNaCl。则a等于 。(2)、71g Cl2完全反应,理论上最多生成ClO2的质量为 g。19. NaOH、KNO3和Na2CO3在不同温度下的溶解度如表所示。
18. 二氧化氯(ClO2)是安全消毒剂,杀菌能力优于氯气(Cl2),可由NaClO2与Cl2反应制得。(1)、配平化学方程式:2NaClO2+Cl2═2ClO2+aNaCl。则a等于 。(2)、71g Cl2完全反应,理论上最多生成ClO2的质量为 g。19. NaOH、KNO3和Na2CO3在不同温度下的溶解度如表所示。物质
溶解度/g
温度℃
0
10
20
30
40
NaOH
42.0
51.0
109.0
119.0
129.0
KNO3
13.3
20.9
31.6
45.8
63.9
Na2CO3
6.0
16.0
18.0
36.5
50.0
下列实验过程中不考虑化学变化、水的蒸发和结晶水合物等因素。
(1)、10℃时,KNO3的溶解度 (填“>”,“<”或“=”)Na2CO3的溶解度。(2)、20℃时,将129gNaOH固体加入到100g水中,搅拌后固体全部消失,放置到t1时刻开始析出固体,到t2时刻析出10g固体为 (填“饱和”或“不饱和”)溶液。t2时刻溶液的温度为℃。(3)、40℃时,将等质量的三种物质的饱和溶液冷却到30℃,所得溶液中溶剂质量最多______ (填序号)。A、Na2CO3溶液 B、KNO3溶液 C、NaOH溶液20. 金属与人类的生产、生活密切相关,请回答下列问题:(1)、铁制品容易锈蚀,请写出铁生锈的条件。(2)、如图为实验室模拟工业炼铁的反应过程,写出工业炼铁的反应原理(用化学方程式表示)。 21. 化学与我们的生活、生产息息相关。(1)、小满时节,为促进农作物生长,可施用的化肥有:尿素[CO(NH2)2],硝酸钠(NaNO3),硫酸钾(K2SO4),其中属于钾肥的是。(2)、目前我国已掌握在-269℃下加压,将氦气转化为液氦的技术,该转化过程属于(填“物理变化”或“化学变化”)。22. 酸、碱、盐在生产、生活中有广泛的应用。(1)、下列关于酸、碱、盐的说法错误的是______。A、浓氨水具有挥发性 B、用食醋可除去水壶中的水垢 C、发明联合制碱法的科学家是侯德榜 D、利用氢氧化钠能去除油污,原因是氢氧化钠具有乳化作用(2)、要配制200mL稀盐酸,用量筒量取浓盐酸时俯视读数(其他操作正确),则所配稀盐酸中溶质质量分数(填“偏大”“偏小”或“不变”)。(3)、某同学利用数字化传感设备,探究盐酸和NaOH溶液反应过程中温度和pH的变化,测定结果如图所示。通过图像可知:该实验是将(填“盐酸”或“NaOH溶液”)滴入另一溶液中;盐酸和NaOH溶液的反应属于反应(填“吸热”或“放热”);通过对温度和pH的图像判断,当滴加盐酸的体积为mL时,酸和碱恰好完全反应。
21. 化学与我们的生活、生产息息相关。(1)、小满时节,为促进农作物生长,可施用的化肥有:尿素[CO(NH2)2],硝酸钠(NaNO3),硫酸钾(K2SO4),其中属于钾肥的是。(2)、目前我国已掌握在-269℃下加压,将氦气转化为液氦的技术,该转化过程属于(填“物理变化”或“化学变化”)。22. 酸、碱、盐在生产、生活中有广泛的应用。(1)、下列关于酸、碱、盐的说法错误的是______。A、浓氨水具有挥发性 B、用食醋可除去水壶中的水垢 C、发明联合制碱法的科学家是侯德榜 D、利用氢氧化钠能去除油污,原因是氢氧化钠具有乳化作用(2)、要配制200mL稀盐酸,用量筒量取浓盐酸时俯视读数(其他操作正确),则所配稀盐酸中溶质质量分数(填“偏大”“偏小”或“不变”)。(3)、某同学利用数字化传感设备,探究盐酸和NaOH溶液反应过程中温度和pH的变化,测定结果如图所示。通过图像可知:该实验是将(填“盐酸”或“NaOH溶液”)滴入另一溶液中;盐酸和NaOH溶液的反应属于反应(填“吸热”或“放热”);通过对温度和pH的图像判断,当滴加盐酸的体积为mL时,酸和碱恰好完全反应。 (4)、NaOH是化学实验常用的试剂。
(4)、NaOH是化学实验常用的试剂。①向长期敞口放置在空气中的NaOH溶液中滴加稀盐酸,发现有气泡产生,请用化学方程式表示氢氧化钠变质的原因。
②请设计实验验证上述NaOH溶液已完全变质(写出操作方法、现象和结论)。
(5)、实验室常用石灰石与稀盐胶反应制取二氧化碳。若溶质质量分数为7.3%的稀盐酸100g与一定量的石灰石恰好完全反应,计算生成二氧化碳的质量。四、综合题
-
23. 如图为化合物与单质相互转化的关系(反应条件已略去)。请回答:
 (1)、若A为地壳中含量最多的金属,甲的相对分子质量为98且常用于金属除锈,反应①的化学方程式为。(2)、若甲、A均为黑色固体且物质X为单质,则B可能是 , A与足量X反应的化学方程式为。24. 下图是实验室中常见装置。回答下列问题。
(1)、若A为地壳中含量最多的金属,甲的相对分子质量为98且常用于金属除锈,反应①的化学方程式为。(2)、若甲、A均为黑色固体且物质X为单质,则B可能是 , A与足量X反应的化学方程式为。24. 下图是实验室中常见装置。回答下列问题。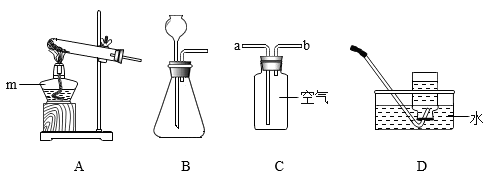 (1)、装置A中仪器m的名称是。(2)、用过氧化氢溶液制取氧气的化学方程式为 , 发生装置是(填字母序号)。(3)、用装置C收集CO2气体时,气体应从(填“a”或“b”)端通入。(4)、下列气体中,只能用装置D而不能用装置C收集的是(填数字序号)。
(1)、装置A中仪器m的名称是。(2)、用过氧化氢溶液制取氧气的化学方程式为 , 发生装置是(填字母序号)。(3)、用装置C收集CO2气体时,气体应从(填“a”或“b”)端通入。(4)、下列气体中,只能用装置D而不能用装置C收集的是(填数字序号)。①H2 ②N2 ③O2
25. 牙膏中常用碳酸钙粉末做摩擦剂。利用石灰石(杂质不溶于水和酸)制备纯净碳酸钙的一种方法如图。 (1)、反应①的化学方程式为;操作Ⅰ的名称是。(2)、反应②的化学方程式为 , 该反应属于反应(填基本反应类型)。(3)、该方法中,用稀硫酸代替稀盐酸对制备碳酸钙是否有影响?判断并简述理由。(4)、大气中CO2含量不断上升,会导致。我国在联合国大会上提出:努力争取2060年前实现“碳中和”,请提出一条实现“碳中和”的措施。
(1)、反应①的化学方程式为;操作Ⅰ的名称是。(2)、反应②的化学方程式为 , 该反应属于反应(填基本反应类型)。(3)、该方法中,用稀硫酸代替稀盐酸对制备碳酸钙是否有影响?判断并简述理由。(4)、大气中CO2含量不断上升,会导致。我国在联合国大会上提出:努力争取2060年前实现“碳中和”,请提出一条实现“碳中和”的措施。
-