河南省平顶山市2022年中考三模化学试题
试卷更新日期:2022-08-31 类型:中考模拟
一、单选题
-
1. 科学家利用元素周期表来寻找新元素及化合物。编制出元素周期表的科学家是( )A、侯德榜 B、门捷列夫 C、张青莲 D、拉瓦锡2. 下列变化能证明分子可以再分的是( )A、电解水 B、蜡熔化 C、盐结晶 D、碘升华3. 珍受生命,关注生活。以下做法错误的是( )A、油锅起火时用锅盖盖灭 B、冬季吃炭火锅时打开门窗 C、甲醛溶液浸泡海产品用来保鲜 D、适量补充维生素C能预防坏血病4. 鲁山县境内有丰富的温泉资源,下列对温泉水的说法错误的是( )A、清澈的温泉水属于溶液 B、过滤可以除去温泉水中可溶性杂质 C、活性炭可用于净化温泉水 D、检验温泉水是硬水还是软水可用肥皂水5. 分类是学习和研究化学常用的方法。下列物质分类正确的是( )A、微量元素:硒、碘、锌 B、氧化物:干冰、熟石灰、石灰石 C、合金:生铁、硬铝、黄金 D、合成材料:棉花、蚕丝、聚乙烯6. 合理的操作是实验成功的保证。下列实验操作无法达到目的的是( )A、
 检查装置气密性
B、
检查装置气密性
B、 比较合金和纯金属的硬度
C、
比较合金和纯金属的硬度
C、 证明CO2密度比空气的大
D、
证明CO2密度比空气的大
D、 探究燃烧的条件
7. Al与NaOH溶液反应会生成NaAlO2和一种气体,该气体可能是( )A、CO B、SO2 C、NH3 D、H28. 根据如图所示的溶解度曲线,下列说法中正确的是( )
探究燃烧的条件
7. Al与NaOH溶液反应会生成NaAlO2和一种气体,该气体可能是( )A、CO B、SO2 C、NH3 D、H28. 根据如图所示的溶解度曲线,下列说法中正确的是( ) A、甲物质的溶解度小于乙物质的溶解度 B、t2℃时,甲物质的溶液和乙物质的溶液中含有溶质的质量相等 C、当甲物质中混有少量乙物质时,可用冷却热饱和溶液的方法提纯甲 D、将t2℃时甲、乙两物质的饱和溶液升温至t3℃,所得甲、乙溶液中溶质的质量分数不相等9. 用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是( )
A、甲物质的溶解度小于乙物质的溶解度 B、t2℃时,甲物质的溶液和乙物质的溶液中含有溶质的质量相等 C、当甲物质中混有少量乙物质时,可用冷却热饱和溶液的方法提纯甲 D、将t2℃时甲、乙两物质的饱和溶液升温至t3℃,所得甲、乙溶液中溶质的质量分数不相等9. 用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是( ) A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处10. 配制130g溶质质量分数为6%的氯化钠溶液时,下列操作会导致溶质质量分数偏小的是( )
A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处10. 配制130g溶质质量分数为6%的氯化钠溶液时,下列操作会导致溶质质量分数偏小的是( )①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时俯视读数;③将氯化钠固体放在托盘天平的右盘称量;④往烧杯中加水时有水洒出;⑤转移配好的溶液时有少量溅出。
A、②③ B、①⑤ C、②④ D、①③11. 为除去下列物质中的杂质(括号内物质为杂质),所选试剂正确的是( )A、O2(H2O)—浓硫酸 B、铁粉(铜粉)—盐酸 C、CO2(HCl)—KOH溶液 D、FeSO4溶液(CuSO4)一锌粒12. 甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是( )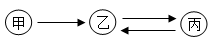 A、C、CO、CO2 B、H2O2、H2O、O2 C、KOH、K2CO3、KNO3 D、CuO、CuCl2、Cu(OH)213. 小山同学构建的“硫元素的化合价及其物质类别间的关系图”(见图),体现了“价类二维思想”。下列说法错误的是( )
A、C、CO、CO2 B、H2O2、H2O、O2 C、KOH、K2CO3、KNO3 D、CuO、CuCl2、Cu(OH)213. 小山同学构建的“硫元素的化合价及其物质类别间的关系图”(见图),体现了“价类二维思想”。下列说法错误的是( ) A、a为硫单质 B、b为SO2 C、c为H2SO4 D、d可能为Na2SO314. 实验室有一包含杂质的碳酸氢钠样品50g(杂质不含钠元素,受热不变化),其中钠元素的质量分数为23%,180℃时,将样品加热一段时间后称得固体质量为43.8g,则分解的碳酸氢钠占原碳酸氢钠的质量分数为(已知 )( )A、60% B、47.3% C、40% D、33.6%
A、a为硫单质 B、b为SO2 C、c为H2SO4 D、d可能为Na2SO314. 实验室有一包含杂质的碳酸氢钠样品50g(杂质不含钠元素,受热不变化),其中钠元素的质量分数为23%,180℃时,将样品加热一段时间后称得固体质量为43.8g,则分解的碳酸氢钠占原碳酸氢钠的质量分数为(已知 )( )A、60% B、47.3% C、40% D、33.6%二、填空题
-
15. 了解物质的用途,可以帮助我们更好的生活。请按要求选择合适的物质填空(填序号)。
①氢氧化钠 ②尿素 ③氯化钠 ④氢氧化钙 ⑤磷酸氢二铵
(1)、可以用来腌制食物的是。(2)、农业上用作复合肥的是。(3)、工业上用来制肥皂的是。16. 我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。(1)、现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、和天然气。(2)、乙醇属于可再生能源,则乙醇燃烧的化学反应方程式为。(3)、捕集、利用和封存CO2是实现碳中和的途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为。17. 将一定量的Zn加入含有Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中,充分反应后过滤,可以得到固体和溶液。其中会导致溶液质量减小的化学反应方程式为;若反应后溶液呈蓝色,此时溶液中一定含有的金属离子有 , 可能含有的金属离子有。18. 下图是去除粗盐中难溶性杂质实验的三步操作。 (1)、三步操作的正确顺序是(填序号)。(2)、B中,用璃棒不断搅拌的目的是。19. “笔、墨、纸、砚”是中国古代传统文化中的文书工具。狼毫笔的笔头是用黄鼠狼尾巴上的毛制成的,区分动物毛和腈纶线的方法是。端砚石的主要成分中有水白云母,其化学式为KAl2【(SiAl)4O10】·(OH)2﹒n H2O,水白云母中共含种非金属元素。20. 高纯CO可用于半导体领域某些芯片的刻蚀,利用甲酸(HCOOH)分解制取高纯CO,同时得到另一种氧化物。下图为甲酸分解的微观示意图,请补全方框中另一种产物的微粒图示 , 生成物的质量比为。
(1)、三步操作的正确顺序是(填序号)。(2)、B中,用璃棒不断搅拌的目的是。19. “笔、墨、纸、砚”是中国古代传统文化中的文书工具。狼毫笔的笔头是用黄鼠狼尾巴上的毛制成的,区分动物毛和腈纶线的方法是。端砚石的主要成分中有水白云母,其化学式为KAl2【(SiAl)4O10】·(OH)2﹒n H2O,水白云母中共含种非金属元素。20. 高纯CO可用于半导体领域某些芯片的刻蚀,利用甲酸(HCOOH)分解制取高纯CO,同时得到另一种氧化物。下图为甲酸分解的微观示意图,请补全方框中另一种产物的微粒图示 , 生成物的质量比为。 21. 已知A、B、C、D、E是五种不同类别的物质,它们有如图的转化关系(部分物质和反应条件略去)。A是年产量最高的金属,B中氧元素占30%,D的水溶液呈蓝色,常用于配制农药波尔多液。则B→A的化学方程式为;溶液中发生的一个置换反应的化学方程式为;E所属的物质类别是。
21. 已知A、B、C、D、E是五种不同类别的物质,它们有如图的转化关系(部分物质和反应条件略去)。A是年产量最高的金属,B中氧元素占30%,D的水溶液呈蓝色,常用于配制农药波尔多液。则B→A的化学方程式为;溶液中发生的一个置换反应的化学方程式为;E所属的物质类别是。
三、综合题
-
22. 回答下列问题(1)、室温下,分别向盐酸、NaOH溶液和NaCl溶液中加适量水稀释后,哪种溶液的pH变大?(2)、北京冬奥会利用液态二氧化碳蒸发吸热实现制冷,使水变成冰。请用分子的相关知识解释:将气态CO2压缩为液态的原理。23. 实验室有一瓶久置的氢氧化钠固体。为探究该固体的成分,小山同学取少量该固体样品进行以下实验:
 (1)、氢氧化钠变质的原因是什么?(用化学方程式表示)(2)、写出生成白色沉淀的化学反应方程式。(3)、根据溶液变红这一现象说明样品中含有的物质是什么?24. 如图所示为光亮铁钉的一系列变化。
(1)、氢氧化钠变质的原因是什么?(用化学方程式表示)(2)、写出生成白色沉淀的化学反应方程式。(3)、根据溶液变红这一现象说明样品中含有的物质是什么?24. 如图所示为光亮铁钉的一系列变化。 (1)、写出①中发生反应生成红色物质名称。(2)、写出③中除去铁锈的化学方程式。(3)、若光亮铁钉、锈蚀铁钉、无锈铁钉的质量分别为m1、m2、m3 , 写出它们质量由大到小的顺序(用字母表示)。25. 生活中常见物质的性质、制法等是化学研究的重要内容。(1)、下图是实验室制取气体的常用装置。
(1)、写出①中发生反应生成红色物质名称。(2)、写出③中除去铁锈的化学方程式。(3)、若光亮铁钉、锈蚀铁钉、无锈铁钉的质量分别为m1、m2、m3 , 写出它们质量由大到小的顺序(用字母表示)。25. 生活中常见物质的性质、制法等是化学研究的重要内容。(1)、下图是实验室制取气体的常用装置。
①仪器b的名称为。
②实验室用氯酸钾和二氧化锰制取O2应选用的一套实验装置为(填字母代号);该反应的化学方程式为。
③B和C装置均可制取CO2 , 与C相比较,B装置的主要优点是。
(2)、下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
①B装置玻璃管里可观察到的现象是。
②C装置中发生反应的化学方程式为。
③若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因。
(3)、实验室需制备22gCO2 , 用足量盐酸与含杂质20%(杂质不与盐酸反应)的石灰石反应,则需要这种石灰石的质量是多少?