广西河池市宜州区2022年中考二模化学试题
试卷更新日期:2022-08-31 类型:中考模拟
一、单选题
-
1. “三月三”是广西壮族传统节日,下列民俗活动主要体现化学变化的是( )A、抛绣球 B、打铜鼓 C、酿米酒 D、织布匹2. 空气中含量最多的气体是( )A、氮气 B、氧气 C、稀有气体 D、水蒸气3. 下列不属于空气污染指数(简称API)中监测的污染物是( )A、CO B、SO2 C、N2 D、PM2.54. 稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )A、
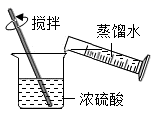 稀释浓硫酸
B、
稀释浓硫酸
B、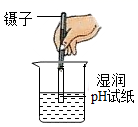 测稀硫酸的pH
C、
测稀硫酸的pH
C、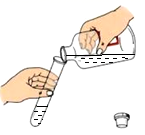 倾倒稀硫酸
D、
倾倒稀硫酸
D、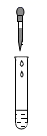 滴加稀硫酸
5. 下列做法与“碳达峰、碳中和”理念不相符的是( )A、限制燃放烟花 B、发展燃煤发电 C、分类处理垃圾 D、倡导公交出行6. 2022年3月22日是第30个“世界水日”,下列有关水的说法正确的是( )A、正常的雨水一般呈中性 B、蒸馏对天然水的净化程度最高 C、利用活性炭可软化硬水 D、煤炉边放一盆水可预防煤气中毒7. 下列有关实验现象的描述,正确的是( )A、打开浓盐酸的瓶盖,瓶口冒白烟 B、铁丝燃烧生成四氧化三铁 C、硫燃烧生成有刺激性气味的气体 D、点燃塑料产生烧焦羽毛气味8. 分类是一种重要的学习方法。下列物质属于碱的是( )A、NaHCO3 B、CH3COOH C、He D、Ca(OH)29. 下列对二氧化碳与一氧化碳的描述,正确的是( )A、都是氧化物 B、都能冶炼金属 C、都有可燃性 D、都可用于灭火10. 有关燃烧和灭火的说法中正确的是( )A、用嘴吹灭蜡烛—隔绝氧气 B、木柴架空—增大了氧气浓度 C、森林着火开辟隔离带—清除可燃物 D、煤炉火越扇越旺—增大与氧气的接触面积11. 下列关于氢氧化钠的描述中错误的是( )A、对皮肤有强烈的腐蚀作用 B、其水溶液能使石蕊溶液变红 C、固体氢氧化钠可做干燥剂 D、易溶于水,溶解时放出热量12. “宏观一微观一符号”是学习化学的重要内容和方法。如图表示镓在元素周期表中的部分信息和核外电子排布情况,据图所得信息描述正确的是( )
滴加稀硫酸
5. 下列做法与“碳达峰、碳中和”理念不相符的是( )A、限制燃放烟花 B、发展燃煤发电 C、分类处理垃圾 D、倡导公交出行6. 2022年3月22日是第30个“世界水日”,下列有关水的说法正确的是( )A、正常的雨水一般呈中性 B、蒸馏对天然水的净化程度最高 C、利用活性炭可软化硬水 D、煤炉边放一盆水可预防煤气中毒7. 下列有关实验现象的描述,正确的是( )A、打开浓盐酸的瓶盖,瓶口冒白烟 B、铁丝燃烧生成四氧化三铁 C、硫燃烧生成有刺激性气味的气体 D、点燃塑料产生烧焦羽毛气味8. 分类是一种重要的学习方法。下列物质属于碱的是( )A、NaHCO3 B、CH3COOH C、He D、Ca(OH)29. 下列对二氧化碳与一氧化碳的描述,正确的是( )A、都是氧化物 B、都能冶炼金属 C、都有可燃性 D、都可用于灭火10. 有关燃烧和灭火的说法中正确的是( )A、用嘴吹灭蜡烛—隔绝氧气 B、木柴架空—增大了氧气浓度 C、森林着火开辟隔离带—清除可燃物 D、煤炉火越扇越旺—增大与氧气的接触面积11. 下列关于氢氧化钠的描述中错误的是( )A、对皮肤有强烈的腐蚀作用 B、其水溶液能使石蕊溶液变红 C、固体氢氧化钠可做干燥剂 D、易溶于水,溶解时放出热量12. “宏观一微观一符号”是学习化学的重要内容和方法。如图表示镓在元素周期表中的部分信息和核外电子排布情况,据图所得信息描述正确的是( ) A、镓的相对原子质量为69.72g B、镓是一种非金属元素 C、镓原子核内有31个质子 D、氯化镓的化学式为GaCl213. 下列事实的微观解释不合理的是( )A、氮原子和磷原子属于不同元素——质子数不同 B、镁原子和镁离子化学性质不同——最外层电子数不同 C、干冰升华——二氧化碳分子变大 D、一氧化碳有毒,二氧化碳无毒——不同种分子化学性质不同14. 下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是( )A、浓盐酸 B、浓硫酸 C、石灰水 D、烧碱溶液15. 下列人体必需的元素中,青少年缺乏会引起食欲不振,生长迟缓的是( )A、锌 B、碘 C、钙 D、铁16. 下列物质间的转化关系,不能实现的是( )A、H2→H2O→O2 B、Mg→MgO→MgSO4 C、KCl→KNO3→K2SO4 D、NaOH→Na2CO3→NaCl17. 推理是学习化学的一种方法。以下推理正确的是( )A、离子是带电的粒子,则带电的粒子一定是离子 B、点燃可燃性气体前要验纯,所以点燃甲烷前一定要验纯 C、某物质在氧气中燃烧生成CO2和H2O,则该物质一定含有氧元素 D、有机物含有碳元素,因此含有碳元素的化合物一定是有机物18. 对某pH=1的无色溶液成分进行分析、检测,下列结果合理的是( )A、HCl MgCl2 Na2SO4 NaCl B、KNO3 K2CO3 NaNO3 CaCl2 C、NaCl ZnSO4 KNO3 KOH D、HNO3 KNO3 MgSO4 CuCl219. 下列实验设计能达到实验目的的是( )
A、镓的相对原子质量为69.72g B、镓是一种非金属元素 C、镓原子核内有31个质子 D、氯化镓的化学式为GaCl213. 下列事实的微观解释不合理的是( )A、氮原子和磷原子属于不同元素——质子数不同 B、镁原子和镁离子化学性质不同——最外层电子数不同 C、干冰升华——二氧化碳分子变大 D、一氧化碳有毒,二氧化碳无毒——不同种分子化学性质不同14. 下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是( )A、浓盐酸 B、浓硫酸 C、石灰水 D、烧碱溶液15. 下列人体必需的元素中,青少年缺乏会引起食欲不振,生长迟缓的是( )A、锌 B、碘 C、钙 D、铁16. 下列物质间的转化关系,不能实现的是( )A、H2→H2O→O2 B、Mg→MgO→MgSO4 C、KCl→KNO3→K2SO4 D、NaOH→Na2CO3→NaCl17. 推理是学习化学的一种方法。以下推理正确的是( )A、离子是带电的粒子,则带电的粒子一定是离子 B、点燃可燃性气体前要验纯,所以点燃甲烷前一定要验纯 C、某物质在氧气中燃烧生成CO2和H2O,则该物质一定含有氧元素 D、有机物含有碳元素,因此含有碳元素的化合物一定是有机物18. 对某pH=1的无色溶液成分进行分析、检测,下列结果合理的是( )A、HCl MgCl2 Na2SO4 NaCl B、KNO3 K2CO3 NaNO3 CaCl2 C、NaCl ZnSO4 KNO3 KOH D、HNO3 KNO3 MgSO4 CuCl219. 下列实验设计能达到实验目的的是( )选项
实验目的
实验设计
A
粗盐提纯
溶解、过滤、洗涤、干燥
B
检验CH4中是否混有H2
点燃,在火焰上方罩一干冷烧杯
C
鉴别MnO2粉末和木炭粉
取样,分别加水搅拌
D
除去N2中混有的少量O2
将气体缓缓通过足量的灼热铜网
A、A B、B C、C D、D20. 下列各图像中有关量的变化趋势与选项要求相符合的是( )A、 向等质量等浓度的稀硫酸中分别逐渐加入锌粉和铁粉至过量
B、
向等质量等浓度的稀硫酸中分别逐渐加入锌粉和铁粉至过量
B、 向一定质量MnO2固体中加入一定质量的H2O2溶液
C、
向一定质量MnO2固体中加入一定质量的H2O2溶液
C、 温度不变,向一定质量饱和Ca(OH)2溶液中加入CaO
D、
温度不变,向一定质量饱和Ca(OH)2溶液中加入CaO
D、 向一定质量H2SO4和CuSO4的混合溶液中加入NaOH溶液
向一定质量H2SO4和CuSO4的混合溶液中加入NaOH溶液
二、填空题
-
21. 请用数字和化学符号填空:(1)、铝元素。(2)、2个氢离子。(3)、+7价氯的氧化物。(4)、2个二氧化氮分子。(5)、氢氧化铁中氢氧根化合价为-1。22. 用序号填空:①发酵粉 ②活性炭 ③聚乙烯塑料 ④维生素A ⑤食盐(1)、可用于炒菜调味的是。(2)、属于合成材料的是。(3)、能预防夜盲症的是。(4)、可用作焙制糕点的是。(5)、可用于冰箱除异味的是。23. 化学与人类生产及生活紧密关联。回答下列问题:(1)、炊具上的油污可用洗洁精清洗,这是利用了洗洁精的作用。(2)、石墨烯是由碳原子构成的单层石墨片,可制成石墨烯电池。由此可推测石墨烯应具有的性质是。(3)、75%的酒精溶液和84消毒液均可用来消杀病毒。通常盛放84消毒液的容器是一种具有链状结构的塑料,这种塑料具有(填“热塑性”或“热固性”);酒精溶液中的溶剂是。(4)、以玉米、薯类等为原材料生产的可降解餐具,代替塑料制品为北京冬奥会提供了相关服务。玉米、薯类属于六大基本营养素中的;使用可降解餐具缓解的环境问题有(答一点即可)。24. 金属和金属材料在生产和生活中应用广泛。(1)、铜作导线,是利用铜的性;黄铜的熔点比铜的熔点。(2)、为防止家里面的铁锅生锈,你的做法是。(3)、将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是;若滤液显蓝色,则滤液中溶质一定有。25. 如图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,按要求填空。
 (1)、在℃时,甲和丙的溶解度相等。(2)、除去甲中含有的少量丙,可采用(填“降温结晶”或“蒸发结晶”)法。(3)、t1℃时,将乙溶液的状态由M点变为N点,方法是。(4)、t3℃时,将甲和乙饱和溶液分别降温到t1℃溶液,析出晶体的质量关系为____。A、甲>乙 B、甲<乙 C、甲=乙 D、无法确定(5)、t2℃时甲、乙、丙三种物质的饱和溶液,溶质的质量分数最大的是。
(1)、在℃时,甲和丙的溶解度相等。(2)、除去甲中含有的少量丙,可采用(填“降温结晶”或“蒸发结晶”)法。(3)、t1℃时,将乙溶液的状态由M点变为N点,方法是。(4)、t3℃时,将甲和乙饱和溶液分别降温到t1℃溶液,析出晶体的质量关系为____。A、甲>乙 B、甲<乙 C、甲=乙 D、无法确定(5)、t2℃时甲、乙、丙三种物质的饱和溶液,溶质的质量分数最大的是。三、综合题
-
26. 广西有丰富的钨(W)资源。如图是某工厂生产高纯度钨的工业流程。

已知:白钨矿的主要成分是钨酸钙(CaWO4),还含有CaO、SiO2 等;碳在高温条件下会与金属钨反应生成碳化钨。
(1)、操作1中粉碎白钨矿的目的是;操作3的名称为。(2)、操作2所得滤液中一定含有的阳离子是。(3)、氨水(NH3·H2O)和钨酸(H2WO4)反应生成(NH4)2WO4的化学方程式为。(4)、用H2还原WO3获得金属钨时,不宜用焦炭代替H2的原因是。27. A、B、C、D和E是初中化学常见的五种不同类别的物质。C和F的组成元素相同,A俗称纯碱,G可用于医疗急救。它们之间的反应关系如图所示:(“—”表示物质之间可以反应,“→”表示能生成;反应条件、部分反应物和生成物已省略)。 (1)、写出下列物质的化学式:A.;E.。(2)、D属于的物质类别为(选填“酸”“碱”“盐”或氧化物)。(3)、F→C的化学方程式为 , 图中没有涉及到的基本反应类型是。28. 下图是实验室制取气体的有关仪器和装置,据图回答下列问题。
(1)、写出下列物质的化学式:A.;E.。(2)、D属于的物质类别为(选填“酸”“碱”“盐”或氧化物)。(3)、F→C的化学方程式为 , 图中没有涉及到的基本反应类型是。28. 下图是实验室制取气体的有关仪器和装置,据图回答下列问题。 (1)、写出图中标有序号仪器名称:①;②。(2)、用加热高锰酸钾固体的方法制取氧气,应选择(从A~G中选择)组合装置,反应的化学方程式为。(3)、实验室制取CO2 , 为便于控制反应速率,应选择组合发生装置。将气体通入H装置(从a口进),还可以进行许多实验。下列实验不能达到预期目的的是(填序号,下同)。
(1)、写出图中标有序号仪器名称:①;②。(2)、用加热高锰酸钾固体的方法制取氧气,应选择(从A~G中选择)组合装置,反应的化学方程式为。(3)、实验室制取CO2 , 为便于控制反应速率,应选择组合发生装置。将气体通入H装置(从a口进),还可以进行许多实验。下列实验不能达到预期目的的是(填序号,下同)。① 收集CO2
② H中盛澄清石灰水,检验CO2
③ H中盛满水,b口连接量筒,测CO2的体积
④ H中盛NaOH溶液,除去CO2中的HCl气体
(4)、利用下图所示装置进行CO(CO中混有少量CO2)还原CuO实验,并验证反应后的气体产物。装置连接顺序正确的是____。 A、丙→甲→乙→丁 B、甲→丙→乙→丁 C、丙→乙→甲→乙→丁 D、乙→甲→丙→乙→丁29. 氢化钙(CaH2)是一种白色细颗粒状固体,能与水发生剧烈反应,反应的化学方程式为:CaH2+2H2O = Ca(OH)2+2H2↑。某实验小组的同学将一定量的CaH2加入碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。(1)、充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是(填写化学式)。(2)、【提出问题】滤液中溶质的成分是什么?
A、丙→甲→乙→丁 B、甲→丙→乙→丁 C、丙→乙→甲→乙→丁 D、乙→甲→丙→乙→丁29. 氢化钙(CaH2)是一种白色细颗粒状固体,能与水发生剧烈反应,反应的化学方程式为:CaH2+2H2O = Ca(OH)2+2H2↑。某实验小组的同学将一定量的CaH2加入碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。(1)、充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是(填写化学式)。(2)、【提出问题】滤液中溶质的成分是什么?【作出猜想】猜想一:NaOH;
猜想二:NaOH和Ca(OH)2;
猜想三:;
猜想四:NaOH、Na2CO3、Ca(OH)2。
经过分析,大家一致认为猜想四不合理,原因是(用化学方程式表示)。
(3)、【实验探究】实验方案
实验操作
现象
方案一
取一定量的滤液于试管中,往其中滴加少量稀盐酸
无明显实验现象
方案二
取一定量的滤液于另一试管中,往其中滴加
(4)、【讨论交流】根据实验现象,得出猜想三是正确的。请解释方案一中无明显现象的原因是。(5)、【反思拓展】若向NH4Cl的溶液中加一定量CaH2 , 充分反应,产生的气体有。四、计算题
-
30. 向100g溶质的质量分数为8%的氢氧化钠溶液中,加入一定质量的稀硫酸至恰好完全反应,反应后所得溶液质量为149g。(1)、硫酸(H2SO4)中H、S、O元素质量比是。(2)、用氢氧化钠固体配制100g溶质的质量分数为8%的氢氧化钠溶液,需要水的质量为。(3)、所加稀硫酸中溶质的质量分数(写出计算过程)。