广西百色市乐业县2022年中考二模化学试题
试卷更新日期:2022-08-31 类型:中考模拟
一、单选题
-
1. 下列日常生活中的现象,没有发生化学变化的是( )A、光合作用 B、滴水成冰 C、牛奶酸败 D、食醋酿造2. 牛肉、禽蛋里富含的营养素是( )A、油脂 B、蛋白质 C、无机盐 D、维生素3. 下列气体会造成酸雨的是( )A、一氧化碳、二氧化碳 B、氧气、氮气 C、氢气、水蒸气 D、二氧化硫、二氧化氮4. 硝酸铵是一种氮肥,易溶于水,受热易分解,遇碱时放出氨气,在高温或受猛烈撞击时易爆炸,下列使用硝酸铵的做法错误的是( )A、储存和运输时密封防潮 B、结块时用铁锤砸碎再用 C、施用时不宜与碱混和使用 D、给农作物施肥后及时盖土5. 学习化学应树立社会责任意识。下列有关环境保护措施和说法不合理的是( )A、火力发电厂需进行燃煤脱硫、控尘处理 B、为减少“白色污染”,可用布袋代替塑料袋 C、工业废水只要无色透明就可以随意排放 D、开发和利用清洁能源6. 有两种粒子,它们的核内质子数不相等,但是核外电子数相等。则这两种粒子不可能是( )A、同一种元素的原子和离子 B、两种不同的离子 C、两种电性不同的离子 D、两种不同元素的原子和离子7. 下列化学实验操作正确的是( )A、闻气味
 B、滴加蒸馏水
B、滴加蒸馏水  C、引燃酒精灯
C、引燃酒精灯 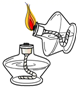 D、装入MnO2粉末
D、装入MnO2粉末 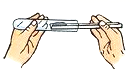 8. 下列说法错误的是( )A、密度最小的气体是氢气 B、地壳中含量最多的元素是氧元素 C、人体内含量最高的金属元素是铁元素 D、空气中含量最多的气体是氮气9. 下列有关溶液的说法错误的是( )A、溶液是均一、稳定的混合物 B、溶液中的溶质可以是固体、液体或气体 C、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 D、洗涤剂能洗去衣服上的油污,原因是洗涤剂具有乳化作用10. 下列物质的用途和性质对应关系错误的是( )A、钨——作灯丝——能导电、熔点高 B、一氧化碳——治金工业——可燃性 C、氖气——作霓虹灯——通电时能发出有色的光 D、生石灰——食品干燥剂——能与水发生反应11. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、电器在使用时着火,立即用水灭火 C、炒菜时油锅着火,立即盖上锅盖 D、高楼住宅发生火灾时,立即乘坐电梯逃生12. 如图是“尾气催化转换器”将汽车尾气中的有毒气体转变为无毒气体的微观示意图。下列说法错误的是( )
8. 下列说法错误的是( )A、密度最小的气体是氢气 B、地壳中含量最多的元素是氧元素 C、人体内含量最高的金属元素是铁元素 D、空气中含量最多的气体是氮气9. 下列有关溶液的说法错误的是( )A、溶液是均一、稳定的混合物 B、溶液中的溶质可以是固体、液体或气体 C、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 D、洗涤剂能洗去衣服上的油污,原因是洗涤剂具有乳化作用10. 下列物质的用途和性质对应关系错误的是( )A、钨——作灯丝——能导电、熔点高 B、一氧化碳——治金工业——可燃性 C、氖气——作霓虹灯——通电时能发出有色的光 D、生石灰——食品干燥剂——能与水发生反应11. 为强化安全意识,提升安全素养,某校举行了消防安全知识竞赛。下列做法正确的是( )A、室内起火,打开所有门窗通风 B、电器在使用时着火,立即用水灭火 C、炒菜时油锅着火,立即盖上锅盖 D、高楼住宅发生火灾时,立即乘坐电梯逃生12. 如图是“尾气催化转换器”将汽车尾气中的有毒气体转变为无毒气体的微观示意图。下列说法错误的是( )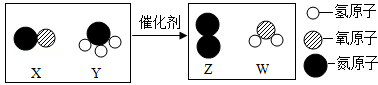 A、参加反应的x与y的分子个数比为1:1 B、该反应中NO发生了还原反应 C、反应前后催化剂的化学性质不变 D、反应物中只有一种物质是氧化物13. 经过实验探究,人们总结出了金属活动性顺序规律,下列有关说法正确的是( )A、金属铝比铁更耐腐蚀,是因为铁更活泼 B、工业上可以利用单质铁回收硫酸锌溶液中的金属锌 C、铜、银单质分别与稀盐酸混合,铜置换出氢气更快 D、金属活动性顺序可作为金属能否在溶液中发生置换反应的一种判断依据14. 不同元素在相互结合形成化合物时,呈现的化合价有所不同。在以下四个选项中,元素表现+3价的是( )A、SO2 B、Al2O3 C、NaCl D、NH315. 如图是初中化学中的一些常见实验,下列说法错误的是( )
A、参加反应的x与y的分子个数比为1:1 B、该反应中NO发生了还原反应 C、反应前后催化剂的化学性质不变 D、反应物中只有一种物质是氧化物13. 经过实验探究,人们总结出了金属活动性顺序规律,下列有关说法正确的是( )A、金属铝比铁更耐腐蚀,是因为铁更活泼 B、工业上可以利用单质铁回收硫酸锌溶液中的金属锌 C、铜、银单质分别与稀盐酸混合,铜置换出氢气更快 D、金属活动性顺序可作为金属能否在溶液中发生置换反应的一种判断依据14. 不同元素在相互结合形成化合物时,呈现的化合价有所不同。在以下四个选项中,元素表现+3价的是( )A、SO2 B、Al2O3 C、NaCl D、NH315. 如图是初中化学中的一些常见实验,下列说法错误的是( )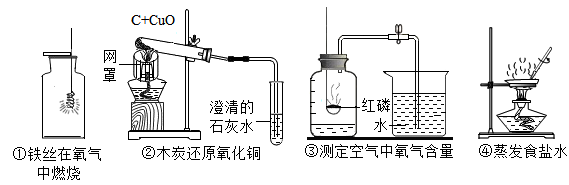 A、实验②能够证明C具有氧化性 B、实验①造成的后果是集气瓶炸裂 C、实验③红磷要足量的原因是将瓶内的氧气完全反应 D、实验④玻璃棒不断搅拌的目的是防止液滴飞溅16. 现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B的质量比是( )A、20:11 B、20:7 C、5:4 D、16:1117. 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( )
A、实验②能够证明C具有氧化性 B、实验①造成的后果是集气瓶炸裂 C、实验③红磷要足量的原因是将瓶内的氧气完全反应 D、实验④玻璃棒不断搅拌的目的是防止液滴飞溅16. 现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B的质量比是( )A、20:11 B、20:7 C、5:4 D、16:1117. 如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是( ) A、三种物质的溶解度大小关系为甲>乙>丙 B、t2℃时,将20g甲加入50g水中,得到70g溶液 C、t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙 D、将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲18. 下列各组离子在指定的溶液中,能大量共存的一组是( )A、无色溶液中:K+、Na+、、 B、酸性溶液中:Zn2+、Na+、、Cl- C、pH=11的溶液中:Mg2+、Ba2+、、Cl- D、含有大量Ba2+的溶液中:K+、、、19. 根据初中化学所学知识判断,下列物质间的转化不能通过一步反应实现的是( )A、H2SO4→HCl B、KNO3→NaNO3 C、Cu→Ag D、CO2→CO20. 下列实验方法能达到实验目的的是( )
A、三种物质的溶解度大小关系为甲>乙>丙 B、t2℃时,将20g甲加入50g水中,得到70g溶液 C、t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙 D、将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲18. 下列各组离子在指定的溶液中,能大量共存的一组是( )A、无色溶液中:K+、Na+、、 B、酸性溶液中:Zn2+、Na+、、Cl- C、pH=11的溶液中:Mg2+、Ba2+、、Cl- D、含有大量Ba2+的溶液中:K+、、、19. 根据初中化学所学知识判断,下列物质间的转化不能通过一步反应实现的是( )A、H2SO4→HCl B、KNO3→NaNO3 C、Cu→Ag D、CO2→CO20. 下列实验方法能达到实验目的的是( )选项
实验目的
实验方法
A
鉴别碳粉和四氧化三铁粉末
观察颜色
B
除去CO中的H2
通过灼热的CuO
C
分离NaCl和CuCl2混合溶液
加入适量的NaOH溶液,过滤
D
除去KNO3溶液中混有的KCl
加入适量的AgNO3溶液,过滤
A、A B、B C、C D、D二、填空题
-
21. 请从下列物质中选择合适的物质,用相应序号填空。
①氢气 ②肥皂水 ③熟石灰 ④氯化钠 ⑤甲醛
(1)、最清洁的燃料是。(2)、可改良酸性土壤的是。(3)、可用于制作动物标本的是。(4)、厨房里常用的调味品是。(5)、能区分硬水和软水的是。22. 化学用语是化学学科的精随。请完成下列填空:(1)、2个锰原子。(2)、醋酸。(3)、人体血液中含有亚铁离子的符号是。(4)、符号“ ”中“+5”表示。“2”表示。23. 水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。(1)、自来水生产过程中,常用明矾来净化水,明矾的作用是。(2)、在电解水的实验中,电源的正极与负极产生的气体的质量比为。(3)、凌芸同学配制50g溶液质量分数为10%的Na2CO3溶液,操作过程如图所示:
①配制溶液的正确操作顺序为(填字母序号):
②步骤D中玻璃棒的作用是。
③取1mL配制好的溶液于试管中,滴加紫色石蕊溶液,溶液变成色。
24. 元素周期表是学习和研究化学的重要工具,请根据下列信息回答有关问题。 (1)、上图中16号元素的原子在化学反应中,易(选填“得到”或“失去”)电子。(2)、发现的规律是:同一周期(横行)从左到右依次递增(写一点)。(3)、下图中,X=。氘、氚是核聚变的热核材料。氘和氚属于(选填“同种”或“不同种”)元素的原子。
(1)、上图中16号元素的原子在化学反应中,易(选填“得到”或“失去”)电子。(2)、发现的规律是:同一周期(横行)从左到右依次递增(写一点)。(3)、下图中,X=。氘、氚是核聚变的热核材料。氘和氚属于(选填“同种”或“不同种”)元素的原子。原子种类
质子数
中子数
核外电子数
氕
1
0
1
氘
1
1
1
氚
1
2
X
(4)、利用氘、氚热核聚变的“人造太阳将为人类提供永不枯竭的清洁能源。除核能外,清洁的新能源还有(填一种)。25. “新冠肺炎”疫情防控是一项长期的工作,不能松懈。(1)、一次性医用口罩阻隔病毒的关键材料熔喷布,是以聚丙烯为原料生产的。聚丙烯属于(选填“合成”或“复合”)材料。(2)、测量体温时,水银温度计的汞柱会升高。请从微观角度解释汞柱升高的原因:。(3)、84消毒液(含NaClO)常用于环境消毒。84消毒液(含NaClO)与洁厕灵(含盐酸)不能混用,否则会产生有毒的氯气和海水中含量最多的两种化合物,写出该反应的化学方程式。(4)、过氧乙酸是一种有效的新型消毒试剂,教室里喷洒后,同学们能够闻到特殊气味,说明分子具有的性质是。(5)、注意环境卫生,学会垃圾分类。果皮、烂菜叶属于下列图示中的____(填序号)。A、 B、
B、 C、
C、 D、
D、 26. 燃料和能源与社会发展息息相关。(1)、2021年中国科学院航天催化材料实验室将甲烷转化为甲醇(CH3OH),实现了天然气的高效利用。甲烷和甲醇均属于(选填“有机物”或“无机物”),甲烷在空气中完全燃烧的化学方程式为。(2)、运载火箭使用的燃料有液氢、煤油等。氢气目前还不能在生活和生产中大规模使用的原因之一是;为使煤油充分燃烧,一是要有足够的氧气,二是。(3)、铜镁合金是一种潜在的贮氢材料,可用一定质量比的铜、镁单质在氩气环境下高温熔炼获得。铜镁合金的熔点比镁或铜(选填“高”或“低”);熔炼制备该合金时,氩气的作用是。
26. 燃料和能源与社会发展息息相关。(1)、2021年中国科学院航天催化材料实验室将甲烷转化为甲醇(CH3OH),实现了天然气的高效利用。甲烷和甲醇均属于(选填“有机物”或“无机物”),甲烷在空气中完全燃烧的化学方程式为。(2)、运载火箭使用的燃料有液氢、煤油等。氢气目前还不能在生活和生产中大规模使用的原因之一是;为使煤油充分燃烧,一是要有足够的氧气,二是。(3)、铜镁合金是一种潜在的贮氢材料,可用一定质量比的铜、镁单质在氩气环境下高温熔炼获得。铜镁合金的熔点比镁或铜(选填“高”或“低”);熔炼制备该合金时,氩气的作用是。三、综合题
-
27. 红城百色蕴藏丰富的铝土资源,铝工业是百色传统优势产业、右江河谷某工厂用铝土矿(主要成分为Al2O3、Fe2O3、SiO2等)提取Al2O3 , 提取流程如图所示:
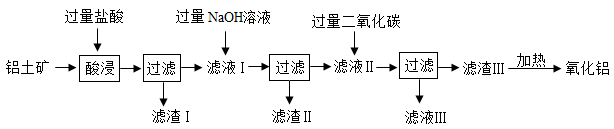
已知:I、 ;
II、
(1)、“酸浸”前,通常将铝土矿进行粉碎处理,“粉碎”的主要目的是。(2)、经检验,滤渣I的主要成分是SiO2。由此可推知SiO2的性质有(填序号)。①难溶于水 ②化学性质很活泼 ③不能与盐酸反应 ④不能与NaOH溶液反应
(3)、滤液Ⅱ中含有的溶质是(用化学式表示)。(4)、滤渣加热时,生成Al2O3和一种常见的氧化物,请写出反应的化学方程式。28. 根据下列装置回答问题: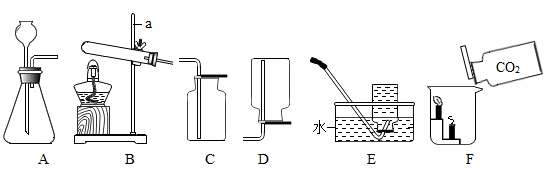
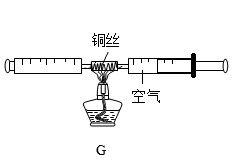 (1)、图B中仪器a的名称是。(2)、实验室制取二氧化碳气体,反应的化学方程式为;收集二氧化碳气体应选用的收集装置是(填序号)。(3)、如图F所示,将二氧化碳气体慢慢倒入烧杯中,观察到的现象是。(4)、图G所示装置可测定空气中氧气的含量。实验过程中需反复推拉铜丝两端注射器的活塞,目的是 , 铜丝表面变黑是生成了(填化学式)。29.(1)、碳酸钠在生活中具有广泛的用途,百色六中化学兴趣小组为探究碳酸钠的化学性质,进行了如下实验:向盛有适量碳酸钠溶液的四支试管中分别加入下列试剂,实验现象记录如下:
(1)、图B中仪器a的名称是。(2)、实验室制取二氧化碳气体,反应的化学方程式为;收集二氧化碳气体应选用的收集装置是(填序号)。(3)、如图F所示,将二氧化碳气体慢慢倒入烧杯中,观察到的现象是。(4)、图G所示装置可测定空气中氧气的含量。实验过程中需反复推拉铜丝两端注射器的活塞,目的是 , 铜丝表面变黑是生成了(填化学式)。29.(1)、碳酸钠在生活中具有广泛的用途,百色六中化学兴趣小组为探究碳酸钠的化学性质,进行了如下实验:向盛有适量碳酸钠溶液的四支试管中分别加入下列试剂,实验现象记录如下:试管编号
1
2
3
4
加入试剂
无色酚酞溶液
稀盐酸
澄清石灰水
氯化钡溶液
实验现象
有气泡产生
有白色沉淀产生
有白色沉淀产生
(2)、写出试管编号为“4”发生反应的化学方程式。(3)、化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,得到滤液A。【提出问题】滤液A中溶质的成分是什么?
【猜想假设】猜想一:NaOH:
猜想二:NaOH和Na2CO3:
猜想三:。
猜想四:NaOH、Na2CO3和Ca(OH)2。
(4)、【活动探究】小组讨论:有同学认为猜想四不成立,原因是。
(5)、进行实验:实验操作
实验现象
实验结论
方案甲:取少量滤液A于试管中,加入过量的稀盐酸
有气泡生成
猜想成立
方案乙:取少量滤液A于试管中,加入适量的Ba(NO3)2溶液
产生
(6)、【反思与评价】碳酸钠溶液呈性,可以和盐酸、氢氧化钙、氯化钡等物质发生反应。
(7)、要验证反应后物质的成分,既要考虑生成物,还应考虑。四、计算题