山东省枣庄市薛城区2021-2022学年高一上学期期中考试化学试题
试卷更新日期:2022-08-30 类型:期中考试
一、单选题
-
1. 下列行为中符合安全要求的是( )A、进入矿井时,用火把照明 B、实验时,将水倒入浓硫酸中配稀硫酸 C、节日期间,在开阔的广场燃放焰火 D、用点燃的火柴检验氢气钢瓶口是否漏气2. 下列实验操作与粒子大小无直接关系的是( )




A.过滤
B.渗析
C.萃取
D.丁达尔效应
A、A B、B C、C D、D3. 下列物质的转化中,不能够一步实现的是( )A、铁→氯化亚铁 B、氧化铁→氢氧化铁 C、氢氧化钙→氢氧化钠 D、次氯酸钙→次氯酸4. 用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作.下列图示对应的操作规范的是( )A、 称量
B、
称量
B、 溶解
C、
溶解
C、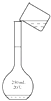 转移
D、
转移
D、 定容
5. 经检测,某工业废水显酸性,且废水中含有大量的Na+、Cu2+、Cl-、SO、NO。下列离子中,不可能大量存在于该废水中的是( )A、Ag+ B、K+ C、Fe3+ D、Mg2+6. 某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的①钠的密度比水的小②钠的熔点较低③钠与水反应时放出热量④钠与水反应后的溶液呈碱性( )A、①④ B、①②④ C、①③④ D、①②③④7. 下列关于氯气的叙述中,正确的是( )A、干燥的氯气是一种黄绿色、有毒的气体,可以贮存于钢瓶中 B、氯在自然界中既有化合态的,也有游离态的 C、氯气不能溶解于水,所以可用排水法收集氯气 D、氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物8. 下列关于钠的说法中,错误的是( )A、实验时用剩的钠块应该放回原试剂瓶 B、金属钠着火时,可用细沙灭火 C、工业上常将大量钠保存在四氯化碳中 D、实验室常将少量钠保存在煤油中9. 对某次酸雨成分的分析数据如下表,此次酸雨中c(H+)约为( )
定容
5. 经检测,某工业废水显酸性,且废水中含有大量的Na+、Cu2+、Cl-、SO、NO。下列离子中,不可能大量存在于该废水中的是( )A、Ag+ B、K+ C、Fe3+ D、Mg2+6. 某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的①钠的密度比水的小②钠的熔点较低③钠与水反应时放出热量④钠与水反应后的溶液呈碱性( )A、①④ B、①②④ C、①③④ D、①②③④7. 下列关于氯气的叙述中,正确的是( )A、干燥的氯气是一种黄绿色、有毒的气体,可以贮存于钢瓶中 B、氯在自然界中既有化合态的,也有游离态的 C、氯气不能溶解于水,所以可用排水法收集氯气 D、氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物8. 下列关于钠的说法中,错误的是( )A、实验时用剩的钠块应该放回原试剂瓶 B、金属钠着火时,可用细沙灭火 C、工业上常将大量钠保存在四氯化碳中 D、实验室常将少量钠保存在煤油中9. 对某次酸雨成分的分析数据如下表,此次酸雨中c(H+)约为( )离子
NH
Na+
Cl-
NO
SO
浓度/mol·L-1
2.0×10-5
1.9×10-5
6.0×10-5
2.3×10-5
2.8×10-5
A、1.5×10-4 B、1.0×10-4 C、6.2×10-5 D、1.0×10-510. 将4.6g金属钠与95.6g水中,得到的溶液中溶质的质量分数是( )A、稍小于4.6% B、4.6% C、8.0% D、稍小于8.0%11. 在蒸发皿中放一小块钠,加热熔化时,用玻璃棒蘸取少量无水硫酸铜与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成,据此判断下列说法中错误的是( ) A、上述反应发生了置换反应 B、上述反应说明钠比铜活泼 C、上述反应放出大量的热 D、上述反应证明钠可以从CuSO4溶液中置换出铜12. 归纳法是化学的重要方法之一、下表中正确的是( )
A、上述反应发生了置换反应 B、上述反应说明钠比铜活泼 C、上述反应放出大量的热 D、上述反应证明钠可以从CuSO4溶液中置换出铜12. 归纳法是化学的重要方法之一、下表中正确的是( )



A.地壳中元素含量顺序
B.物质的分类
C.金属的性质
D.氧的价一类二维图
A、A B、B C、C D、D13. 一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入9molN2 , 右边充入CO和CO2的混合气体共96g时,隔板处于如图位置(保持温度不变),下列说法正确的是( ) A、右边CO与CO2分子数之比为3∶1 B、右侧CO的质量为11g C、右侧气体密度是相同条件下氧气密度的2倍 D、若右边充入252gCO和CO2混合气体,改变混合气体CO和CO2的个数比能使隔板处于中间的处
A、右边CO与CO2分子数之比为3∶1 B、右侧CO的质量为11g C、右侧气体密度是相同条件下氧气密度的2倍 D、若右边充入252gCO和CO2混合气体,改变混合气体CO和CO2的个数比能使隔板处于中间的处二、多选题
-
14. 设NA表示阿伏加德罗常数值,下列说法中正确的是( )A、通常状况下,16g O2和O3混合气体所含的氧原子数为NA B、1mol/L的Na2SO4溶液中,含有的氧原子数为4NA C、标准状况下,22.4L H2O中含有的分子个数为NA D、标准状况下,22.4L空气所含气体的分子总数为NA15. 下列离子方程式的书写正确的是( )A、铜片投入稀硫酸中:Cu+2H+=Cu2++H2↑ B、过量的CO2与澄清石灰水反应:OH-+CO2=HCO C、食醋与大理石反应:CaCO3+2H+=Ca2++CO2↑+H2O D、金属钠与氯化镁溶液反应:2Na+Mg2++2H2O=2Na++H2↑+Mg(OH)2
三、综合题
-
16. “84”消毒液是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、医院、食品加工行业、家庭等的卫生消毒。某“84”消毒液瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
 (1)、此“84消毒液”的物质的量浓度约为mol/L。(计算结果保留一位小数)(2)、某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)mol/L。(3)、该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制所需的480mL含NaClO质量分数为24%的消毒液。
(1)、此“84消毒液”的物质的量浓度约为mol/L。(计算结果保留一位小数)(2)、某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)mol/L。(3)、该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制所需的480mL含NaClO质量分数为24%的消毒液。①配制溶液需要使用图2中所示的仪器有(填仪器序号),还缺少的玻璃仪器是。
②下列操作中,容量瓶不具备的功能是(填仪器序号)。
a.配制一定体积准确浓度的标准溶液b.贮存溶液
c.用来加热溶解固体溶质d.准确稀释某一浓度的溶液
③配制此溶液该同学需称取称量NaClO固体的质量为g。
(4)、若实验遇下列情况,导致所配溶液的物质的量浓度偏高是____(填序号)。A、定容时俯视刻度线 B、转移前,容量瓶内有蒸馏水 C、称量所用砝码生锈 D、定容时加多水,用胶头滴管吸出17. 按如图所示装置连接,然后向滴有几滴酚酞的200.00mL 0.01mol/L Ba(OH)2溶液中逐滴滴入0.20mol/L H2SO4溶液,直至过量。请回答下列问题: (1)、滴加酚酞的Ba(OH)2溶液呈红色,原因是。(2)、开始滴加时,反应的离子方程式为: , 当所滴0.20mol/L硫酸溶液的体积为mL时,电导率的值最小。(3)、若实验改为:用0.5mol/L醋酸溶液滴入到滴有酚酞的0.4mol/L氨水时,电导率传感器绘制的图像可能为(填:“甲”、“乙”或“丙”)。若实验改为:向氢氧化钡溶液中通入二氧化碳气体,电导率传感器绘制的图像可能为(填:“甲”、“乙”或“丙”)。
(1)、滴加酚酞的Ba(OH)2溶液呈红色,原因是。(2)、开始滴加时,反应的离子方程式为: , 当所滴0.20mol/L硫酸溶液的体积为mL时,电导率的值最小。(3)、若实验改为:用0.5mol/L醋酸溶液滴入到滴有酚酞的0.4mol/L氨水时,电导率传感器绘制的图像可能为(填:“甲”、“乙”或“丙”)。若实验改为:向氢氧化钡溶液中通入二氧化碳气体,电导率传感器绘制的图像可能为(填:“甲”、“乙”或“丙”)。 18. 现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样纯度(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
18. 现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样纯度(可供选用的反应物只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
回答下列问题:
(1)、装置A中盛装液体仪器的名称是。(2)、装置A中液体试剂选用 , 理由是。(3)、装置B的作用是除去挥发的HCl,反应的离子方程式为;装置C的作用是;装置E中碱石灰的作用是。(4)、装置D中发生主要反应的化学方程式。(5)、若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为。19. 现有失去标签的四瓶无色溶液:Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。实验顺序
实验内容
实验现象
实验顺序
实验内容
实验现象
①
A+B
生成白色沉淀
④
B+C
无明显变化
②
A+C
放出无色气体
⑤
B+D
生成白色沉淀
③
A+D
放出无色气体
⑥
C+D
无明显变化
已知:NaHSO4在水溶液中的电离方程式为:NaHSO4=Na++H++SO。回答下列问题:
(1)、A为。(2)、依据电解质的电离分类,NaHSO4属于____ (填标号)。A、酸 B、正盐 C、酸式盐(3)、写出A与B反应的离子方程式。(4)、等物质的量浓度、等体积的B、D混合反应的离子方程式为。反应后得到的溶液中含有的阴离子有。(5)、上述没有明显变化的实验④、⑥,其中发生了离子反应,离子方程式为。20. 游泳池水中的氯气含量应该控制在0.5~1.0 mg·L-1之间。(1)、写出氯气溶于水的化学方程式:。溶于水后的哪种物质可杀菌消毒:(写化学式)。(2)、如图显示一星期中每天19时游泳池水中的氯气含量,哪几天19时使用游泳池不安全?。 (3)、你认为哪几天的天气炎热、阳光强烈? , 说出一种理由。(4)、若把一片紫色的花瓣放入氯水中,可观察到的现象是 (花瓣所含色素性质与石蕊相似)。(5)、小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:。
(3)、你认为哪几天的天气炎热、阳光强烈? , 说出一种理由。(4)、若把一片紫色的花瓣放入氯水中,可观察到的现象是 (花瓣所含色素性质与石蕊相似)。(5)、小型游泳池通常使用次氯酸钠溶液而非氯气给池水消毒,用化学方程式说明工业上如何生产次氯酸钠:。