山东省潍坊市市区2022年中考三模化学试题
试卷更新日期:2022-08-17 类型:中考模拟
一、单选题
-
1. 2021 年 10 月,神舟十三号载人飞船成功升空,下列有关变化属于化学变化的是( )A、氢气液化填充 B、火箭点火上升 C、隔热材料脱落 D、导流槽内的水受热汽化2. 下列物质的用途中,利用其物理性质的是( )A、生石灰做干燥剂 B、小苏打治疗胃酸过多 C、75%的酒精溶液对皮肤消毒 D、活性炭除去自来水中的异味和色素3. 材料科学是国民经济发展的支撑。下列属于有机合成材料的是( )A、用作人造关节的钛合金材料 B、用作体育器材的玻璃钢 C、制作奥运吉祥物“冰墩墩”的外材料纯羊毛 D、速滑竞赛服使用的高性能合成纤维和聚酯材料4. 2022 年 5 月 12 日是我国第 14 个防灾减灾日,今年的主题是“减轻灾害风险,守护美 好家园”。下列做法不符合安全要求的是( )A、发生震灾不能乘坐电梯逃生 B、水基型灭火器用于扑救带电设备的火灾 C、加油站、面粉加工厂等场所必须严禁烟火 D、在有明火的区域内禁止喷洒含酒精的消毒剂5. 实验室中的药品常按物质的性质、类别等不同而有规律地放置.在做“酸的性质”实验时,实验桌上部分药品的摆放如图.某同学取用Na2CO3溶液后把它放回位置最好在()A、
 B、
B、 C、
C、 D、
D、 6. 下列关于宏观事实的微观解释中,正确的是()A、将二氧化碳气体制成干冰体积变小 分子体积变小 B、氢气在氧气中燃烧生成水 化学反应中分子和原子都可以再分 C、自然界中水的天然循环 水分子不断运动且分子间的间隔发生改变 D、食物变质 食物中的分子种类不变,但分子的性质发生了变化7. 多巴胺(化学式为 C8H11NO2)是大脑中含量最丰富的儿茶酚胺类神经递质。多巴胺作为神经递质调控中枢神经系统的多种生理功能。多巴胺系统调节障碍涉及帕金森病,精神分裂症,Tourette 综合症,注意力缺陷多动综合症和垂体肿瘤的发生等。下列有关多巴胺的说法错误的是( )A、多巴胺属于有机物 B、多巴胺分子中含有氧分子 C、多巴胺的相对分子质量为 153 D、每个多巴胺分子是由 8 个碳原子,11 个氢原子,1 个氮原子和 2 个氧原子构成8. 如图表示元素化合价与物质类别的关系,“→”表示物质类别之间可以转化。A、B、C、D 是初中所学物质, 分别由H、C、O中的一种、两种或三种元素组成。下列说法正确的是( )
6. 下列关于宏观事实的微观解释中,正确的是()A、将二氧化碳气体制成干冰体积变小 分子体积变小 B、氢气在氧气中燃烧生成水 化学反应中分子和原子都可以再分 C、自然界中水的天然循环 水分子不断运动且分子间的间隔发生改变 D、食物变质 食物中的分子种类不变,但分子的性质发生了变化7. 多巴胺(化学式为 C8H11NO2)是大脑中含量最丰富的儿茶酚胺类神经递质。多巴胺作为神经递质调控中枢神经系统的多种生理功能。多巴胺系统调节障碍涉及帕金森病,精神分裂症,Tourette 综合症,注意力缺陷多动综合症和垂体肿瘤的发生等。下列有关多巴胺的说法错误的是( )A、多巴胺属于有机物 B、多巴胺分子中含有氧分子 C、多巴胺的相对分子质量为 153 D、每个多巴胺分子是由 8 个碳原子,11 个氢原子,1 个氮原子和 2 个氧原子构成8. 如图表示元素化合价与物质类别的关系,“→”表示物质类别之间可以转化。A、B、C、D 是初中所学物质, 分别由H、C、O中的一种、两种或三种元素组成。下列说法正确的是( ) A、B和C可以互相转化 B、A→C 的反应一定是化合反应 C、B→C 的反应条件一定是点燃 D、A 的化学式一定是O29. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是( )A、阴离子带负电,所以带负电的粒子都是阴离子 B、碱溶液一定显碱性,显碱性的溶液一定是碱溶液 C、同种元素的原子质子数相同,则质子数相同的原子一定是同种元素 D、铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀10. 近日中国科学技术大学曾杰教授研究团队通过构筑原子级分散的钌催化剂实现高效 氮气电还原合成氨,反应前后分子变化的微观示意图如图,下列说法正确的是( )
A、B和C可以互相转化 B、A→C 的反应一定是化合反应 C、B→C 的反应条件一定是点燃 D、A 的化学式一定是O29. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是( )A、阴离子带负电,所以带负电的粒子都是阴离子 B、碱溶液一定显碱性,显碱性的溶液一定是碱溶液 C、同种元素的原子质子数相同,则质子数相同的原子一定是同种元素 D、铝比铁更易与氧气发生化学反应,则在空气中铝制品比铁制品更易被腐蚀10. 近日中国科学技术大学曾杰教授研究团队通过构筑原子级分散的钌催化剂实现高效 氮气电还原合成氨,反应前后分子变化的微观示意图如图,下列说法正确的是( ) A、反应前后分子数目不变 B、生成物的质量之比为 4:3 C、催化剂的化学性质发生了变化 D、反应前后氮元素的化合价降低11. 下列各组离子在指定的溶液中,能大量共存的是( )A、无色溶液中:K+、Na+、、Cu2+ B、能使紫色石蕊溶液变红的溶液中:Mg2+、Na+、、OH- C、pH=10 的溶液中:Ba2+、Ca2+、、Cl- D、pH=0 的溶液中:Na+、K+、、Cl-12. 为了探究“烧不坏的手帕”原理,将滤纸(着火点 130℃)浸在不同浓度的酒精溶液中,进行如图 1 所示实验,并收集实验过程滤纸中心温度,绘制曲线如图 2所示,下列说法错误的是( )
A、反应前后分子数目不变 B、生成物的质量之比为 4:3 C、催化剂的化学性质发生了变化 D、反应前后氮元素的化合价降低11. 下列各组离子在指定的溶液中,能大量共存的是( )A、无色溶液中:K+、Na+、、Cu2+ B、能使紫色石蕊溶液变红的溶液中:Mg2+、Na+、、OH- C、pH=10 的溶液中:Ba2+、Ca2+、、Cl- D、pH=0 的溶液中:Na+、K+、、Cl-12. 为了探究“烧不坏的手帕”原理,将滤纸(着火点 130℃)浸在不同浓度的酒精溶液中,进行如图 1 所示实验,并收集实验过程滤纸中心温度,绘制曲线如图 2所示,下列说法错误的是( )
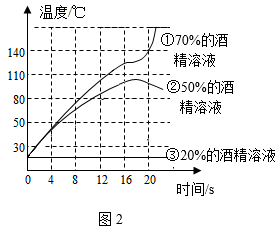 A、曲线 1 在 20 s 时温度突然升高的原因是滤纸燃烧 B、曲线 2 的温度始终没有达到滤纸的着火点,滤纸不燃烧 C、曲线 3 所示的温度没有明显变化,是酒精没有与氧气接触 D、“烧不坏的手帕”原理是液体汽化吸热使其温度达不到着火点
A、曲线 1 在 20 s 时温度突然升高的原因是滤纸燃烧 B、曲线 2 的温度始终没有达到滤纸的着火点,滤纸不燃烧 C、曲线 3 所示的温度没有明显变化,是酒精没有与氧气接触 D、“烧不坏的手帕”原理是液体汽化吸热使其温度达不到着火点二、多选题
-
13. 下列图像与对应的叙述相符合的是( )A、
 图 A 是一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体
B、
图 A 是一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体
B、 图 B 是分别向足量相同的硫酸铜溶液中加入质量相等的锌粉和铁粉
C、
图 B 是分别向足量相同的硫酸铜溶液中加入质量相等的锌粉和铁粉
C、 图 C 是高温灼烧一定质量的大理石
D、
图 C 是高温灼烧一定质量的大理石
D、 图 D 是向一定质量的 HCl 和 MgCl2的混合溶液中,逐滴加入 NaOH 溶液
14. 下列实验方案能达到目的的是( )
图 D 是向一定质量的 HCl 和 MgCl2的混合溶液中,逐滴加入 NaOH 溶液
14. 下列实验方案能达到目的的是( )选项
实验目的
实验方案
A
除去生石灰中少量的碳酸钙
高温煅烧
B
检验久置的NaOH是否变质
取样,滴加酚酞溶液
C
鉴别氯化钠和碳酸钠
加水溶解,滴加稀盐酸
D
分离Cu粉和Fe粉的混合物
加入足量的稀硫酸,过滤、洗涤、干燥
A、A B、B C、C D、D15. 某化学小组的同学将单质锌和单质银的混合物ag加入到一定量的Cu(NO3)2溶液中,充分反应后过滤,得到一定温度下的滤液(不饱和)和滤渣,在滤渣中加入稀盐酸,有气泡冒出。下列有关说法中,不合理的是( )A、滤液一定是无色溶液 B、滤液中一定含有Ag+、Zn2+ C、滤渣的质量一定大于ag D、滤渣中一定含有单质银、单质铜和单质锌16. 20℃时KCl的溶解度是34g。取65gKCl溶液放入甲烧杯中,按如图所示进行操作(整个过程中无溶剂损失)。以下说法正确的是( ) A、甲烧杯中是KCl的饱和溶液 B、乙和丙烧杯中KCl的质量分数相等 C、丁烧杯中KCl和H2O的质量之比为17:50 D、若乙烧杯中溶液恰好饱和,则40℃时KCl的溶解度为40g17. 向盛有硫酸和硫酸铜混合溶液的烧杯中滴入 Ba(OH)2溶液,烧杯中溶质的质量与加入 的 Ba(OH)2溶液的质量关系如图所示。下列有关说法错误的是( )
A、甲烧杯中是KCl的饱和溶液 B、乙和丙烧杯中KCl的质量分数相等 C、丁烧杯中KCl和H2O的质量之比为17:50 D、若乙烧杯中溶液恰好饱和,则40℃时KCl的溶解度为40g17. 向盛有硫酸和硫酸铜混合溶液的烧杯中滴入 Ba(OH)2溶液,烧杯中溶质的质量与加入 的 Ba(OH)2溶液的质量关系如图所示。下列有关说法错误的是( ) A、a→b 段溶液的质量一定减小 B、b→c 段有水生成 C、b 点溶液溶质为硫酸铜 D、d 点沉淀质量与 b 点沉淀质量不相等
A、a→b 段溶液的质量一定减小 B、b→c 段有水生成 C、b 点溶液溶质为硫酸铜 D、d 点沉淀质量与 b 点沉淀质量不相等三、填空题
-
18. 2022 年北京冬奥会体现了“健康饮食”“绿色冬奥”“科技冬奥”的理念。(1)、运动员的健康饮食受到关注。北京烤鸭是很多运动员喜欢的一道美食,为运动员提 供的主要营养素有油脂和 , 运动员需要多食用蔬菜水果补充各种维生素,缺乏维生素 C 引起的疾病是 , 东北大米入住奥运村,水稻种植过程中使用 的硝酸钾属于肥。(2)、“绿色”是北京冬奥会的主要理念,冬奥会首次采用了氢气作为火炬燃料,氢气可由电解水的(填“正极”或“负极”)产生。关闭火炬燃料开关可使火炬熄灭, 依据的灭火原理是。冬奥会部分交通工具以氢氧燃料电池为动力来源,氢氧燃料电池工作时的能量转化方式为。(3)、颁奖礼服为增强保温效果添加了石墨烯发热材料。石墨烯属于(填“单质” 或“化合物”)。(4)、国家速滑馆又称“冰丝带”,是 2022 年北京冬奥会最具科技含量的场馆。它采用了当前最环保的制冰技术——二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳 汽化实现制冷。下列说法中正确的是____(填字母序号)。A、制冰过程中二氧化碳分子的构成没有发生变化 B、液态二氧化碳汽化放热,使水凝结成冰 C、二氧化碳分子的质量和体积发生了变化 D、二氧化碳跨临界直接制冰技术利用了其化学性质19. 我国承诺 2030 年前,二氧化碳排放量不再增长,实现“碳达峰”,到 2060 年要采取各种方式抵消自身产生的二氧化碳排放量,实现“碳中和”。(1)、捕集、利用和封存 CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与 CO2反应生成碳酸镁,该反应的化学方程式为。(2)、在高温高压下,CO2和 NH3可以合成尿素[CO(NH2)2],同时生成水,该反应中参加反 应的 CO2与 NH3的分子个数比是。(3)、低碳冶金:氢基熔融冶金技术是利用氢作为还原剂代替碳还原剂,从而实现减少 CO2排放的目的,实现低碳冶金。氢基熔融还原生产高纯铸造生铁的主要流程如下图。

①燃烧区的作用是 , 燃烧区发生的燃烧反应还有(用化学方程式表示)。
②还原区的反应除 , 另一主要反应的化学方程式是。
③与高炉炼铁技术相比,从环境保护角度看氢基熔融冶金技术的优点是。
20. 钠是一种性质活泼的金属,常温下能与水、氧气、盐溶液等多种物质发生反 应。如图为金属钠与硫酸铜溶液反应的微观过程示意图,请据图回答。 (1)、金属钠在化学反应中容易(填“得”或“失”)电子,反应Ⅰ的化学方程式 , 该反应的基本反应类型是。(2)、反应Ⅱ的化学方程式为 , 从微观角度分析该反应的实质是。(3)、由反应Ⅰ和反应Ⅱ可以推测金属钠投入硫酸铜溶液中发生的实验现象为。21. 化学是一门以实验为基础的科学。根据下列装置回答问题。
(1)、金属钠在化学反应中容易(填“得”或“失”)电子,反应Ⅰ的化学方程式 , 该反应的基本反应类型是。(2)、反应Ⅱ的化学方程式为 , 从微观角度分析该反应的实质是。(3)、由反应Ⅰ和反应Ⅱ可以推测金属钠投入硫酸铜溶液中发生的实验现象为。21. 化学是一门以实验为基础的科学。根据下列装置回答问题。 (1)、写出字母 a 的仪器名称。(2)、写出用装置 B 制取氧气的化学方程式 , 装置 B 相比于装置 A 的优点是。用 F 装置收集氧气, 请写出检验该气体集满的方法。(3)、从 C 装置制取氧气的剩余产物中提取二氧化锰,需要的操作是溶解、(填上述装置序号)、、干燥,其中溶解时玻璃棒的作用是。22. 火法炼铜,是我国古代的一种炼铜技术,部分流程如图所示。
(1)、写出字母 a 的仪器名称。(2)、写出用装置 B 制取氧气的化学方程式 , 装置 B 相比于装置 A 的优点是。用 F 装置收集氧气, 请写出检验该气体集满的方法。(3)、从 C 装置制取氧气的剩余产物中提取二氧化锰,需要的操作是溶解、(填上述装置序号)、、干燥,其中溶解时玻璃棒的作用是。22. 火法炼铜,是我国古代的一种炼铜技术,部分流程如图所示。 (1)、步骤Ⅰ中发生的反应有 , X 的化学式是 , 上述反应中生成的 Cu2S 中铜元素的化合价为。(2)、如图是步骤Ⅱ中用到竖炉的内部部分构造。
(1)、步骤Ⅰ中发生的反应有 , X 的化学式是 , 上述反应中生成的 Cu2S 中铜元素的化合价为。(2)、如图是步骤Ⅱ中用到竖炉的内部部分构造。
①吹炼过程中,冰铜中的 FeS 在高温下被氧化成氧化亚铁和二氧化硫,请写出该反应的化学方程式。
②竖炉内部“进气环管”环形设计的优点是(写出一点即可)。
(3)、铜中加入铅、锡制得的铜合金具有很多优良性能,如(填一种即可)。(4)、我国古代还出现浸铁为铜的“湿法炼铜”工艺,反应的化学方程式为 , 与“火法炼铜”相比,该工艺的优点是。23. 化学社团的同学在探究金属化学性质时,进行了如图 1 所示的实验。 (1)、图 1 实验中观察到的现象是:锌片表面产生气泡,铜片表面锌 和稀硫酸反应的化学方程式为。
(1)、图 1 实验中观察到的现象是:锌片表面产生气泡,铜片表面锌 和稀硫酸反应的化学方程式为。实验过程中小辰意外发现:当两种金属发生触碰时(如图 2),铜片表面产生了气泡。
(2)、【提出问题】图 2 中铜是否发生了化学反应?产生的气体是什么?【作出猜想】同学们对产生的气体进行了以下猜想:
小知猜想是二氧化硫;小辰猜想是氧气;小彬猜想是氢气。
【查阅资料】
①将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面产生气体。该反应过程中 金属失去的电子通过导线发生了转移。
②二氧化硫能使品红溶液褪色。
【设计并进行实验】他们设计了图 3 装置进行实验,将产生的气体分别通过导管与图 4 中的装置连接,验证自己的猜想。
实验操作
实验现象
实验结论
小知
连接导管a与导管d,向品红溶液中通入气体一段时间
小彬的猜想正确
小辰
选用正确方法收集气体一段时间后,向试管内伸入带火星的木条
小彬
连接导管a与导管(填序号),收集气体后拇指堵住试管口,靠近酒精灯火焰,移开拇指点火
气体燃烧,听到轻微的“噗”声
(3)、【教师释疑】图 1 实验中,锌与稀硫酸反应,锌原子失去电子,酸溶液中氢离子在锌片 表面获得电子生成氢气。【学生感悟】图 3 实验中,酸溶液中的氢离子从铜片表面获得(填“锌”或“铜”) 失去的电子生成了氢气。
(4)、【得出结论】图 2 中两种金属触碰后铜(填“有”或“没有”)发生化学反应。(5)、【延伸应用】制造钢制船闸门时,为防止铁被腐蚀,常在钢闸门表面安装比铁更活泼的金属。这种金属可以是____(填字母序号)。A、锌 B、铜 C、银四、计算题
-
24. 国家标准规定工业纯碱中碳酸钠的质量分数≥98.0%为合格。为测定某工业纯碱是否为合格品,某兴趣小组进行实验:取 22g 样品加水溶解,慢慢加入溶质质量分 数 10%的 BaCl2溶液,反应过程中产生沉淀的质量与所加入 BaCl2溶液的质量关系如图所示。请完成下列问题。
 (1)、当加入 BaCl2溶液 200g 时(即图中 A 点),溶液里存在的酸根离子是(用符号表示)。(2)、当加入 BaCl2溶液的质量为 416g 时,恰好完全反应, 求纵坐标 M 的值。(计算结果精确至 0.1)(3)、通过计算判断该纯碱样品是否合格。
(1)、当加入 BaCl2溶液 200g 时(即图中 A 点),溶液里存在的酸根离子是(用符号表示)。(2)、当加入 BaCl2溶液的质量为 416g 时,恰好完全反应, 求纵坐标 M 的值。(计算结果精确至 0.1)(3)、通过计算判断该纯碱样品是否合格。