上海市浦东新区2022年6月线下中考二模化学试题
试卷更新日期:2022-08-10 类型:月考试卷
一、单选题
-
1. 计算机硬件材料中大量使用硅,硅的元素符号是( )A、S B、P C、Si D、Hg2. 属于化学性质的是( )A、酸碱性 B、挥发性 C、熔沸点 D、导电性3. 放入水中能形成溶液的是( )A、麻油 B、蔗糖 C、淀粉 D、牛奶4. 氮化锶(Sr3N2)是生产高端荧光粉的主要原料。已知Sr3N2中N的化合价为﹣3,则Sr的化合价为( )A、﹣3 B、﹣2 C、+2 D、+35. 属于有机物的是( )A、石墨 B、酒精 C、碳酸 D、氮气6. 净水过程中加入的吸附剂是( )A、氯气 B、明矾 C、生石灰 D、活性炭7. 互为同素异形体的是( )A、铁丝和铁片 B、氧气和臭氧 C、纯碱和烧碱 D、水银和银粉8. 高铁快速发展方便了出行。工业上可利用如下反应焊接钢轨:2Al+Fe2O32Fe+Al2O3.则该反应属于( )A、化合反应 B、分解反应 C、复分解反应 D、置换反应9. 化学用语与含义相符的是( )A、NO3-:硝酸根 B、2Zn:2 个锌元素 C、H2:2 个氢原子 D、 :+2 价的铜10. 物质用途描述错误的是( )A、氦气:制作霓虹灯 B、熟石灰:改良酸性土壤 C、氧气:可用做燃料 D、氯化钠:作厨房调味品11. O4是一种新型的分子,下列叙述正确的是( )A、O4是一种化合物 B、O4中氧元素以游离态存在 C、O4与 O2性质一定相同 D、一个 O4分子中有二个氧分子12. 化学方程式书写正确的是( )A、 B、 C、 D、13. 能达到实验目的是( )
选项
实验目的
实验操作
A
鉴别 O2和 N2
燃着的木条伸入
B
鉴别食盐水和稀盐酸
加入酚酞试剂
C
除去 CO2 中的 CO
点燃混合气体
D
除去 KCl 溶液中的 Na2SO4
加入氯化钡溶液
A、A B、B C、C D、D14. 为探究影响化学反应速率的因素,在等质量的大理石中加入足量的酸溶液(杂质不与酸反应),产生的 CO2体积随时间的变化曲线如图所示。以下说法正确的是( )
实验编号
药品
I
块状大理石 10%H2SO4溶液
II
块状大理石 7%HCl 溶液
Ⅲ
大理石粉末 7%HCl 溶液
A、图中丙对应的实验是Ⅲ B、甲对应实验中碳酸钙的利用率最高 C、对比乙、丙,影响化学反应速率的因素是酸的浓度 D、对比甲、乙,反应物接触面积越大,反应速率越快15. 关于阿司匹林(化学式为 C9H8O4)的说法正确的是( )A、摩尔质量为 180 B、氧元素的质量分数最小 C、碳、氢元素质量比为 9∶8 D、0.1mol 该物质约含有 6.02×1022 个分子二、多选题
-
16. 如图是电解水实验装置图,下列说法正确的是( )
 A、b 端连接的是电源的负极 B、a 处产生的气体能使带火星木条复燃 C、a 处与 b 处产生气体的体积比为 2∶1 D、此实验证明水是由氢元素和氧元素组成的17. 有关氧化物的说法正确的是( )A、氧化物一定含有氧元素 B、含有氧元素的物质是氧化物 C、能与酸反应生成盐和水的物质是碱性氧化物 D、能与碱反应生成盐和水的氧化物是酸性氧化物
A、b 端连接的是电源的负极 B、a 处产生的气体能使带火星木条复燃 C、a 处与 b 处产生气体的体积比为 2∶1 D、此实验证明水是由氢元素和氧元素组成的17. 有关氧化物的说法正确的是( )A、氧化物一定含有氧元素 B、含有氧元素的物质是氧化物 C、能与酸反应生成盐和水的物质是碱性氧化物 D、能与碱反应生成盐和水的氧化物是酸性氧化物三、填空题
-
18. 社会可持续发展离不开能源。(1)、如图,所占消费比例最大的能源是;
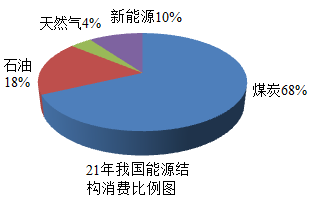 (2)、石油的主要成分是多种碳氢化合物,石油是(选填“混合物”或“纯净物”);(3)、煤燃烧会产生 CO2和 SO2等物质,其中会导致温室效应的是;(4)、天然气的主要成分是 CH4 , CH4由种元素组成;(5)、长征 5 号火箭采用液氢为燃料,写出液氢(H2)燃烧的化学方程式;(6)、科学家用“人工树叶”模拟光合作用,吸收 CO2 , 获得 O2 , 其反应的微观示意图如下:
(2)、石油的主要成分是多种碳氢化合物,石油是(选填“混合物”或“纯净物”);(3)、煤燃烧会产生 CO2和 SO2等物质,其中会导致温室效应的是;(4)、天然气的主要成分是 CH4 , CH4由种元素组成;(5)、长征 5 号火箭采用液氢为燃料,写出液氢(H2)燃烧的化学方程式;(6)、科学家用“人工树叶”模拟光合作用,吸收 CO2 , 获得 O2 , 其反应的微观示意图如下: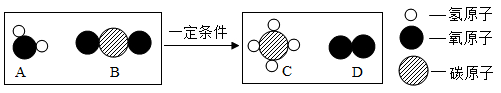
在该反应中,生成 C 和 D 的质量之比为。
19. 学习小组对常见的几种酸、碱、盐的相关知识进行了实验探究。(1)、实验一:比较两种酸的性质
C 试管中发生反应的化学方程式为;
(2)、对比(填写序号)中的实验,可说明稀盐酸和稀硫酸具有相似的化学性质;(3)、能得出金属活动性 Zn>Cu 的现象是:F 中无明显现象和。(4)、实验二:比较两种碱的性质
对比甲、乙实验,说明(选填“NaOH”、“Ca(OH)2”)固体具有吸水性;
(5)、丙、丁处反应产生的气体是。(6)、实验三:鉴别碳酸钠和氯化钾两瓶无色溶液填写下表。
实验方案
实验步骤
现象和结论
1
取样,分别滴入几滴无色酚酞试液
变色的是碳酸钠溶液,不变色的是氯化钾溶液。
2
分别用铂丝蘸取两种溶液放在酒精灯火焰上灼烧。
(7)、实验四:判断混合物的成分现有一瓶含有杂质的氯化钠固体(可能含有碳酸钙、碳酸钠、硝酸钡、硫酸钾中的一种或几种),为了判定成分,做了以下实验,烧杯中的固体质量随加入的水或稀盐酸质量的变化情况如下图所示。

原氯化钠固体中一定含有的物质是;
(8)、若原固体中含有 a mol NaCl,最终得到的溶液中含有 b mol NaCl,a 与 b 的关系是 a<b,理由是。20. 化学实验是学习化学的重要活动。根据下图实验回答问题:

(图中夹持仪器省略,白磷、红磷着火点分别是 40℃和 240℃)
(1)、能随时控制反应发生或停止的装置是(选填“A”或“C”);(2)、装置 A 中发生反应的化学方程式为 , 把装置 B 放在 80℃的热水中,白磷燃烧红磷不燃烧,说明可燃物燃烧的条件之一是;(3)、装置 D 中发生反应的化学方程式为;(4)、装置 E 中观察到的现象是 , 装置 F 的作用是;(5)、含 0.1mol 碳酸钙的大理石与足量稀盐酸完全反应,能生成二氧化碳g。21. 下图是 NH4Cl、NaCl、NaHCO3(碳酸氢钠)三种物质的溶解度曲线,回答下列问题: (1)、60℃时,NH4Cl 的溶解度是g/100g 水;(2)、能将接近饱和的 NaHCO3溶液转化为饱和溶液的一种方法是;(3)、60℃的饱和 NH4Cl 溶液中含有少量的 NaCl,提纯 NH4Cl 的方法是;(4)、20℃时,将 NH3、CO2通入饱和 NaCl 溶液中,可生成 NaHCO3和 NH4Cl,反应的化学方程式为:
(1)、60℃时,NH4Cl 的溶解度是g/100g 水;(2)、能将接近饱和的 NaHCO3溶液转化为饱和溶液的一种方法是;(3)、60℃的饱和 NH4Cl 溶液中含有少量的 NaCl,提纯 NH4Cl 的方法是;(4)、20℃时,将 NH3、CO2通入饱和 NaCl 溶液中,可生成 NaHCO3和 NH4Cl,反应的化学方程式为:
Ⅰ、以上过程中,操作 a 是 , 产物中可作氮肥的是;
Ⅱ、经测定,以上反应中,参加反应的 NaCl 的物质的量为 1mol,20℃的固液混合物中,NaHCO3固体首先析出,而 NH4Cl 固体不析出,请结合相关数据分析说明 。