上海市宝山区2022年中考二模化学试题
试卷更新日期:2022-08-10 类型:中考模拟
一、单选题
-
1. 氦气是常见的冶炼及焊接保护气,氦的元素符号是( )A、Hg B、He C、H D、Cl2. 在空气的成分中,体积分数约占21%的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体3. 灼烧时火焰呈黄色的物质是( )A、NaCl B、KNO3 C、CuCl2 D、BaSO44. 不含原子团的物质是( )A、KCl B、NaOH C、NH4NO3 D、CuSO45. 物质加入水中形成悬浊液的是( )A、植物油 B、泥沙 C、白糖 D、食盐6. 不属于物质化学性质的是( )A、可燃性 B、还原性 C、稳定性 D、吸附性7. 属于有机物的是( )A、CO2 B、CaCO3 C、H2CO3 D、CH48. 在氧气中燃烧生成黑色固体的是( )A、木炭 B、镁带 C、红磷 D、铁丝9. 下列物质可作复合肥的是( )A、NH4Cl B、CO(NH2)2(尿素) C、KNO3 D、Ca(H2PO4)210. 物质俗称正确的是( )A、Na2CO3:烧碱 B、Ag:水银 C、CuSO4:胆矾 D、CaO:生石灰11. 只含有游离态氧元素的物质是( )A、空气 B、水 C、液氧 D、二氧化碳12. 用
 表示不同种元素的原子,表示化合物的微观模拟图是( ) A、
表示不同种元素的原子,表示化合物的微观模拟图是( ) A、 B、
B、 C、
C、 D、
D、 13. 将X、Z两种金属分别放入Y(NO3)2的溶液中,仅X的表面有Y单质析出,则X、Y、Z三种金属的活动性顺序是( )A、Z>X>Y B、X>Y>Z C、X>Z>Y D、Y>X>Z14. 关于过氧化氢(H2O2)的说法正确的是( )A、过氧化氢由氢分子和氧分子构成的 B、过氧化氢由氢原子和氧原子构成的 C、过氧化氢的摩尔质量是34 D、过氧化氢中氢、氧原子物质的量比为1:115. 下列说法正确的是( )A、化合反应的反应物中一定有单质 B、分解反应的反应物一定是化合物 C、生成单质和化合物的反应一定属于置换反应 D、生成盐和水的反应一定属于复分解反应16. 除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
13. 将X、Z两种金属分别放入Y(NO3)2的溶液中,仅X的表面有Y单质析出,则X、Y、Z三种金属的活动性顺序是( )A、Z>X>Y B、X>Y>Z C、X>Z>Y D、Y>X>Z14. 关于过氧化氢(H2O2)的说法正确的是( )A、过氧化氢由氢分子和氧分子构成的 B、过氧化氢由氢原子和氧原子构成的 C、过氧化氢的摩尔质量是34 D、过氧化氢中氢、氧原子物质的量比为1:115. 下列说法正确的是( )A、化合反应的反应物中一定有单质 B、分解反应的反应物一定是化合物 C、生成单质和化合物的反应一定属于置换反应 D、生成盐和水的反应一定属于复分解反应16. 除去下列各组物质中的杂质,所用试剂和方法均正确的是( )选项
物质
杂质
除杂所用的试剂和方法
A
CaO固体
CaCO3固体
加入适量的稀盐酸
B
NaOH溶液
Ca(OH)2溶液
先加入过量的Na2CO3溶液,再过滤
C
干燥的CO
CO2
将气体缓缓通过足量NaOH溶液
D
BaSO4
BaCO3
加入足量稀硫酸,充分反应后,过滤
A、A B、B C、C D、D二、多选题
-
17. 常温下,对100mL硫酸铜饱和溶液进行如下图示实验。有关分析正确的是( )
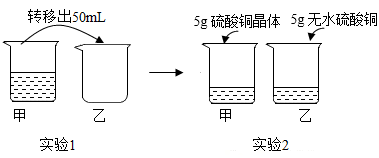 A、实验1后甲、乙烧杯中的溶液均为饱和溶液 B、实验2后甲、乙烧杯中的溶剂质量:m甲>m乙 C、实验2后甲、乙烧杯中的溶液质量:m甲=m乙 D、实验2后甲、乙烧杯中溶液的溶质质量分数:m甲<m乙
A、实验1后甲、乙烧杯中的溶液均为饱和溶液 B、实验2后甲、乙烧杯中的溶剂质量:m甲>m乙 C、实验2后甲、乙烧杯中的溶液质量:m甲=m乙 D、实验2后甲、乙烧杯中溶液的溶质质量分数:m甲<m乙三、填空题
-
18. 化学是一门研究物质的组成、结构、性质及变化规律的自然科学,用化学的相关知识完成下列填空。(1)、水在通电条件下反应的化学方程式为: , 正极和负极生成的气体体积比为: , 0.5mol水分子中含有氢原子个。(2)、下图为甲物质(CH3OH)燃烧的微粒示意图:

反应物甲属于(选填“有机物”或“无机物”),其摩尔质量为 , 丙物质过量排放会引起 , 反应中甲和丁的物质的量之比为。
19. 以下是NaCl、NH4Cl的溶解度表,请根据表格回答问题:温度/℃
10
20
30
40
50
60
溶解度(g/100g水)
NaCl
35.8
36.0
36.3
36.6
37.0
37.3
NH4Cl
33.5
37.2
41.4
45.8
50.4
55.2
(1)、溶解度受温度变化影响较小的物质是。(2)、30℃时,氯化钠的溶解度(填“>”、“=”或“<”)氯化铵的溶解度;(3)、氯化钠和氯化铵具有相同溶解度的温度范围为。(4)、甲是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到12.8gNH4Cl固体。
Ⅰ、操作1的名称是;
Ⅱ、丁烧杯中溶液的质量是g,甲、乙、丙、丁烧杯中属于不饱和溶液的是。
Ⅲ、对以上过程的分析,正确的是。
a.甲→乙过程中,溶质质量没有改变
b.丙→丁过程中,溶质质量减少
c.乙→丙过程中,开始析出NH4Cl固体的温度在40℃至50℃之间
20. 利用相关装置进行气体的制备及性质实验。
 (1)、图C所示气体收集方法的名称为。(2)、实验室取氯酸钾和二氧化锰的混合物3.0g制取氧气,可选择制取氧气的装置组合为(填装置编号)。反应过程中固体总质量随加热时间的变化如图所示,则消耗的氯酸钾物质的量为。(3)、利用E、F、G组合装置进行气体性质实验(不考虑酸和水的挥发)。回答下列问题:
(1)、图C所示气体收集方法的名称为。(2)、实验室取氯酸钾和二氧化锰的混合物3.0g制取氧气,可选择制取氧气的装置组合为(填装置编号)。反应过程中固体总质量随加热时间的变化如图所示,则消耗的氯酸钾物质的量为。(3)、利用E、F、G组合装置进行气体性质实验(不考虑酸和水的挥发)。回答下列问题:【问题1】E装置中发生的反应化学方程式为 , E装置的优点是。
(4)、【问题2】实验中,G装置中蜡烛熄灭的原因是。(5)、【问题3】F装置内:甲、丙为湿润的蓝色石蕊试纸,乙为干燥的蓝色石蕊试纸。实验中F装置内证明二氧化碳与水发生反应的现象是 , 证明二氧化碳的密度比空气大的实验依据是。21. 电解饱和食盐水可以制得烧碱,其反应原理为:。某化学实验室的电解器中残留有久置的电解液,兴趣小组同学对其溶质成分探究过程如下:
【提出问题】久置电解液中的溶质成分有哪些?
【作出猜想】可能有:氢氧化钠、氯化钠、碳酸钠
【设计方案】为确定上述猜想中的各成分,兴趣小组同学设计如下实验方案并进行实验。
 (1)、【搜集证据】
(1)、【搜集证据】①观察到试管甲中的现象为。
②根据试管乙中的现象,得出电解液中含有碳酸钠。电解液中之所以有碳酸钠的原因是(用化学方程式表示)。
③试管丙中反应的化学方程式为。
【实验结论】根据上述实验,得出结论:久置的电解液中含有氢氧化钠、氯化钠、碳酸钠;
(2)、【实验评价】请你评价上述实验方案及结论是否正确,是请简述理由,否请修改方案。。
-