江苏省盐城市滨海县2022年中考第二次调研化学试题
试卷更新日期:2022-08-10 类型:中考模拟
一、单选题
-
1. 2021年我国政府工作报告中提出“做好碳中和工作”。碳中和是指通过植树造林,节能减排等措施,抵消因人类活动产生的二氧化碳等温室气体排放量,达到相对“零排放”。下列行为不利于实现碳中和的是( )A、大量使用一次性餐具 B、使用新技术提高传统能源的利用效率 C、利用风能实现清洁发电 D、研发新工艺将二氧化碳转化为化工产品2. 生活、工作场所常见到一些警示图标。下列图标放置地点错误的是( )A、
 运输NaOH的车辆
B、
运输NaOH的车辆
B、 存放红磷的试剂柜
C、
存放红磷的试剂柜
C、 高铁车厢内
D、
高铁车厢内
D、 城市居民住宅区
3. 5月20日为“中国学生营养日”,青少年应关注营养与健康。下列有关说法正确的是( )A、微量元素氟能防治龋齿,补充越多越好 B、奶茶具有良好的口感,可取代水长期饮用 C、油脂是提供能量的重要物质,可大量食用 D、糖类是人体所需营养成分之一,每天应适量摄入4. 4月16日,我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断,液氦是制造超低温的“神器”。根据图中信息判断,下列关于氦的说法正确的是( )
城市居民住宅区
3. 5月20日为“中国学生营养日”,青少年应关注营养与健康。下列有关说法正确的是( )A、微量元素氟能防治龋齿,补充越多越好 B、奶茶具有良好的口感,可取代水长期饮用 C、油脂是提供能量的重要物质,可大量食用 D、糖类是人体所需营养成分之一,每天应适量摄入4. 4月16日,我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断,液氦是制造超低温的“神器”。根据图中信息判断,下列关于氦的说法正确的是( ) A、氦属于金属元素 B、氦的元素符号是He C、氦的相对原子质量是4.003g D、氦原子容易得到电子5. 抗击新冠肺炎疫情离不开化学知识和技术。下列说法错误的是( )A、高温消毒餐具,使病毒在高温下失去活性 B、使用医用酒精消毒要远离火源,因为酒精有可燃性 C、将酒精加工成免洗消毒凝胶,使酒精分子停止运动而不挥发 D、测定新冠病毒的组成和结构,有助于研发治疗新冠肺炎的药物6. 水是生命之源。下列关于水的操作正确的是( )A、活性炭净水器净水
A、氦属于金属元素 B、氦的元素符号是He C、氦的相对原子质量是4.003g D、氦原子容易得到电子5. 抗击新冠肺炎疫情离不开化学知识和技术。下列说法错误的是( )A、高温消毒餐具,使病毒在高温下失去活性 B、使用医用酒精消毒要远离火源,因为酒精有可燃性 C、将酒精加工成免洗消毒凝胶,使酒精分子停止运动而不挥发 D、测定新冠病毒的组成和结构,有助于研发治疗新冠肺炎的药物6. 水是生命之源。下列关于水的操作正确的是( )A、活性炭净水器净水 B、除水中不溶物
B、除水中不溶物  C、量水的体积
C、量水的体积  D、测水的pH
D、测水的pH  7. 下列物质用途主要由化学性质决定的是( )A、稀有气体填充霓虹灯 B、液氮制造低温环境 C、生石灰作食品干燥剂 D、木炭作冰箱除味剂8. 有关粉尘爆炸实验说法正确的是( )
7. 下列物质用途主要由化学性质决定的是( )A、稀有气体填充霓虹灯 B、液氮制造低温环境 C、生石灰作食品干燥剂 D、木炭作冰箱除味剂8. 有关粉尘爆炸实验说法正确的是( )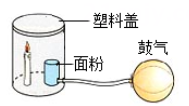 A、剧烈燃烧一定会引起爆炸 B、燃着的蜡烛可升高面粉着火点 C、鼓空气是为了增大氧气的含量 D、面粉加工厂必须严禁烟火9. 《齐民要术》中描述:“凡美田之法,绿豆为上,小豆、胡麻次之”,说明豆科植物与根瘤菌共生起固氮效果,使用豆科植物肥田可减少下列化肥使用量的是( )A、KCl B、K2SO4 C、Ca3(PO4)2 D、CO(NH2)210. 传统中药“金银花”的有效成分中含有一种名为绿原酸(C16H18O9)的物质,下列说法正确的是( )A、绿原酸由三种元素组成 B、绿原酸的相对分子质量为354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由碳、氢、氧原子构成11. 化学变化总伴随着能量的变化。如图为氢氧燃料电池的工作原理示意图。下列说法错误的是( )
A、剧烈燃烧一定会引起爆炸 B、燃着的蜡烛可升高面粉着火点 C、鼓空气是为了增大氧气的含量 D、面粉加工厂必须严禁烟火9. 《齐民要术》中描述:“凡美田之法,绿豆为上,小豆、胡麻次之”,说明豆科植物与根瘤菌共生起固氮效果,使用豆科植物肥田可减少下列化肥使用量的是( )A、KCl B、K2SO4 C、Ca3(PO4)2 D、CO(NH2)210. 传统中药“金银花”的有效成分中含有一种名为绿原酸(C16H18O9)的物质,下列说法正确的是( )A、绿原酸由三种元素组成 B、绿原酸的相对分子质量为354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由碳、氢、氧原子构成11. 化学变化总伴随着能量的变化。如图为氢氧燃料电池的工作原理示意图。下列说法错误的是( ) A、氢气是未来最理想的绿色能源 B、任何条件下都可实现物质或能量之间的相互转化 C、氢气燃烧生成水并放出大量的热是化学能转化为热能 D、氢氧燃料电池把氢气和氧气反应的化学能直接转化为电能12. 2021年中科院航天催化材料实验室将甲烷转化为甲醇(CH3OH,常温下是液态)实现了天然气的高效利用,反应历程如图所示。下列说法错误的是( )
A、氢气是未来最理想的绿色能源 B、任何条件下都可实现物质或能量之间的相互转化 C、氢气燃烧生成水并放出大量的热是化学能转化为热能 D、氢氧燃料电池把氢气和氧气反应的化学能直接转化为电能12. 2021年中科院航天催化材料实验室将甲烷转化为甲醇(CH3OH,常温下是液态)实现了天然气的高效利用,反应历程如图所示。下列说法错误的是( ) A、铁为该反应的催化剂 B、该过程中,CH4发生还原反应 C、生成CH3OH过程中,分子数目减少 D、将甲烷转化为甲醇有利于储存和运输13. 甲、乙、丙三种物质有如下转化关系: 。在不断搅拌下,往装有甲溶液的容器中持续通入CO2依次发生了①、②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( )
A、铁为该反应的催化剂 B、该过程中,CH4发生还原反应 C、生成CH3OH过程中,分子数目减少 D、将甲烷转化为甲醇有利于储存和运输13. 甲、乙、丙三种物质有如下转化关系: 。在不断搅拌下,往装有甲溶液的容器中持续通入CO2依次发生了①、②反应,同时测定容器中液体的透光度强度(液体越浑浊,透光强度越小),结果如图。下列分析错误的是( ) A、乙难溶于水 B、QM段对应的反应是② C、甲可能是NaOH D、E,F点溶质不同14. 下列实验方案不能达到实验目的的是( )
A、乙难溶于水 B、QM段对应的反应是② C、甲可能是NaOH D、E,F点溶质不同14. 下列实验方案不能达到实验目的的是( )选项
实验目的
实验方案
A
除去粗盐水中的 , 得到精盐水
加入过量的BaCl2溶液,充分反应后过滤
B
鉴别固体CaCO3、NaOH、NH4NO3
取样加水,观察溶解和温度的变化情况
C
除去FeCl2溶液中的CuCl2
加入过量的铁屑充分反应,过滤
D
鉴别棉纤维、涤纶、羊毛线
取样点燃,观察现象并闻气味
A、A B、B C、C D、D15. 下列说法错误的是( )A、某CaO和CaCO3的混合物中钙元素的质量分数为60%,将50g该混合物高温煅烧至固体质量不再改变,剩余固体的质量是42g B、NaHSO4与MgSO4的混合物中,硫的质量分数为26.67%,金属的质量分数为20% C、现有KOH和KCl的混合物20.5g,向其中加入100g质量分数为3.65%的稀盐酸,恰好完全反应,则原混合物中钾元素的质量为11.7g D、MgO、Al2O3和Fe粉的混合物9.9g,向其中加入245g质量分数为10%的稀硫酸,恰好完全反应,得到254.8g溶液,则原混合物中MgO的质量为2g。二、填空题
-
16. 化学在生产,生活中有着广泛应用。(1)、现有a.熟石灰 b.碳酸氢钠 c.氯化钠 d.空气,选择适当的物质填空(填序号)。
①可用作厨房调味品的是;
②可用于焙制糕点的是;
③可用来改良酸性土壤的是;
④工业上高炉炼铁的原料之一是;
(2)、2021年5月,“天问一号”搭我祝融号火星车成功着陆火星。①火星车使用的新型镁锂合金属于(填“金属”或“合成”)材料。
②火星车热控材料—纳米气疑胶的主要成分是二氧化硅,化学式为。
③火星车集热窗内装有正十一烷(C11H24),此物质属于(填“无机物”或“有机物”),其中碳、氢元素的质量比为。
④火星车动力来源于太阳能,人类正在利用和开发的新能源还有(写一种)。
17. 下图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。
温度/℃
20
60
100
溶解度
(g)
NaCl
36.0
37.3
39.8
MgCl2
54.8
61.3
73.0
(1)、“晒结浮白”指海水浸渍草灰,日晒后出现白色盐颗粒的过程,化学上称之为。(2)、经“扫而复淋”,获得“上等卤水”(NaCl的质量分数为15%)用于煎炼海盐。①1000g“上等卤水”蒸干后,可得到氯化钠的质量约为g。
②从燃料利用角度分析,用“上等卤水”而不直接用海水煎炼海盐的原因是。
③将“上等卤水”在100℃恒温蒸发至刚有晶体析出,所得溶液组成为:150g溶液中含水100g、NaCl39.8g、MgCl27.65g及其他成分2.55g。将150g此溶液降温至20℃,有gNaCl析出(溶解度见上表)。此时,(选填“有”或“没有”)MgCl2析出,原因是。
三、综合题
-
18. 根据下列装置或仪器,结合所学化学知识,回答下列问题:
 (1)、图中仪器①的名称是、仪器②的名称是。(2)、实验室欲制取并收集较纯净的氧气,小华同学已选用A装置作为发生装置,则他还需要选择的装置或仪器有(填序号),该反应的化学方程式是。小华利用上述方法收集到的氧气不纯,导致其不纯的原因可能是(任写出一点)。(3)、实验室利用硫化亚铁(FeS)固体和稀硫酸混合制取硫化氢气体,通常选择的发生装置是(填序号)。这个反应属于复分解反应,对应的化学方程式是。19. 科学家利用物质间转化创造新物质,服务于生产和生活。(1)、某工厂生产高锰酸钾的流程如下:
(1)、图中仪器①的名称是、仪器②的名称是。(2)、实验室欲制取并收集较纯净的氧气,小华同学已选用A装置作为发生装置,则他还需要选择的装置或仪器有(填序号),该反应的化学方程式是。小华利用上述方法收集到的氧气不纯,导致其不纯的原因可能是(任写出一点)。(3)、实验室利用硫化亚铁(FeS)固体和稀硫酸混合制取硫化氢气体,通常选择的发生装置是(填序号)。这个反应属于复分解反应,对应的化学方程式是。19. 科学家利用物质间转化创造新物质,服务于生产和生活。(1)、某工厂生产高锰酸钾的流程如下:
①“混合加热室”发生的主要是(选填“物理变化”或“化学变化”);
②“电解室”反应中,反应前后化合价发生变化的元素有(写元素符号)。
③生产流程中可循环利用的物质是(写化学式)。
④写出氧化室中发生反应的化学方程式。
(2)、A、B、C、D、E、F是初中化学常见的六种物质。A、B、D、E、F均由三种元素组成;A、B属于同类别的物质;固态C物质俗称干冰;A、E均合有人体中含量最多的金属元素;F可用于玻璃、造纸、纺织、洗涤剂的生产。部分反应物和产物已经略去,其中“一”表示两种物质间会反应,“→”表示一种物质会一步转化成另一种物质。
①E的化学式是 , D溶液中一定含有的阳离子是。
②写出化学方程式A→B。
20. 钢铁是现代工业的筋骨,科技小组以“铁锈蚀”为主题开展如下项目式学习。【查阅资料】
Ⅰ.氯化钙固体可作干燥剂。
Ⅱ.常温常压,氢气密度是0.089g/L。
III.
(1)、任务一:定性探究铁锈蚀取三枚相同的洁净无锈铁钉分别放入试管,进行图1实验。



对比A、B、C试管中实验现象,说明铁锈蚀主要是与空气中的发生化学反应。
(2)、铁锈蚀后应及时除锈的原因是。(3)、任务二:定量探究铁锈蚀小组设计了图2装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,连接压强传感器、数据采集器,采集数据,绘制出压强随时间变化的曲线如图3.t1时刻利用注射器加入2mL饱和NaCl溶液,再将一只装有稀盐酸的注射器插到烧瓶上。充分反应后共生成气体(常温常压下)体积为224mL。
据图3,对比AB段和BC段说明 , t3时刻压强突然变大的原因是。
(4)、实验后,将烧瓶中剩余物质过滤、洗涤、晾干,得黑色固体,该黑色固体是。经计算,铁粉锈蚀后生成的氧化铁的质量是g。(5)、【实验反思】任务二中铁锈蚀比任务一中铁锈蚀快,你认为可能的原因是。