江苏省淮安市淮阴区2022年中考二模化学试题(二)
试卷更新日期:2022-08-10 类型:中考模拟
一、单选题
-
1. 下列变化中,属于化学变化的是( )A、粉笔折断
 B、棉纱织布
B、棉纱织布  C、木材燃烧
C、木材燃烧  D、汽油挥发
D、汽油挥发  2. 化学与人体健康密切相关。下列说法不科学的是()A、食用加铁酱油可预防贫血 B、合理摄入油脂有益身体健康 C、密闭的房间中可燃煤取暖 D、家庭装修时应使用环保材料3. 额温枪的红外温度传感器所用材料含有钽酸锂(LiTaOx)。钽酸锂中锂元素(Li)和钽元素(Ta)的化合价分别为+1、+5价,则x为( )A、1 B、2 C、3 D、44. “十四五”规划中指出:要构建生态文明体系,推动绿色发展,落实碳达峰行动方案,打好污染防治攻坚战,建设美丽中国。下列不利于生态环境保护的是( )A、工业上“三废”达标再排放 B、推广使用一次性木筷、纸杯 C、少开私家车,倡导绿色出行 D、植树造林,增大绿化面积5. 下列图示实验操作正确的是( )A、
2. 化学与人体健康密切相关。下列说法不科学的是()A、食用加铁酱油可预防贫血 B、合理摄入油脂有益身体健康 C、密闭的房间中可燃煤取暖 D、家庭装修时应使用环保材料3. 额温枪的红外温度传感器所用材料含有钽酸锂(LiTaOx)。钽酸锂中锂元素(Li)和钽元素(Ta)的化合价分别为+1、+5价,则x为( )A、1 B、2 C、3 D、44. “十四五”规划中指出:要构建生态文明体系,推动绿色发展,落实碳达峰行动方案,打好污染防治攻坚战,建设美丽中国。下列不利于生态环境保护的是( )A、工业上“三废”达标再排放 B、推广使用一次性木筷、纸杯 C、少开私家车,倡导绿色出行 D、植树造林,增大绿化面积5. 下列图示实验操作正确的是( )A、 稀释浓硫酸
B、
稀释浓硫酸
B、 夹持蒸发皿
C、
夹持蒸发皿
C、 测定pH
D、
测定pH
D、 O2验满
6. 近年来,一些手机厂商纷纷发布自己的可折叠手机,化学物质吡唑啉是生产折叠手机用的柔性屏幕的重要物质,其化学式是C3H6N2 , 下列有关吡唑啉C3H6N2的说法正确的是( )A、吡唑啉属于有机高分子化合物 B、吡唑啉由11个原子构成的 C、吡唑啉中碳元素质量分数最大 D、吡唑啉的相对分子质量为70g7. 某反应前后分子变化的微观示意图如下、下列说法正确的是( )
O2验满
6. 近年来,一些手机厂商纷纷发布自己的可折叠手机,化学物质吡唑啉是生产折叠手机用的柔性屏幕的重要物质,其化学式是C3H6N2 , 下列有关吡唑啉C3H6N2的说法正确的是( )A、吡唑啉属于有机高分子化合物 B、吡唑啉由11个原子构成的 C、吡唑啉中碳元素质量分数最大 D、吡唑啉的相对分子质量为70g7. 某反应前后分子变化的微观示意图如下、下列说法正确的是( )
 A、反应有单质生成 B、反应前后原子种类、数目不变 C、反应物和生成物共有8种物质 D、该反应为置换反应8. 节能减排中“减排”的关键是减少CO2的排放,而“减排”的重要手段是合理利用CO2。科学家利用CO2为原料制取炭黑的流程如图。下列说法错误的是( )
A、反应有单质生成 B、反应前后原子种类、数目不变 C、反应物和生成物共有8种物质 D、该反应为置换反应8. 节能减排中“减排”的关键是减少CO2的排放,而“减排”的重要手段是合理利用CO2。科学家利用CO2为原料制取炭黑的流程如图。下列说法错误的是( ) A、过程2的变化中太阳能转化为化学能 B、过程1和过程2的变化都属于分解反应 C、此流程中有炭黑生成,还有氧气生成 D、此流程还需要解决炭黑和Fe3O4的分离问题9. 下列实验操作不能达到实验目的的是( )
A、过程2的变化中太阳能转化为化学能 B、过程1和过程2的变化都属于分解反应 C、此流程中有炭黑生成,还有氧气生成 D、此流程还需要解决炭黑和Fe3O4的分离问题9. 下列实验操作不能达到实验目的的是( )选项
目的
主要操作
A
辨别“羊毛制品”真假
取样,灼烧,闻气味
B
检验土豆中淀粉的存在
取样,滴加少量碘酒
C
配制溶质质量分数为5%的蔗糖溶液
取5g蔗糖,溶于100g水
D
除去氯化钙溶液中混有的少量盐酸
加过量的碳酸钙,搅拌,过滤
A、A B、B C、C D、D10. 下列有关量的变化图像与其对应叙述相符的是 ( )A、 将浓硫酸长时间敞口放置于空气中
B、
将浓硫酸长时间敞口放置于空气中
B、 把一定质量的 NaOH 和 NH4NO3固体分别溶于水
C、
把一定质量的 NaOH 和 NH4NO3固体分别溶于水
C、 向盛有一定质量稀盐酸的烧杯中加入过量的锌粉
D、
向盛有一定质量稀盐酸的烧杯中加入过量的锌粉
D、 向等质量的锌粉和铁粉中分别加入等质量、等质量分数的足量稀盐酸
向等质量的锌粉和铁粉中分别加入等质量、等质量分数的足量稀盐酸
二、填空题
-
11. 化学在生产、生活中有着广泛应用。现有①石墨 ②钛合金 ③硝酸钾 ④碳酸钠 ⑤碳酸氢钠,选择适当的物质填空(填序号)。(1)、属于复合肥料的是。(2)、可作干电池电极的是。(3)、俗称小苏打的是。(4)、可用来制造人造骨的是。12. 化学源于生活、生产、科技,又用于生活、生产、科技。(1)、“砂锅鱼头”汤鲜汁浓,其烹饪方法为:将鱼头下油锅煎黄后,放入砂锅中加适量食盐、葱段、生姜、香菜、矿泉水等,在火上煨煮数小时即成。“砂锅鱼头”中几乎不含有的营养素是(填字母序号)。用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,此时可将灶具的进风口调大(填“调大”或“调小”)。
A.无机盐 B.油脂 C.糖类 D.水
(2)、新能源汽车越来越受到人们的青睐,华晨宝马530Le新能源汽车定位系统微电脑控制器应用了一种新型材料氮化铝(AlN)。工业上在氮气流中由氧化铝与焦炭在高温条件下制得氮化铝,并生成一种可燃性气体,该反应的化学方程式为。(3)、结合下图所示实验,回答下列问题。
①实验一的目的是利用浓氨水的碱性和挥发性,验证。
②实验二中,在B试管加入(写出一种情况),即可证明温度和固体颗粒大小都是影响冰糖溶解快慢的因素。
③实验三中,通过测定水和氯化钠混合前后的质量不能用来验证质量守恒定律,原因是。
13. 2022年3月23日国家发改委发布《氢能产业发展中长期规划2021-2035年》。规划明确提出:到2025年,部署建设一批加氢站,可再生能源制氢量达10-20万吨/年,实现二氧化碳减排100-200万吨/年等。(1)、除氢能外,请再列举一种可再生能源:。(2)、用天然气制氢是我国最主要的制氢来源。天然气制氢其工艺原理是在转化炉中将甲烷和水蒸气转化为一氧化碳和氢气,余热回收后,在变换塔中,催化剂存在的条件下,控制反应温度,使一氧化碳和水反应,生成氢气和二氧化碳。请写出转化炉中发生反应的化学方程式:。(3)、2022北京冬奥会秉承“绿色办奥”理念,其中如下图“雪花”造型的主火炬使用的燃料就是氢气,主要利用了氢能的优点是。 14. 水是生命之源,万物之基,与人类的生产生活密切相关。(1)、含有较多可溶性钙、镁化合物的水通常称为硬水,生活中可用来检验地下水是硬水还是软水;生活中常用的方法,既可降低水的硬度,又能杀菌消毒。(2)、①研究人员开发出一种用超临界水处理含碳废物的新技术。超临界水是将水加热到超过374℃并加压到超过219个大气压,使水处于气、液相互交融的状态。下列说法正确的是(填字母序号)。
14. 水是生命之源,万物之基,与人类的生产生活密切相关。(1)、含有较多可溶性钙、镁化合物的水通常称为硬水,生活中可用来检验地下水是硬水还是软水;生活中常用的方法,既可降低水的硬度,又能杀菌消毒。(2)、①研究人员开发出一种用超临界水处理含碳废物的新技术。超临界水是将水加热到超过374℃并加压到超过219个大气压,使水处于气、液相互交融的状态。下列说法正确的是(填字母序号)。
A.超临界水与液态水具有相同的物理和化学性质
B.将气态水升温或加压一定使水分子间距离变小
C.超临界水是由液态水和气态水组成的混合物
D.用超临界水处理含碳废物的方法比焚烧法更环保
②新型复合光催化剂(C3N4/CQDs)催化下,利用太阳光高效分解水的原理如图:

反应Ⅰ属于基本反应类型中的反应;反应Ⅱ的化学方程式为。
15. 硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。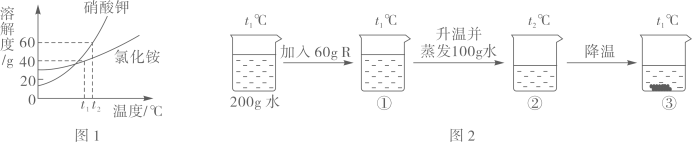 (1)、硝酸钾和氯化铵两种物质的溶解度均随温度的升高而。(2)、由图1可知:t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为。(3)、结合图1和图2判断:烧杯内的物质R是。①、②、③三种情况下,一定是饱和溶液的有(填序号)。
(1)、硝酸钾和氯化铵两种物质的溶解度均随温度的升高而。(2)、由图1可知:t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为。(3)、结合图1和图2判断:烧杯内的物质R是。①、②、③三种情况下,一定是饱和溶液的有(填序号)。三、综合题
-
16. 下图为实验室制取并收集气体的装置图,回答下列问题。

 (1)、a仪器的名称是。(2)、实验室用高锰酸钾制取并收集干燥的氧气应选用的装置组合是(填序号)。(3)、若用F装置收集并测量氧气的体积,应在(填“d”或“e”)段连接量筒。(4)、用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在(填“b”或“c”)。17. 利用废镍催化剂(主要成分:Ni,还含有少量的Zn、Fe、CaO等杂质)制备NiCO3的实验流程如下(虚线处部分流程略去):
(1)、a仪器的名称是。(2)、实验室用高锰酸钾制取并收集干燥的氧气应选用的装置组合是(填序号)。(3)、若用F装置收集并测量氧气的体积,应在(填“d”或“e”)段连接量筒。(4)、用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在(填“b”或“c”)。17. 利用废镍催化剂(主要成分:Ni,还含有少量的Zn、Fe、CaO等杂质)制备NiCO3的实验流程如下(虚线处部分流程略去):
已知:Na2CO3溶液能使无色酚酞溶液变红。碱性条件下NiSO4转化为Ni(OH)2沉淀。
(1)、“酸溶”时,为使废镍充分溶解,可采取的措施有(任写一种)。(2)、“氧化”阶段发生的反应为 , 则a=。(3)、“除铁”的目的是除去溶液中的Fe3+。改变温度、pH,Fe3+转化所得产物可能不同(如图)。80℃、pH=6时,Fe3+转化为(填化学式)。 (4)、“沉镍”是将Na2CO3溶液加入NiSO4溶液中生成NiCO3沉淀,反应的化学方程式为。 该过程不能将NiSO4溶液滴入Na2CO3溶液中,其原因是。18. 过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究。
(4)、“沉镍”是将Na2CO3溶液加入NiSO4溶液中生成NiCO3沉淀,反应的化学方程式为。 该过程不能将NiSO4溶液滴入Na2CO3溶液中,其原因是。18. 过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究。【查阅资料】:过氧化钠能与空气中的水反应生成氧气:2Na2O2+2H2O═4NaOH+O2↑。
过氧化钠能与空气中的二氧化碳反应生成氧气:2Na2O2+2CO2═2Na2CO3+O2。
氯化钙溶液显中性。
【提出问题】:过氧化钠是否变质?
【猜想与假设】:假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质。
(1)、【实验探究】:序号
实验步骤
实验现象
实验结论
①
取部分固体于试管中,加入适量的水,在试管口插入带火星的木条
固体完全溶解,木条
假设3不成立
②
取少量①中溶液于试管中,滴加足量的 , 振荡
有气泡生成
假设2成立
(2)、【提出新问题】:部分变质的过氧化钠样品中是否含有氢氧化钠呢?【实验探究】:实验③:取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红。
【定性分析】:
①由实验③可以确定①中溶液含有的溶质是(填字母序号)。
a.NaOH b.Na2CO3 c.NaOH、Na2CO3
②小美认为,由上述实验无法确定原固体药品中是否含有氢氧化钠,理由是。
(3)、【定量分析】:称取6.04g过氧化钠样品于锥形瓶中,加入适量蒸馏水使固体完全溶解,通过收集到0.64g气体从而算出样品中过氧化钠的质量为3.12g;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g。求6.04g上述样品中含有NaOH的质量(写出计算过程)。(4)、【反思提高】:过氧化钠长时间露置在空气中会全部变质,最终转化为(填化学式)。