吉林省长春市汽车经济开发区2022年中考三模化学试题
试卷更新日期:2022-08-10 类型:中考模拟
一、单选题
-
1. 下列日常劳动中主要涉及化学变化的是( )A、淘米洗菜 B、引火煮饭 C、清水擦地 D、整理书籍2. 物质由微观粒子构成,下列物质由分子构成的是( )A、铜 B、二氧化碳 C、金刚石 D、氯化钠3. 下列基本实验操作错误的是( )A、加热液体
 B、测液体 pH
B、测液体 pH  C、滴加液体
C、滴加液体  D、称量固体
D、称量固体 4. 下列场所或位置的标识使用有误的是( )A、洗手间
4. 下列场所或位置的标识使用有误的是( )A、洗手间 B、面粉厂
B、面粉厂  C、放酒精的试剂柜
C、放酒精的试剂柜 D、运输鞭炮的车
D、运输鞭炮的车 5. 生活中处处蕴含着化学知识。下列说法正确的是( )A、大量使用食品添加剂使食物更加美味 B、农业上用熟石灰改良酸性土壤 C、医疗上用烧碱治疗胃酸过多 D、可多使用化肥以增加粮食的产量6. 豆腐是中华美食之一,它能提供多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2)。下列关于亮氨酸的说法正确的是( )A、亮氨酸由 22 个原子构成 B、亮氨酸相对分子质量为 131g C、亮氨酸属于有机物 D、亮氨酸中氮元素的质量分数最小7. 太空水球“沸腾”了!中国空间站首次太空授课!在“天宫课堂”中,将泡腾片放入蓝色水球中,失重环境下,泡腾片不断产生气泡,却始终不会离开水球。下列有关说法错误的是( )
5. 生活中处处蕴含着化学知识。下列说法正确的是( )A、大量使用食品添加剂使食物更加美味 B、农业上用熟石灰改良酸性土壤 C、医疗上用烧碱治疗胃酸过多 D、可多使用化肥以增加粮食的产量6. 豆腐是中华美食之一,它能提供多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2)。下列关于亮氨酸的说法正确的是( )A、亮氨酸由 22 个原子构成 B、亮氨酸相对分子质量为 131g C、亮氨酸属于有机物 D、亮氨酸中氮元素的质量分数最小7. 太空水球“沸腾”了!中国空间站首次太空授课!在“天宫课堂”中,将泡腾片放入蓝色水球中,失重环境下,泡腾片不断产生气泡,却始终不会离开水球。下列有关说法错误的是( ) A、失重环境下,水分子仍然在运动 B、泡腾片在水中发生了化学反应 C、失重环境下,水分子数目变多 D、在太空中,水分子间依然有间隔8. 逻辑推理是学习化学常用的思维方法,下列分析推理正确的是( )A、氧化物中一定含有氧元素,因此含有氧元素的物质一定是氧化物 B、酸中含有氢元素,因此含有氢元素的物质就是酸 C、氢氧化钠和氢氧化钙都属于碱,因此用氢氧化钠溶液也可以检验二氧化碳 D、糖类是人体供能的主要物质,因此饮食中要适量摄入含糖类的物质9. 实验创新可以使现象更明显,操作更简便。Y型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y型管设计了以下三个实验进行探究活动,下列说法错误的是( )
A、失重环境下,水分子仍然在运动 B、泡腾片在水中发生了化学反应 C、失重环境下,水分子数目变多 D、在太空中,水分子间依然有间隔8. 逻辑推理是学习化学常用的思维方法,下列分析推理正确的是( )A、氧化物中一定含有氧元素,因此含有氧元素的物质一定是氧化物 B、酸中含有氢元素,因此含有氢元素的物质就是酸 C、氢氧化钠和氢氧化钙都属于碱,因此用氢氧化钠溶液也可以检验二氧化碳 D、糖类是人体供能的主要物质,因此饮食中要适量摄入含糖类的物质9. 实验创新可以使现象更明显,操作更简便。Y型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y型管设计了以下三个实验进行探究活动,下列说法错误的是( )
 A、图甲实验,一段时间后,观察到Y型管右侧湿润的蓝色石蕊试纸变红,说明二氧化碳显酸性 B、图乙实验,一段时间后,缓慢倾斜Y型管,将右侧的稀硫酸部分倒入左侧,可比较锌和铜的金属活动性 C、图丙实验,根据Y型管左侧红磷燃烧,右侧红磷不燃烧,可得到的实验结论是物质燃烧需要达到可燃物的着火点 D、图丙实验中气球可以防止红磷燃烧产生的P2O5污染空气10. 下列制备有关物质所设计的途径中,错误的是( )A、 B、 C、 D、
A、图甲实验,一段时间后,观察到Y型管右侧湿润的蓝色石蕊试纸变红,说明二氧化碳显酸性 B、图乙实验,一段时间后,缓慢倾斜Y型管,将右侧的稀硫酸部分倒入左侧,可比较锌和铜的金属活动性 C、图丙实验,根据Y型管左侧红磷燃烧,右侧红磷不燃烧,可得到的实验结论是物质燃烧需要达到可燃物的着火点 D、图丙实验中气球可以防止红磷燃烧产生的P2O5污染空气10. 下列制备有关物质所设计的途径中,错误的是( )A、 B、 C、 D、二、填空题
-
11. 用化学用语填空。(1)、氮元素 ;(2)、氮分子 ;(3)、铵根离子 。12. 钙元素是人体中重要的常量元素,如图是钙元素的相关信息。回答下列问题:
 (1)、钙原子的质子数为 ;(2)、钙属于(填“金属”“非金属”或“稀有气体”)元素;(3)、老年人长期缺钙,易患疾病。13. 水与人类的生产、生活密切相关。回答下列问题:(1)、新版《生活饮用水卫生标准》中的水质检测修订了镉、铅等的限量。这里的镉、铅指的是____(填序号)。A、原子 B、分子 C、元素 D、单质(2)、“生命吸管”是军事上的重要发明,它可以解决士兵在野外极限环境中饮水问题,主要原理与自来水的净化过程相似(如图)。图中过滤棉的作用是____(填字母);
(1)、钙原子的质子数为 ;(2)、钙属于(填“金属”“非金属”或“稀有气体”)元素;(3)、老年人长期缺钙,易患疾病。13. 水与人类的生产、生活密切相关。回答下列问题:(1)、新版《生活饮用水卫生标准》中的水质检测修订了镉、铅等的限量。这里的镉、铅指的是____(填序号)。A、原子 B、分子 C、元素 D、单质(2)、“生命吸管”是军事上的重要发明,它可以解决士兵在野外极限环境中饮水问题,主要原理与自来水的净化过程相似(如图)。图中过滤棉的作用是____(填字母);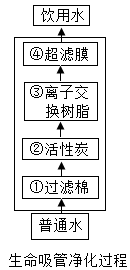 A、去除有害菌和部分病毒 B、除去颗粒较大的难溶性物质(3)、通过“生命吸管”净化后的水属于(填“纯净物或“混合物”);(4)、若无“生命吸管”,要杀灭天然水中的病原微生物,生活中常采取方法。14. 黄铜(铜锌合金)外观和黄金相似,被称为“假黄金”。某同学运用所学的化学知识,提出了鉴别真假黄金的几种方法。回答下列问题:(1)、待测样品与锌片相互刻画,现象,说明该样品是假黄金(黄铜);(2)、将待测样品在酒精灯上加热,表面变黑,说明该样品是(填“真”或“假”)黄金;(3)、将待测样品于支试管中,加入适量硫酸铜溶液,出现现象,说明该样品是假黄金(黄铜)。15. 如图是甲、乙两种固体物质的溶解度曲线,回答下列问题。
A、去除有害菌和部分病毒 B、除去颗粒较大的难溶性物质(3)、通过“生命吸管”净化后的水属于(填“纯净物或“混合物”);(4)、若无“生命吸管”,要杀灭天然水中的病原微生物,生活中常采取方法。14. 黄铜(铜锌合金)外观和黄金相似,被称为“假黄金”。某同学运用所学的化学知识,提出了鉴别真假黄金的几种方法。回答下列问题:(1)、待测样品与锌片相互刻画,现象,说明该样品是假黄金(黄铜);(2)、将待测样品在酒精灯上加热,表面变黑,说明该样品是(填“真”或“假”)黄金;(3)、将待测样品于支试管中,加入适量硫酸铜溶液,出现现象,说明该样品是假黄金(黄铜)。15. 如图是甲、乙两种固体物质的溶解度曲线,回答下列问题。 (1)、t1℃时,甲和乙的溶解度比较:甲乙(填“>”“<”或“=”);(2)、t2℃时,向 50g 水中加入 30g 甲固体,所得溶液是(填“饱和”或“不饱和”)溶液;(3)、下列说法错误的是____。A、t2℃时,将乙溶液的状态由 M 点变为 N 点,可采取降温的方法 B、t2℃时,将等质量的甲、乙的饱和溶液降温至 t1℃,析出固体的质量关系是:甲>乙 C、t1℃时,分别向甲、乙的饱和溶液中加入等质量的水,所得溶液的质量分数仍相等16. “宏—微—符”之间建立联系,有助于我们认识物质的本质。浓度为 75%的酒精常用作防疫消毒液,其有效成分是乙醇,如图是工业上在一定条件下制取乙醇(C2H5OH)的微观示意图,回答下列问题:
(1)、t1℃时,甲和乙的溶解度比较:甲乙(填“>”“<”或“=”);(2)、t2℃时,向 50g 水中加入 30g 甲固体,所得溶液是(填“饱和”或“不饱和”)溶液;(3)、下列说法错误的是____。A、t2℃时,将乙溶液的状态由 M 点变为 N 点,可采取降温的方法 B、t2℃时,将等质量的甲、乙的饱和溶液降温至 t1℃,析出固体的质量关系是:甲>乙 C、t1℃时,分别向甲、乙的饱和溶液中加入等质量的水,所得溶液的质量分数仍相等16. “宏—微—符”之间建立联系,有助于我们认识物质的本质。浓度为 75%的酒精常用作防疫消毒液,其有效成分是乙醇,如图是工业上在一定条件下制取乙醇(C2H5OH)的微观示意图,回答下列问题: (1)、该反应中涉及的氧化物的化学式;(2)、该反应的基本反应类型是;(3)、参加反应的甲、乙两物质的质量比为。
(1)、该反应中涉及的氧化物的化学式;(2)、该反应的基本反应类型是;(3)、参加反应的甲、乙两物质的质量比为。三、综合题
-
17. 图甲某同学整理的六种可以制得氧气的途径,A--F 为实验室制气常见的制取气体的装置。回答下列问题:

 (1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图甲中选择实验室制取氧气的最佳途径是(填序号),该反应的化学方程式为;(2)、若选择题图甲中的②制取较为纯净的氧气,应选择的装置为;(3)、电石(固体)主要成分为碳化钙,遇水立即发生激烈反应,生成乙炔气体(C2H2),密度比空气小、难溶于水。若实验室要制得平缓气流的乙炔气体,应该选用的发生装置是。18. 在丰富多彩的物质世界里,碳及其化合物占有重要地位,请回答相关问题。(1)、在书写具有保存价值的图书档案时,规定使用碳素墨水,其原因是;(2)、工业上,用赤铁矿炼铁的主要反应原理是: ,其中发生了还原反应的物质是(填化学式);(3)、化石燃料燃烧为我们提供能量的同时,使空气中 CO2含量增多。由此导致的环境问题是;(4)、“碳捕捉技术”常利用 NaOH 溶液来“捕捉”CO2 , 从而实现大规模 CO2减排。工艺流程如下图:
(1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图甲中选择实验室制取氧气的最佳途径是(填序号),该反应的化学方程式为;(2)、若选择题图甲中的②制取较为纯净的氧气,应选择的装置为;(3)、电石(固体)主要成分为碳化钙,遇水立即发生激烈反应,生成乙炔气体(C2H2),密度比空气小、难溶于水。若实验室要制得平缓气流的乙炔气体,应该选用的发生装置是。18. 在丰富多彩的物质世界里,碳及其化合物占有重要地位,请回答相关问题。(1)、在书写具有保存价值的图书档案时,规定使用碳素墨水,其原因是;(2)、工业上,用赤铁矿炼铁的主要反应原理是: ,其中发生了还原反应的物质是(填化学式);(3)、化石燃料燃烧为我们提供能量的同时,使空气中 CO2含量增多。由此导致的环境问题是;(4)、“碳捕捉技术”常利用 NaOH 溶液来“捕捉”CO2 , 从而实现大规模 CO2减排。工艺流程如下图:
①用 NaOH 溶液“捕捉”CO2的化学方程式是;
②分离池中分离出 CaCO3固体的操作是;
(5)、二氧化碳和氨气反应生成尿素(CO(NH2)2)和水,不仅有利于 CO2减排还能得到氮肥,该反应的方程式为。19. 酸碱盐是初中化学的重要物质,某同学通过下面的实验验证酸的相关性质。回答下列问题: (1)、把 50g 质量分数为 98℅的浓硫酸稀释为 20℅的硫酸,用于下列实验,需要水的质量是g ;(2)、试管 1 和试管 4 都能观察到的明显现象是 ;(3)、向反应后的试管 3 中滴加酚酞溶液,呈无色。下列试剂能用于确定溶液溶质成分的是____(填序号);A、锌粒 B、BaCl2溶液 C、纯碱 D、烧碱(4)、实验结束后,将实验中的所有液体倒入废液缸,检验废液呈酸性,向该废液中加入适量的____(填序号),处理后再排放。A、碳酸钙粉末 B、氢氧化钠 C、氢氧化铜 D、氢氧化钙20. 劳动课上,老师在演示制作馒头时,向已自然发酵的面粉中加入一种白色粉末,做出的馒头疏松多孔,口感更好。某化学兴趣小组的同学想探究这种“神奇粉末”的成分。老师指出白色粉末的成分只涉及到 Na2CO3和 NaHCO3。
(1)、把 50g 质量分数为 98℅的浓硫酸稀释为 20℅的硫酸,用于下列实验,需要水的质量是g ;(2)、试管 1 和试管 4 都能观察到的明显现象是 ;(3)、向反应后的试管 3 中滴加酚酞溶液,呈无色。下列试剂能用于确定溶液溶质成分的是____(填序号);A、锌粒 B、BaCl2溶液 C、纯碱 D、烧碱(4)、实验结束后,将实验中的所有液体倒入废液缸,检验废液呈酸性,向该废液中加入适量的____(填序号),处理后再排放。A、碳酸钙粉末 B、氢氧化钠 C、氢氧化铜 D、氢氧化钙20. 劳动课上,老师在演示制作馒头时,向已自然发酵的面粉中加入一种白色粉末,做出的馒头疏松多孔,口感更好。某化学兴趣小组的同学想探究这种“神奇粉末”的成分。老师指出白色粉末的成分只涉及到 Na2CO3和 NaHCO3。【提出问题】这种“神奇粉末”的成分是什么?
【查阅资料】
①NaHCO3溶液呈碱性;
②碳酸钠受热不分解,NaHCO3加热能发生分解反应,
③NaHCO3不与 CaCl2发生反应。
(1)、【提出猜想】猜想1:该粉末是 Na2CO3; 猜想 2 :该粉末是 NaHCO3;猜想3 :该粉末是。
(2)、【实验与现象】实验过程与现象如下图:
【问题与讨论】
根据步骤①②,甲同学认为猜想 1 一定正确,乙同学认为根据步骤①②的实验现象,不能得该结论,请解释其原因 ;
结合步骤③现象及查阅资料,可知猜想一定不对;
步骤④中加热至固体质量不再改变,将生成的气体全部通入足量澄清石灰水中,得到白色沉淀 a 经洗涤、干燥后称量质量 2.5g,白色沉淀 b 的质量(填“等于”“小于”或“大于”)2.5g,可得出猜想 3 正确的结论;
(3)、【实验与反思】小斌同学指出只要向步骤①所得溶液中加入足量的CaCl2溶液,出现现象,也可以得出相同的结论;
(4)、【拓展与应用】①Na2CO3固体中混有少量 NaHCO3 , 可采用(填序号)的方法除去;
A.加盐酸 B.通入 CO2 C.加热
②该白色粉末保存时应注意 。