吉林省长春市二道区2022年中考一模化学试题
试卷更新日期:2022-08-10 类型:中考模拟
一、单选题
-
1. 下列变化,属于物理变化的是( )A、蜡烛燃烧 B、冰雪融化 C、粮食酿酒 D、食物腐烂2. 下列可供人呼吸的气体是( )A、氧气 B、氢气 C、氮气 D、二氧化碳3. 下列物质中,由原子构成的是( )A、氯化钠 B、金刚石 C、氧气 D、氨气4. 下列有关试管的实验操作,正确的是( )A、仪器连接
 B、振荡试管
B、振荡试管 C、检查装置气密性
C、检查装置气密性 D、装入锌粒
D、装入锌粒 5. 将少量下列物质分别放入足量水中,充分搅拌,能形成溶液的是( )A、泥土 B、豆油 C、面粉 D、食盐6. 下表是人体内部分体液的正常pH范围,其中酸性最强的是( )
5. 将少量下列物质分别放入足量水中,充分搅拌,能形成溶液的是( )A、泥土 B、豆油 C、面粉 D、食盐6. 下表是人体内部分体液的正常pH范围,其中酸性最强的是( )选项
A.胃液
B.唾液
C.血浆
D.尿液
pH
0.9-1.5
6.6-7.1
7.35-7.45
4.7-8.4
A、A B、B C、C D、D7. 在北京冬奥会的场馆建设中用到了一种耐腐蚀、耐高温的表面涂料,该涂料是以某双环烯酯(C14H18O2)为原料制得的。下列有关该双环烯酯的说法正确的是( )A、相对分子质量是222g B、碳元素的质量分数最大 C、碳、氢元素的质量比为14:18 D、由34个原子构成8. 下列涉及学科观点的有关说法中,错误的是( )A、能量观:所有的化学反应都伴随着能量变化 B、分类观:水和二氧化锰都属于氧化物 C、元素观:水是由氢元素和氧元素组成 D、守恒观:镁条在空气中燃烧,反应前后固体的质量一定相等9. 碳及含碳物质有如图所示转化关系,下列说法错误的是( ) A、X可能是乙醇 B、加入的物质Y可以是稀硫酸 C、在转化①中,碳发生了还原反应 D、在转化②中,CO2和C在高温条件下可以生成CO10. 下列实验方案不合理的是( )A、检验NaOH溶液是否变质——取样,滴加足量的稀盐酸,观察是否有气泡产生 B、鉴别NaOH固体和NH4NO3固体——取样,分别溶解在水中,比较溶液温度 C、分离NaCl和CuCl2混合溶液——加入适量的NaOH溶液,过滤 D、除去N2中混有的少量O2——将混合气体通过足量灼热的铜网
A、X可能是乙醇 B、加入的物质Y可以是稀硫酸 C、在转化①中,碳发生了还原反应 D、在转化②中,CO2和C在高温条件下可以生成CO10. 下列实验方案不合理的是( )A、检验NaOH溶液是否变质——取样,滴加足量的稀盐酸,观察是否有气泡产生 B、鉴别NaOH固体和NH4NO3固体——取样,分别溶解在水中,比较溶液温度 C、分离NaCl和CuCl2混合溶液——加入适量的NaOH溶液,过滤 D、除去N2中混有的少量O2——将混合气体通过足量灼热的铜网二、填空题
-
11. 用化学用语回答问题:(1)、氮元素;(2)、2个镁原子;(3)、3个水分子。12. 坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,水更清,空气更清新”是我们共同的追求。(1)、我国力争在2060年实现碳中和,要实现碳中和,需减少煤、石油、等化石燃料的使用;(2)、天然水多为硬水,生活中降低水硬度的方法是;(3)、要使天更蓝水更清,必须努力改善空气质量。下列做法,有利于改善空气质量的是____。A、积极开展植树造林 B、提倡绿色出行,积极践行“低碳生活” C、就地焚烧农作物秸秆 D、大力开发利用太阳能、风能等新能源13. 如图为某品牌酸奶的营养成分表,请回答下列问题:
营养成分表
项目
每100g
NRV%
能量蛋白质
脂肪
碳水化合物
钠
钙
389kJ3.1g
3.1g
13.0g
65mg
85mg
5%5%
5%
4%
3%
11%
(1)、蛋白质属于(选填“无机物”或“有机物”);(2)、表中的“钠”、“钙”指的是(选填“单质”、“原子”或“元素”);(3)、表中列出的营养成分中,能为人体提供能量的是蛋白质、碳水化合物和。14. 人类的生活和生产都离不开金属材料。请回答下列问题:(1)、生活中常用铜做导线,主要是利用了铜的延展性和;(2)、生铁和钢性能不同,主要是因为二者不同;(3)、铁制品锈蚀的过程,实际上是铁跟空气中的同时接触发生化学反应的过程。15. 化学就在我们身边,它与我们的生活息息相关。请回答下列问题:(1)、俗语道“酒香不怕巷子深”,原因是(用微粒的观点解释);(2)、用加入洗洁精的水更易洗掉餐具上的油污,原因是洗洁精具有作用;(3)、可以用不同方法配制200g溶质的质量分数为10%的氢氧化钠溶液。①若用氢氧化钠固体和水来配制,需要氢氧化钠固体的质量是g;
②若用溶质的质量分数为20%的氢氧化钠溶液和水来配制,需要水的质量是g。
16. 清华大学化学工程学院研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇(CH3OH),其微观示意图如图所示。请回答下列问题: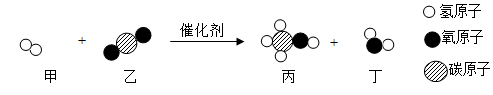 (1)、与反应前相比,反应后原子的总数(选填“增加“减少”或“不变”);(2)、甲、乙、丙、丁四种物质中属于单质的是;(3)、该反应的化学方程式为。17. 根据NaCl和KNO3两种固体物质的溶解度数据表,回答下列问题:
(1)、与反应前相比,反应后原子的总数(选填“增加“减少”或“不变”);(2)、甲、乙、丙、丁四种物质中属于单质的是;(3)、该反应的化学方程式为。17. 根据NaCl和KNO3两种固体物质的溶解度数据表,回答下列问题:温度/℃
0
20
40
60
80
100
溶解度/g
KNO3
13.3
31.6
63.9
110
169
246
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
(1)、40℃时,KNO3的溶解度是g:(2)、20℃时,将10gNaCl固体放入50g水中,若将其变成该温度下的饱和溶液,至少需要再加入NaClg;(3)、下列说法正确的是____。A.KNO3的溶解度大于NaClA、60℃时,向100g水中加入130gKNO3 , 可制得230gKNO3溶液 B、40℃时,若配制相等质量的KNO3、NaCl的饱和溶液,NaCl需要水的质量多 C、将KNO3的饱和溶液从60℃降温到20℃,过滤后得到的溶液仍然是KNO3的饱和溶液 D、在20℃到40℃之间的某一温度下,能配制出溶质质量分数相等的NaCl饱和溶液和KNO3饱和溶液三、综合题
-
18. 下列实验中均用到了红磷,请回答下列问题:
甲:测定空气中氧气的含量

乙:红磷燃烧前后质量的测定
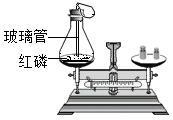
丙:探究燃烧的条件
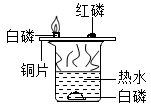 (1)、甲实验:能否将红磷换成铁丝来进行该实验?;(2)、乙实验:若取用红磷的量不足,对实验的结果是否有影响?;(3)、丙实验:通过铜片上的白磷燃烧而红磷不燃烧的实验现象,可以得出可燃物燃烧的条件之一是。19. 在某些食品包装袋内,有白色颗粒状固体的透气小纸袋,上面写着“石灰干燥剂,其主要成分为生石灰(CaO)”。请回答下列问题:(1)、生石灰能作干燥剂的原因是;(用化学方程式表示)(2)、已知小纸袋内含有2.8g生石灰,将其长期放置在空气中,若生石灰最终全部转化成碳酸钙,则理论上最终转化成碳酸钙的质量是多少?
(1)、甲实验:能否将红磷换成铁丝来进行该实验?;(2)、乙实验:若取用红磷的量不足,对实验的结果是否有影响?;(3)、丙实验:通过铜片上的白磷燃烧而红磷不燃烧的实验现象,可以得出可燃物燃烧的条件之一是。19. 在某些食品包装袋内,有白色颗粒状固体的透气小纸袋,上面写着“石灰干燥剂,其主要成分为生石灰(CaO)”。请回答下列问题:(1)、生石灰能作干燥剂的原因是;(用化学方程式表示)(2)、已知小纸袋内含有2.8g生石灰,将其长期放置在空气中,若生石灰最终全部转化成碳酸钙,则理论上最终转化成碳酸钙的质量是多少?解:设理论上最终转化成碳酸钙的质量是x。
由于CaO中的钙元素最终全部转化为CaCO3中的钙元素。
根据“化学反应前后钙元素的原子的种类、数目、质量不变”,
找出对应关系 CaO~CaCO3
写出相关的量 56 100
2.8g x
列出比例式
求解 x=g
答:理论上最终转化成的碳酸钙的质量是(略)。
20. 实验室利用如图装置制取常见的气体,请回答下列问题: (1)、仪器①的名称是;(2)、在实验室里,用装置B制取氧气,发生反应的化学方程式为;(3)、在常温下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室里,用加热氯化铵和氢氧化钙固体混合物的方法制取氮气,应选择的装置组合是(填字母)。
(1)、仪器①的名称是;(2)、在实验室里,用装置B制取氧气,发生反应的化学方程式为;(3)、在常温下,氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室里,用加热氯化铵和氢氧化钙固体混合物的方法制取氮气,应选择的装置组合是(填字母)。四、科学探究题
-
21. 归纳是学习化学的重要方法,小明用图1总结了酸的五条化学性质,请回答下列问题:

 (1)、稀盐酸和稀硫酸具有相似的化学性质,是因为它们的水溶液中都含有(填离子符号);(2)、醋酸是生活中常见的酸,将醋酸滴入紫色石蕊溶液中,观察到 , 由此能验证酸的性质1;(3)、将生锈的铁钉放入足量的稀硫酸中,可以观察到铁锈慢慢溶解,该反应的化学方程式为 , 将生锈的铁钉长时间浸泡后,还能观察到铁钉表面会产生 , 由此能验证酸的性质Ⅱ和Ⅲ;(4)、为了验证性质V,小明进行了如图2所示实验,当观察到 , 说明氢氧化钠和盐酸发生了化学反应,该反应的化学反应方程式。实验后,小明对得到的无色溶液中溶质的成分产生了兴趣,并进行了实验探究;(5)、【提出问题】反应后得到的无色溶液中溶质的成分是什么?
(1)、稀盐酸和稀硫酸具有相似的化学性质,是因为它们的水溶液中都含有(填离子符号);(2)、醋酸是生活中常见的酸,将醋酸滴入紫色石蕊溶液中,观察到 , 由此能验证酸的性质1;(3)、将生锈的铁钉放入足量的稀硫酸中,可以观察到铁锈慢慢溶解,该反应的化学方程式为 , 将生锈的铁钉长时间浸泡后,还能观察到铁钉表面会产生 , 由此能验证酸的性质Ⅱ和Ⅲ;(4)、为了验证性质V,小明进行了如图2所示实验,当观察到 , 说明氢氧化钠和盐酸发生了化学反应,该反应的化学反应方程式。实验后,小明对得到的无色溶液中溶质的成分产生了兴趣,并进行了实验探究;(5)、【提出问题】反应后得到的无色溶液中溶质的成分是什么?【猜想与假设】猜想一:酚酞、NaCl;猜想二:酚酞、NaCl、(填化学式);
(6)、【实验探究】取少量反应后的无色溶液于试管中,用pH试纸测得该无色溶液的pH7(选填“>”、“<”或“=”),推得猜想一成立;(7)、【查阅资料】a.Cu(OH)2是一种蓝色、不溶于水的碱;b.在溶液中Ag+和Cl-不共存,会产生白色沉淀AgCl。
【反思与评价】小明认为还可以用其它物质来检验无色溶液中溶质的成分。该物质可以是下列物质中的____(填序号)。
A、紫色石蕊溶液 B、Cu C、CuO D、AgNO3溶液 E、Cu(OH)2