2022年化学中考真题汇编:基本的实验技能(非选择题)
试卷更新日期:2022-08-09 类型:二轮复习
一、综合题
-
1. 某同学利用含MgCl2、Na2SO4、CaCl2杂质的粗盐,配制一定溶质质量分数的氯化钠溶液,他设计了如下实验流程,请结合物质溶解性表,回答下列问题。

部分物质在水中的溶解性表(室温)
阴离子
阳离子
OH﹣
Ba2+
溶
不溶
不溶
Ca2+
微溶
微溶
不溶
Mg2+
不溶
溶
微溶
(1)、步骤二中使用的三种试剂为:①Na2CO3溶液②BaCl2溶液③NaOH溶液,依次加入试剂的顺序为(填序号)。(2)、步骤二中加入足量NaOH溶液发生反应的化学方程式。(3)、若经过滤,滤液仍浑浊的原因可能是(填序号)。①滤纸破损
②液面高于滤纸边缘
③仪器不干净
(4)、步骤三操作X的名称是。用经X操作后得到的6gNaCl固体,配制溶质质量分数为6%的氯化钠溶液,所需水的质量为g。2. 我国古代提纯焰硝(含KNO3和少量NaCl、CaCl2等)工艺的主要过程示意如下: (1)、步骤中,“搅拌”的作用是(写一种)。(2)、步骤Ⅲ加小灰水(含K2CO3)时,发生反应的化学方程式为。(3)、下图为硝酸钾、氯化钠的溶解度曲线。步骤Ⅳ在较高温度下过滤的目的是。
(1)、步骤中,“搅拌”的作用是(写一种)。(2)、步骤Ⅲ加小灰水(含K2CO3)时,发生反应的化学方程式为。(3)、下图为硝酸钾、氯化钠的溶解度曲线。步骤Ⅳ在较高温度下过滤的目的是。 (4)、步骤V析出硝酸钾晶体的过程称之为。(5)、“溶液2”一定含有的溶质有KCl、和(填化学式)。3. 二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某学习组以此粉末为原料,设计以下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体[NH4Fe(SO4)2·xH2O]。
(4)、步骤V析出硝酸钾晶体的过程称之为。(5)、“溶液2”一定含有的溶质有KCl、和(填化学式)。3. 二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某学习组以此粉末为原料,设计以下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体[NH4Fe(SO4)2·xH2O]。
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液;②SiO2不溶于酸(氢氟酸除外)。
回答下列问题:
(1)、稀酸A是;(2)、操作①的名称为;(3)、滤渣2是(填化学式);(4)、滤液2中发生反应的化学方程式为:2Ce2(SO4)3+12NaOH+O2+2甲=4Ce(OH)4↓+6Na2SO4 , 甲的化学式是;(5)、硫酸铁铵[NH4Fe(SO4)2]中Fe元素的化合价为价。4. 在完成“实验室用氯酸钾和二氧化锰混合物加热制取氧气”的实验后,小明在老师的指导下回收二氧化锰和氯化钾,实验流程如下图所示。 (1)、操作a的名称是。(2)、在这个反应中二氧化锰的作用是。(3)、请你计算:若制得1.92g氧气,则参加反应的氯酸钾(KClO3)的质量为g。(4)、请你设计实验方案,证明滤渣已洗净。5. 参加社会实践,提升科学素养。(1)、家务劳动。做凉拌皮蛋时,放入适量的食醋,主要目的是除去皮蛋中含有的(填“酸”或“碱”)性物质。餐后利用洗涤剂的作用清洗餐具油污。(2)、疫情防控。佩戴口罩能有效阻挡病毒的传播,其原理类似于化学实验中的操作。测量体温时,水银温度计的汞柱随温度的升高而变长,其微观原因是。(3)、研学实践。走进农田,给果树施化肥,该化肥是一种灰白色粉末,可能属于肥(填“氮”“磷”或“钾”)。步入工厂,用除锈剂(主要成分是稀盐酸)给铁螺钉除锈,反应的化学方程式为。(4)、实践感悟。物质的决定用途,化学在保证人类生存并提高生活质量方面起着重要的作用。6. 海洋封存是实现“碳中和”的途径之一,其原理是利用CO2在水等溶剂中的溶解性来吸收CO2。某小组开展如下探究。(1)、【活动一】探究CO2在水和食盐水(模拟海水)中的溶解情况
(1)、操作a的名称是。(2)、在这个反应中二氧化锰的作用是。(3)、请你计算:若制得1.92g氧气,则参加反应的氯酸钾(KClO3)的质量为g。(4)、请你设计实验方案,证明滤渣已洗净。5. 参加社会实践,提升科学素养。(1)、家务劳动。做凉拌皮蛋时,放入适量的食醋,主要目的是除去皮蛋中含有的(填“酸”或“碱”)性物质。餐后利用洗涤剂的作用清洗餐具油污。(2)、疫情防控。佩戴口罩能有效阻挡病毒的传播,其原理类似于化学实验中的操作。测量体温时,水银温度计的汞柱随温度的升高而变长,其微观原因是。(3)、研学实践。走进农田,给果树施化肥,该化肥是一种灰白色粉末,可能属于肥(填“氮”“磷”或“钾”)。步入工厂,用除锈剂(主要成分是稀盐酸)给铁螺钉除锈,反应的化学方程式为。(4)、实践感悟。物质的决定用途,化学在保证人类生存并提高生活质量方面起着重要的作用。6. 海洋封存是实现“碳中和”的途径之一,其原理是利用CO2在水等溶剂中的溶解性来吸收CO2。某小组开展如下探究。(1)、【活动一】探究CO2在水和食盐水(模拟海水)中的溶解情况
相同条件下,该小组分别用排水法、排食盐水法收集CO2(如图1),待收集100mLCO2后,移出导管,每隔一段时间观察并记录量筒内CO2体积。重复实验,所测数据平均值如下表:
时间/h
0
0.5
6
12
24
48
排水法时CO2体积/mL
100
98.5
85.5
77
66
59
排食盐水法时CO2体积/mL
100
99
93
90.5
89
88
图1发生装置中反应的化学方程式为 , 反应类型是。
(2)、由上表数据分析:①能用排水法收集CO2的理由是。
②相同条件下,等体积水和食盐水吸收CO2更多的是(填“水”或“食盐水”)。
(3)、海洋封存CO2可能带来的危害是(写出1点即可)。(4)、【活动二】探究植物油隔离对CO2在水中溶解情况的影响
小方设计并完成以下对照实验:用两个量筒分别收集100mLCO2倒置于水槽中,向其中一个量筒内注入少量植物油,使CO2与水被植物油隔开(CO2与植物油不反应),测得量筒内CO2体积随时问变化曲线如图2。分析该图可得出的结论是。
(5)、【活动三】深度探究【活动二】中CO2的溶解情况①小松用图3表示无植物油隔离时,量筒内气体中存在的CO2分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图(植物油分子用
 表示)。
表示)。

②为检验有植物油隔离时CO2是否会进入水中,请设计实验方案:。
7. 水是生存之本、文明之源。(1)、天然水中含有不溶性杂质和可溶性杂质等。不溶性杂质可通过的方法除去:区分天然水是硬水还是软水可用 , 生活中可通过的方法降低水的硬度。(2)、电解水实验能证明水是由两种元素组成,反应的化学方程式为 , 该反应的基本类型是反应。8. 根据下列实验图示回答问题。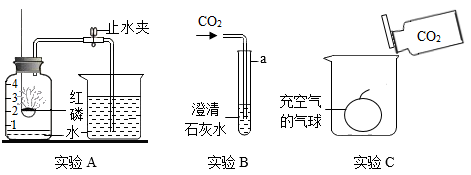 (1)、实验A可测定空气中氧气的含量,(填“能”或“不能”)用木炭代替红磷。(2)、实验B中,仪器a的名称是;澄清石灰水与CO2反应的化学方程式是。(3)、实验C中,观察到气球浮起,说明CO2的密度比空气(填“大”或“小”),因此实验室里常用向排空气法收集CO2。9. 利用工业废液(主要含NaHS以及少量Na2S和Mg、Ca、Fe的化合物)制备重要化工原料硫酸钠的流程图如下。
(1)、实验A可测定空气中氧气的含量,(填“能”或“不能”)用木炭代替红磷。(2)、实验B中,仪器a的名称是;澄清石灰水与CO2反应的化学方程式是。(3)、实验C中,观察到气球浮起,说明CO2的密度比空气(填“大”或“小”),因此实验室里常用向排空气法收集CO2。9. 利用工业废液(主要含NaHS以及少量Na2S和Mg、Ca、Fe的化合物)制备重要化工原料硫酸钠的流程图如下。
已知:Ⅰ、粗品硫酸钠含少量H2SO4、MgSO4、CaSO4、FeSO4等杂质。
Ⅱ、在溶液里,微溶物发生复分解反应可转化为不溶物。
Ⅲ、部分物质的溶解性见表。
部分物质的溶解性表(室温)
阴离子
阳离子
Na+
溶
溶
Ca2+
微溶
不溶
Mg2+
溶
微溶
Fe2+
溶
不溶
(1)、操作①名称是。(2)、“反应器1、2”内均需要进行的操作是。(3)、泥渣的成分有MgCO3、等。(4)、流程中可循环使用的物质是和。(5)、“反应器1”中NaHS发生复分解反应生成H2S气体的化学方程式是。10. 水是生命之源。(1)、对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度最高的是;(2)、下图是电解水的示意图,图中与电池负极相连的试管内收集到的气体是; (3)、生活中我们常用区分硬水和软水;(4)、保护水资源是每个公民应尽的责任和义务,下列防治水体污染的措施正确的有(填序号)。
(3)、生活中我们常用区分硬水和软水;(4)、保护水资源是每个公民应尽的责任和义务,下列防治水体污染的措施正确的有(填序号)。①大量使用含磷洗衣粉 ②农业上禁止使用农药和化肥
③生活污水集中处理达标后再排放 ④工业上应用新技术、新工艺减少污染物的产生
11. 以下是KNO3和NaCl在不同温度时的溶解度和对应的溶解度曲线。请回答:温度/℃
0
10
20
30
40
50
60
溶解度/g
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
(1)、代表KNO3溶解度曲线的是 (填“甲”或“乙”)。(2)、若KNO3中混有少量NaCl,可采用 的方法提纯KNO3。(3)、t1的范围为____(填标号)。A.10~20A、20~30 B、30~40 C、50~60(4)、t2℃时,将等质量的KNO3的饱和溶液和NaCl的饱和溶液分别降温到t1℃,所得溶液中溶质的质量m(KNO3) m(NaCl)(填“>”或“<”或“=”)。 12. 根据下图所示实验回答问题
12. 根据下图所示实验回答问题
 (1)、A实验:探究酸与指示剂的作用,(填“a”或“b”)中的液体变红。(2)、B实验:向盛有水的小烧杯中加入少量品红,静置。一段时间后,观察到烧杯中溶液呈均匀的红色。此现象说明分子。(3)、C实验:I中的蜡烛很快熄灭,Ⅱ中的蜡烛正常燃烧。说明可燃物燃烧的条件之一是。(4)、D实验:量液时,量筒必须放平,视线要与量筒内液体保持水平,再读出液体的体积。13. 日常防疫中蕴含化学知识。(1)、医用外科口罩对空气中的粉尘、飞沫主要起到(填一种化学操作的名称)和吸附的作用。(2)、监测体温使用的测温枪的塑料外壳属于(填“金属材料”或“合成材料”)。(3)、防疫用的“84”消毒液是以次氯酸钠(NaClO)为主要有效成分的消毒液,次氯酸钠中氯元素的化合价为价。(4)、合理膳食可以增强人体的免疫力,下列食物中富含糖类的是____(填字母)。A、馒头 B、牛肉 C、黄瓜14. 中国芯彰显中国“智”造。芯片的基材主要是高纯硅,如图是用粗硅原料(含氧化镁等杂质,不考虑其他杂质与酸反应)制备高纯硅的一种简易流程。
(1)、A实验:探究酸与指示剂的作用,(填“a”或“b”)中的液体变红。(2)、B实验:向盛有水的小烧杯中加入少量品红,静置。一段时间后,观察到烧杯中溶液呈均匀的红色。此现象说明分子。(3)、C实验:I中的蜡烛很快熄灭,Ⅱ中的蜡烛正常燃烧。说明可燃物燃烧的条件之一是。(4)、D实验:量液时,量筒必须放平,视线要与量筒内液体保持水平,再读出液体的体积。13. 日常防疫中蕴含化学知识。(1)、医用外科口罩对空气中的粉尘、飞沫主要起到(填一种化学操作的名称)和吸附的作用。(2)、监测体温使用的测温枪的塑料外壳属于(填“金属材料”或“合成材料”)。(3)、防疫用的“84”消毒液是以次氯酸钠(NaClO)为主要有效成分的消毒液,次氯酸钠中氯元素的化合价为价。(4)、合理膳食可以增强人体的免疫力,下列食物中富含糖类的是____(填字母)。A、馒头 B、牛肉 C、黄瓜14. 中国芯彰显中国“智”造。芯片的基材主要是高纯硅,如图是用粗硅原料(含氧化镁等杂质,不考虑其他杂质与酸反应)制备高纯硅的一种简易流程。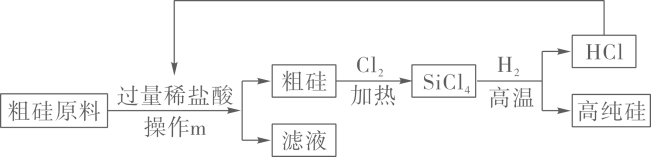 (1)、写出操作m的名称。(2)、写出SiCl4中硅元素的化合价。(3)、上述流程中,可以循环利用的物质是。(填化学式)(4)、滤液中含有的阳离子为。(写离子符号)(5)、写出SiCl4与H2反应的化学方程式。15. 某化学兴趣小组将下图所示的实验搬上了舞台,震撼了师生,展示了化学的魅力。
(1)、写出操作m的名称。(2)、写出SiCl4中硅元素的化合价。(3)、上述流程中,可以循环利用的物质是。(填化学式)(4)、滤液中含有的阳离子为。(写离子符号)(5)、写出SiCl4与H2反应的化学方程式。15. 某化学兴趣小组将下图所示的实验搬上了舞台,震撼了师生,展示了化学的魅力。A.粉尘爆炸实验
 B.空气与呼出气体的比较
B.空气与呼出气体的比较
C.电解水
 D.CO2与NaOH溶液反应
D.CO2与NaOH溶液反应 (1)、A实验说明可燃物与氧气 , 燃烧越剧烈。(2)、B实验可以比较空气与呼出气体中含量的不同。(3)、C实验中电源负极端的玻璃管中生成的气体是。(4)、D实验可用于研究CO2与NaOH溶液的反应。关闭止水夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开止水夹K。即可观察到水倒吸入烧瓶,变为红色,形成美丽喷泉。写出该反应的化学方程式。16. 豆腐是由两千多年前西汉淮南王刘安发明的,它享有“富贵贫困皆厚爱,人人称其菜中王”的美誉。下表是豆腐中主要成分的平均质量分数:
(1)、A实验说明可燃物与氧气 , 燃烧越剧烈。(2)、B实验可以比较空气与呼出气体中含量的不同。(3)、C实验中电源负极端的玻璃管中生成的气体是。(4)、D实验可用于研究CO2与NaOH溶液的反应。关闭止水夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开止水夹K。即可观察到水倒吸入烧瓶,变为红色,形成美丽喷泉。写出该反应的化学方程式。16. 豆腐是由两千多年前西汉淮南王刘安发明的,它享有“富贵贫困皆厚爱,人人称其菜中王”的美誉。下表是豆腐中主要成分的平均质量分数:成分
水
蛋白质
脂肪
糖类
钙
磷
铁
维生素B1
质量分数/%
89.3
4.7
1.3
2.8
0.24
0.064
1.4
0.00006
(1)、用石磨将黄豆磨成豆浆,发生了(填“化学”或“物理”)变化,制作豆腐块的过程涉及豆腐与水分离的环节,该分离操作的名称是。(2)、豆腐含有的营养素中,能为人体提供能量的是(任填一种),含人体所需的微量元素是。(3)、除大豆外,下列也能提供丰富蛋白质的食物是 (填字母)。
A.萝卜 B.鱼 C.大米 D.苹果二、实验探究题
-
17. 下图是实验室制取气体的常用装置,请回答下列问题:
 (1)、写出标号仪器的名称:① , ②。(2)、实验室用高锰酸钾制取氧气,写出该反应的化学方程式: , 可选用的发生装置是(填字母序号)。用F装置收集氧气,停止实验时,应先 , 再熄灭酒精灯。(3)、实验室用锌粒和稀硫酸制取氢气,可选用C装置作为发生装置,该装置的优点是 , 锌粒应该放在。(4)、通常情况下,甲烷是一种无色、无味的气体,密度比空气小,难溶于水。实验室制取甲烷可选用的收集装置是(填字母序号,写一种即可)。18. 实验是科学探究的重要手段。下图是实验室制取气体的常用装置,请回答有关问题:
(1)、写出标号仪器的名称:① , ②。(2)、实验室用高锰酸钾制取氧气,写出该反应的化学方程式: , 可选用的发生装置是(填字母序号)。用F装置收集氧气,停止实验时,应先 , 再熄灭酒精灯。(3)、实验室用锌粒和稀硫酸制取氢气,可选用C装置作为发生装置,该装置的优点是 , 锌粒应该放在。(4)、通常情况下,甲烷是一种无色、无味的气体,密度比空气小,难溶于水。实验室制取甲烷可选用的收集装置是(填字母序号,写一种即可)。18. 实验是科学探究的重要手段。下图是实验室制取气体的常用装置,请回答有关问题: (1)、仪器①的名称。实验室利用高锰酸钾制取氧气的装置中,试管口略向下倾斜的原因是。(2)、实验室里,在常温下用硫化亚铁固体和稀硫酸反应来制取硫化氢气体。通常情况下,硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,密度比空气的大。实验室制取硫化氢气体应选用的发生装置是(填序号),收集装置是(填序号)。19. 下图是实验室制取气体的常用装置。请回答下列问题
(1)、仪器①的名称。实验室利用高锰酸钾制取氧气的装置中,试管口略向下倾斜的原因是。(2)、实验室里,在常温下用硫化亚铁固体和稀硫酸反应来制取硫化氢气体。通常情况下,硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,密度比空气的大。实验室制取硫化氢气体应选用的发生装置是(填序号),收集装置是(填序号)。19. 下图是实验室制取气体的常用装置。请回答下列问题 (1)、写出装置B中仪器①的名称。(2)、实验室用高锰酸钾制取一瓶较纯净的氧气,应选择的装置是(填字母),发生反应的化学方程式是。(3)、实验室制取二氧化碳应选择的收集装置是(填字母),检验二氧化碳已集满的方法是。20. 根据下图所示的实验回答问题:
(1)、写出装置B中仪器①的名称。(2)、实验室用高锰酸钾制取一瓶较纯净的氧气,应选择的装置是(填字母),发生反应的化学方程式是。(3)、实验室制取二氧化碳应选择的收集装置是(填字母),检验二氧化碳已集满的方法是。20. 根据下图所示的实验回答问题: (1)、A实验(填“能”或“不能”)用来测定空气中氧气的含量;(2)、B实验现象说明:空气中的氧气含量比呼出气体中的(“高”或“低”);(3)、C实验中小灯泡发亮,说明石墨具有性;(4)、D实验用来验证质量守恒定律,其中气球的作用是。21. 结合下列实验装置,回答有关问题。
(1)、A实验(填“能”或“不能”)用来测定空气中氧气的含量;(2)、B实验现象说明:空气中的氧气含量比呼出气体中的(“高”或“低”);(3)、C实验中小灯泡发亮,说明石墨具有性;(4)、D实验用来验证质量守恒定律,其中气球的作用是。21. 结合下列实验装置,回答有关问题。 (1)、写出图中对应仪器的名称:a , b。(2)、加热氯酸钾和二氧化锰可制备O2 , 应选择的气体发生装置是(填字母)。(3)、实验室常用锌和稀硫酸反应制取氢气,该反应的化学方程式为 , 若用装置C收集H2 , 气体应从 (填“e”或“f”)端进入。22. 根据如图所示的实验回答问题。
(1)、写出图中对应仪器的名称:a , b。(2)、加热氯酸钾和二氧化锰可制备O2 , 应选择的气体发生装置是(填字母)。(3)、实验室常用锌和稀硫酸反应制取氢气,该反应的化学方程式为 , 若用装置C收集H2 , 气体应从 (填“e”或“f”)端进入。22. 根据如图所示的实验回答问题。
 (1)、甲是粗盐提纯实验中的过滤操作。仪器a的名称是;若过滤后所得溶液仍然浑浊,可能的原因是。(2)、乙是金属化学性质的实验。实验前先用砂纸打磨铝丝的目的是;步骤②中观察到铝丝表面的现象是。设计该实验的依据是。23. 根据下列实验装置图,回答有关问题。
(1)、甲是粗盐提纯实验中的过滤操作。仪器a的名称是;若过滤后所得溶液仍然浑浊,可能的原因是。(2)、乙是金属化学性质的实验。实验前先用砂纸打磨铝丝的目的是;步骤②中观察到铝丝表面的现象是。设计该实验的依据是。23. 根据下列实验装置图,回答有关问题。 (1)、仪器 a的名称。(2)、写出实验室用B制取氧气的化学方程式;若用C装置收集氧气,应将气体从导管口(填“m”或“n”)通入,检验氧气已收集满的操作为。(3)、实验室常用氯化铵固体与熟石灰加热制取氨气,同时生成水和一种盐,写出该反应的化学方程式;选择的发生装置为(填字母),你选择该发生装置的依据是。24. 根据下列装置,回答问题:
(1)、仪器 a的名称。(2)、写出实验室用B制取氧气的化学方程式;若用C装置收集氧气,应将气体从导管口(填“m”或“n”)通入,检验氧气已收集满的操作为。(3)、实验室常用氯化铵固体与熟石灰加热制取氨气,同时生成水和一种盐,写出该反应的化学方程式;选择的发生装置为(填字母),你选择该发生装置的依据是。24. 根据下列装置,回答问题: (1)、写出图中标号①仪器的名称:。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,选择的发生装置是(填字母),反应的化学方程式为。(3)、一氧化氮(NO)是抗菌领域的明星分子。常温下,NO难溶于水且不与水反应。易与O2反应生成NO2气体。实验室收集少量NO,选择的装置是(填字母)。25. 下图是实验室制取气体的部分装置,请根据实验装置回答问题。
(1)、写出图中标号①仪器的名称:。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,选择的发生装置是(填字母),反应的化学方程式为。(3)、一氧化氮(NO)是抗菌领域的明星分子。常温下,NO难溶于水且不与水反应。易与O2反应生成NO2气体。实验室收集少量NO,选择的装置是(填字母)。25. 下图是实验室制取气体的部分装置,请根据实验装置回答问题。 (1)、装置A中仪器a的名称是。(2)、实验室制取氧气和二氧化碳均可选用的发生装置是(填字母序号),用该装置制取氧气的化学方程式为。(3)、若用装置D收集H2 , 气体应从(填“m”或“n”)端通入。26. 具备基本化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了I、Ⅱ两组试题。可供选择的实验药品有大理石、KClO3、MnO2、稀盐酸、NaOH溶液、H2O2溶液、酚酞溶液、石蕊溶液等,相关实验装置如图所示。
(1)、装置A中仪器a的名称是。(2)、实验室制取氧气和二氧化碳均可选用的发生装置是(填字母序号),用该装置制取氧气的化学方程式为。(3)、若用装置D收集H2 , 气体应从(填“m”或“n”)端通入。26. 具备基本化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了I、Ⅱ两组试题。可供选择的实验药品有大理石、KClO3、MnO2、稀盐酸、NaOH溶液、H2O2溶液、酚酞溶液、石蕊溶液等,相关实验装置如图所示。
I组:O2和CO2的实验室制取
(1)、仪器a的名称是。(2)、小明想用同一套装置分别制取O2和CO2 , 应选用发生装置和收集装置(填字母)。其中,制取O2的化学方程式为。(3)、为了鉴别稀盐酸和NaOH溶液,小英要测定溶液的pH,正确的操作是。测得pH=1的溶液为。(4)、稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加溶液,再逐滴加入稀盐酸至过量,观察到溶液由色变为无色。27. 下图是实验室制取气体的常用装置,回答下列问题: (1)、仪器a的名称是。(2)、实验室用氯酸钾和二氧化锰混合制取氧气,应选择的发生装置是(填序号),该反应的化学方程式为。若用装置C收集氧气,刚开始有气泡产生时不宜立即收集,原因是。(3)、若用装置B、D、E组合制取并收集一瓶干燥的二氧化碳,按气流方向,导管口的连接顺序为k→(填导管接口的字母)。28. 下列装置常用于实验室制取气体,请回答问题。
(1)、仪器a的名称是。(2)、实验室用氯酸钾和二氧化锰混合制取氧气,应选择的发生装置是(填序号),该反应的化学方程式为。若用装置C收集氧气,刚开始有气泡产生时不宜立即收集,原因是。(3)、若用装置B、D、E组合制取并收集一瓶干燥的二氧化碳,按气流方向,导管口的连接顺序为k→(填导管接口的字母)。28. 下列装置常用于实验室制取气体,请回答问题。 (1)、仪器a的名称是。(2)、用高锰酸钾并选择A、E装置制取氧气,该反应的化学方程式为。当观察到导管口有时,开始收集。(3)、制取二氧化碳时,应选择的发生装置和收集装置是(填字母)。(4)、实验室里,常用于干燥二氧化碳气体的药品是(填物质名称)。29. 请根据下图回答问题。
(1)、仪器a的名称是。(2)、用高锰酸钾并选择A、E装置制取氧气,该反应的化学方程式为。当观察到导管口有时,开始收集。(3)、制取二氧化碳时,应选择的发生装置和收集装置是(填字母)。(4)、实验室里,常用于干燥二氧化碳气体的药品是(填物质名称)。29. 请根据下图回答问题。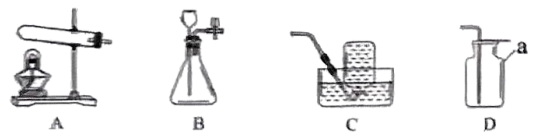 (1)、仪器a的名称为。(2)、实验室制取二氧化碳,应选择的发生装置是。(3)、用高锰酸钾制取氧气的化学方程式为。(4)、用C装置收集O2时,集满氧气的标志是。30. 请根据下列各图中的有关信息,回答下列问题。
(1)、仪器a的名称为。(2)、实验室制取二氧化碳,应选择的发生装置是。(3)、用高锰酸钾制取氧气的化学方程式为。(4)、用C装置收集O2时,集满氧气的标志是。30. 请根据下列各图中的有关信息,回答下列问题。 (1)、实验室用 B 装置制氧气,化学方程式是。实验室用装置 A 制取氧气时发生反应的化学方程式为 , 若要收集到较纯净的氧气,应选用的收集装置是(填字母),收集满的标志是。(2)、实验室制取二氧化碳的化学方程式为是 , 若用 G 装置收集 CO2气体,气体从(填“c”“d”)端进入。(3)、若用 C 装置制取 CO2气体,该装置的优点是。关闭开关后,C 中多孔隔板处依次观察到的现象是(用字母 efg 催如图进行排序)
(1)、实验室用 B 装置制氧气,化学方程式是。实验室用装置 A 制取氧气时发生反应的化学方程式为 , 若要收集到较纯净的氧气,应选用的收集装置是(填字母),收集满的标志是。(2)、实验室制取二氧化碳的化学方程式为是 , 若用 G 装置收集 CO2气体,气体从(填“c”“d”)端进入。(3)、若用 C 装置制取 CO2气体,该装置的优点是。关闭开关后,C 中多孔隔板处依次观察到的现象是(用字母 efg 催如图进行排序) 31. 结合下列实验室常用仪器回答问题:
31. 结合下列实验室常用仪器回答问题: (1)、取少量液体试剂时需要的仪器是(写名称)。(2)、需要垫石棉网加热的仪器是(写名称)。(3)、给少量液体加热需要用到的仪器有(填序号)。(4)、用①量取 10mL 液体时俯视读数,则实际所取的液体体积(填“大于”、“小于”或“等于”)10mL。(5)、将少量氯化钠溶解在水中,用③(写名称)搅拌的目的是。32. 如图是实验室制取气体的常用实验装置,请按要求回答问题。
(1)、取少量液体试剂时需要的仪器是(写名称)。(2)、需要垫石棉网加热的仪器是(写名称)。(3)、给少量液体加热需要用到的仪器有(填序号)。(4)、用①量取 10mL 液体时俯视读数,则实际所取的液体体积(填“大于”、“小于”或“等于”)10mL。(5)、将少量氯化钠溶解在水中,用③(写名称)搅拌的目的是。32. 如图是实验室制取气体的常用实验装置,请按要求回答问题。 (1)、仪器a的名称是。(2)、B装置中试管口略微向下倾斜的原因是;实验室用A装置制取氧气的化学方程式是。(3)、下列气体既能用C装置收集又能用D装置收集的是。(填序号)
(1)、仪器a的名称是。(2)、B装置中试管口略微向下倾斜的原因是;实验室用A装置制取氧气的化学方程式是。(3)、下列气体既能用C装置收集又能用D装置收集的是。(填序号)①H2 ②O2 ③CO2
33. 球形干燥管在填充了干燥剂后可以对气体进行干燥。请根据下列两个实验回答相关问题: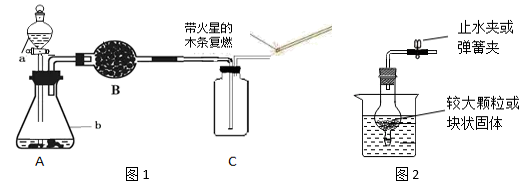 (1)、实验(Ⅰ)(图1)
(1)、实验(Ⅰ)(图1)①球形干燥管内应填充。
A.浓硫酸 B.碱石灰固体
②装置b的名称是。
③使用装置C收集气体的方法是法。
(2)、实验(Ⅱ)(图2)①实验室不能利用图2组合制取的气体是
A.H2 B.O2 C.CO2
②图2组合装置的优点是。
34. 实验案可选用如图所示装置制取气体。 (1)、写出利用A制取O2的化学方程式。(2)、若利用B制取CO2 , 请将开始时所加的药品分别填写在图中相应的虚线框内。(3)、若利用C收集到一瓶无色无味的气体,猜想一种气体并用简单方法加以验证。35. 铁黄(FeOOH)是重要的化工产品。某科研小组在实验室进行铁黄制备研究。
(1)、写出利用A制取O2的化学方程式。(2)、若利用B制取CO2 , 请将开始时所加的药品分别填写在图中相应的虚线框内。(3)、若利用C收集到一瓶无色无味的气体,猜想一种气体并用简单方法加以验证。35. 铁黄(FeOOH)是重要的化工产品。某科研小组在实验室进行铁黄制备研究。已知:①铁黄制备原理
②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)、FeOOH可表示为xFe2O3·yH2O,其中=。(2)、铁皮处理:取一定量铁皮,用稀硫酸除去表面铁锈。该除锈反应的化学方程式为。(3)、制备铁黄:在如图所示装置的三颈烧瓶内进行制备。
步骤一:加入一定量除锈后的碎铁皮
步骤二:加入含有少量铁黄晶种的悬浊液;
步骤三:滴加少量FeSO4溶液;
步骤四:控制合适条件,边搅拌边鼓入空气,充分反应48小时,得到大量FeOOH沉淀。
①将三颈烧瓶中所得FeOOH沉淀分离出来的实验操作是(填操作名称)。
②为提高产品纯度,需洗涤分离出的沉淀。洗涤前沉淀表面吸附的阴离子为(填离子符号)。
③实验中仅滴加少量FeSO4溶液,就能得到大量FeOOH沉淀,其原因是。
36. 下图是初中化学中常用的实验装置,请回答下列问题。 (1)、写出A装置中仪器①的名称。(2)、若用高锰酸钾制取一瓶纯净的氧气,应选择的发生装置是 , 收集装置是 , 该反应的化学方程式是;用制得的氧气做铁丝燃烧的实验,集气瓶中要留少量水的原因是。(3)、实验室制取CO2 , 应选择的发生装置是 , 收集装置是 , 检验CO2是否收集满的操作是。(4)、将收集到的CO2通入澄清石灰水中,石灰水变浑浊,该反应的化学方程式是。37. 化学是一门以实为基础的科学。结合下图回答问题。
(1)、写出A装置中仪器①的名称。(2)、若用高锰酸钾制取一瓶纯净的氧气,应选择的发生装置是 , 收集装置是 , 该反应的化学方程式是;用制得的氧气做铁丝燃烧的实验,集气瓶中要留少量水的原因是。(3)、实验室制取CO2 , 应选择的发生装置是 , 收集装置是 , 检验CO2是否收集满的操作是。(4)、将收集到的CO2通入澄清石灰水中,石灰水变浑浊,该反应的化学方程式是。37. 化学是一门以实为基础的科学。结合下图回答问题。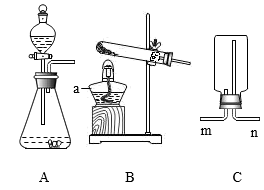 (1)、仪器a的名称为。(2)、实验室用高锰酸钾制取O2 , 选择的发生装置为(填标号),反应的化学方程式为。(3)、实验室制取CO2的化学方程式为。将产生的气体通入澄清石灰水,可用于检验CO2 , 反应的化学方程式为。(4)、某气体的相对分子质量为46,常温下不与空气成分反应。若用C装置收集时,气体应从(填标号)端通入。38. 制取气体是初中化学实验的重要内容,根据要求回答下列问题:
(1)、仪器a的名称为。(2)、实验室用高锰酸钾制取O2 , 选择的发生装置为(填标号),反应的化学方程式为。(3)、实验室制取CO2的化学方程式为。将产生的气体通入澄清石灰水,可用于检验CO2 , 反应的化学方程式为。(4)、某气体的相对分子质量为46,常温下不与空气成分反应。若用C装置收集时,气体应从(填标号)端通入。38. 制取气体是初中化学实验的重要内容,根据要求回答下列问题: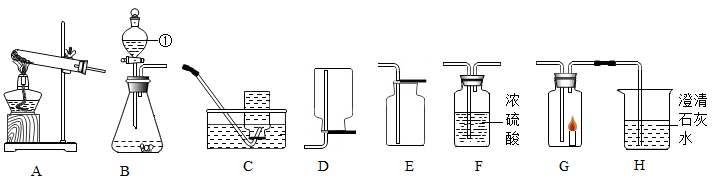 (1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号,下同)。(3)、若要得到干燥的氧气,所选择装置的连接顺序为:B→→。(4)、某气体只能用C装置收集,则该气体可能具有的性质为。
(1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号,下同)。(3)、若要得到干燥的氧气,所选择装置的连接顺序为:B→→。(4)、某气体只能用C装置收集,则该气体可能具有的性质为。a.能与水反应 b.能与空气中的某些成分发生反应 c.密度与空气接近
(5)、某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中反应的化学方程式为。39. 根据下图实验装置,回答问题: (1)、C装置中标有①的仪器名称为。(2)、实验室某小组同学用过氧化氢溶液和二氧化锰制取氧气,请写出化学方程式。根据该反应原理,从控制反应速率的角度考虑,请从上图中选择发生装置和收集装置制取一瓶干燥的氧气,所选装置接口字母连接顺序为(连接顺序全对才得分)。
(1)、C装置中标有①的仪器名称为。(2)、实验室某小组同学用过氧化氢溶液和二氧化锰制取氧气,请写出化学方程式。根据该反应原理,从控制反应速率的角度考虑,请从上图中选择发生装置和收集装置制取一瓶干燥的氧气,所选装置接口字母连接顺序为(连接顺序全对才得分)。