辽宁省锦州市2021-2022学年高二下学期期末考试化学试卷
试卷更新日期:2022-08-08 类型:期末考试
一、单选题
-
1. 下列物质不能用于杀菌消毒的是( )A、乙醇 B、苯酚 C、甲醛 D、乙酸乙酯2. 高分子材料在各个领域都有重要的作用,下列有关说法错误的是( )A、用于生产食品包装袋薄膜的材料属于低密度聚乙烯 B、用于制造轮胎的顺丁橡胶是异戊二烯的聚合物 C、聚乙炔可作为导电高分子材料用在移动电子设备中 D、以醋酸纤维为材料的高分子分离膜广泛用于海水淡化和饮用水的制取3. 下列化合物中,能发生酯化、加成、消去三种反应的是( )A、
 B、CH3-CH=CH-COOH
C、
B、CH3-CH=CH-COOH
C、 D、
D、 4. 下列关于有机化合物的说法错误的是( )A、葡萄糖、果糖、核糖和脱氧核糖都是不能水解的单糖 B、油脂在碱性溶液中水解,生成甘油和高级脂肪酸盐 C、向蛋白质溶液中加入浓硝酸,溶液产生白色沉淀,蛋白质发生了盐析 D、DNA分子的多聚核苷酸链中,核苷酸之间通过磷酯键连接5. 下列关于环状有机物的说法正确的是( )A、
4. 下列关于有机化合物的说法错误的是( )A、葡萄糖、果糖、核糖和脱氧核糖都是不能水解的单糖 B、油脂在碱性溶液中水解,生成甘油和高级脂肪酸盐 C、向蛋白质溶液中加入浓硝酸,溶液产生白色沉淀,蛋白质发生了盐析 D、DNA分子的多聚核苷酸链中,核苷酸之间通过磷酯键连接5. 下列关于环状有机物的说法正确的是( )A、 和
和 都属于芳香烃
B、
都属于芳香烃
B、 和
和 的一氯代物均有4种(不考虑立体异构)
C、
的一氯代物均有4种(不考虑立体异构)
C、 与
与 互为同系物
D、
互为同系物
D、 与
与 互为同分异构体
6. 下列实验装置能达到对应实验目的的是( )
互为同分异构体
6. 下列实验装置能达到对应实验目的的是( ) A、装置甲验证乙醇脱水生成乙烯 B、装置乙验证乙炔可使溴水褪色 C、装置丙制备硝基苯 D、装置丁制备乙酸乙酯7. 有机小分子X通过选择性催化聚合可分别得到聚合物Y、Z。
A、装置甲验证乙醇脱水生成乙烯 B、装置乙验证乙炔可使溴水褪色 C、装置丙制备硝基苯 D、装置丁制备乙酸乙酯7. 有机小分子X通过选择性催化聚合可分别得到聚合物Y、Z。
下列说法错误的是( )
A、X的结构简式是 B、Y中含有酯基,Z中不含有酯基
C、Y和Z的链节中C、H、O的原子个数比相同
D、Y和Z分别通过化学反应均可形成空间网状结构
8. 下列有关物质结构与性质的叙述正确的是( )A、等离子体是只由离子组成的具有带电性的气态物质 B、1molCo3+的八面体配合物[CoClx(NH3)y]Clz与足量AgNO3溶液作用生成2molAgCl沉淀,则x、y、z的值分别为2、4、2 C、若MgO的化学键中离子键的百分数为50%,则MgO可看作离子晶体与共价晶体之间的过渡晶体 D、利用超分子的自组装特征,可以分离C60和C709. 以环戊烷为原料制备环戊二烯的合成路线如下,下列说法错误的是( )
B、Y中含有酯基,Z中不含有酯基
C、Y和Z的链节中C、H、O的原子个数比相同
D、Y和Z分别通过化学反应均可形成空间网状结构
8. 下列有关物质结构与性质的叙述正确的是( )A、等离子体是只由离子组成的具有带电性的气态物质 B、1molCo3+的八面体配合物[CoClx(NH3)y]Clz与足量AgNO3溶液作用生成2molAgCl沉淀,则x、y、z的值分别为2、4、2 C、若MgO的化学键中离子键的百分数为50%,则MgO可看作离子晶体与共价晶体之间的过渡晶体 D、利用超分子的自组装特征,可以分离C60和C709. 以环戊烷为原料制备环戊二烯的合成路线如下,下列说法错误的是( ) A、X的结构简式为
A、X的结构简式为 B、反应④的反应试剂和反应条件是浓硫酸、加热
C、环戊二烯分子中所有碳原子一定在同一平面内
D、环戊二烯与Br以物质的量之比为1:1反应,可生成
B、反应④的反应试剂和反应条件是浓硫酸、加热
C、环戊二烯分子中所有碳原子一定在同一平面内
D、环戊二烯与Br以物质的量之比为1:1反应,可生成 10. 为实现下列各项中的实验目的,对应的实验操作及现象正确的是( )
10. 为实现下列各项中的实验目的,对应的实验操作及现象正确的是( )选项
实验目的
实验操作及现象
A
鉴别乙醇和甲苯
取少量两种试剂,分别加入蒸馏水,其中与水互溶不分层的为乙醇,分层的为甲苯
B
证明丙烯醛(CH2=CHCHO)中含有碳碳双键
取少量内烯醛,滴加溴水,若溴水褪色,证明含有碳碳双键
C
检验甲酸中混有乙醛
取少量试剂,加入氢氧化钠溶液中和甲酸后,加入新制的氢氧化铜,加热,生成砖红色沉淀,说明混有乙醛
D
除去苯中混有的少量苯酚
向混合物中滴加饱和溴水,过滤后弃去沉淀
A、A B、B C、C D、D11. 葡酚酮是由葡萄籽提取的一种花青素类衍生物,具有良好的抗氧化活性,结构简式如图所示。下列关于葡酚酮的叙述错误的是( ) A、露置在空气中,容易发生变质 B、分子内的碳原子存在sp2、sp3两种杂化轨道类型 C、可使酸性KMnO4溶液褪色 D、1mol葡酚酮与足量NaOH溶液反应,最多消耗5molNaOH12. 实验室用苯甲酸和乙醇在浓硫酸催化下制备苯甲酸乙酯的流程如下图所示。已知:①苯甲酸乙酯为无色液体,沸点为212℃,微溶于水,易溶于乙醚。②乙醚的密度为0.834g/cm3 , 沸点为34.5℃。下列说法错误的是( )
A、露置在空气中,容易发生变质 B、分子内的碳原子存在sp2、sp3两种杂化轨道类型 C、可使酸性KMnO4溶液褪色 D、1mol葡酚酮与足量NaOH溶液反应,最多消耗5molNaOH12. 实验室用苯甲酸和乙醇在浓硫酸催化下制备苯甲酸乙酯的流程如下图所示。已知:①苯甲酸乙酯为无色液体,沸点为212℃,微溶于水,易溶于乙醚。②乙醚的密度为0.834g/cm3 , 沸点为34.5℃。下列说法错误的是( ) A、不断分离除去反应生成的水,可以提高苯甲酸乙酯的产率 B、冷水和Na2CO3溶液洗涤的目的是除去浓硫酸和未反应的苯甲酸 C、用乙醚萃取苯甲酸乙酯时,有机相位于分液漏斗的下层 D、蒸馏除去乙醛时,需水浴加热,实验台附近严禁火源13. 根据各物质的结构模型示意图,判断下列说法正确的是( )
A、不断分离除去反应生成的水,可以提高苯甲酸乙酯的产率 B、冷水和Na2CO3溶液洗涤的目的是除去浓硫酸和未反应的苯甲酸 C、用乙醚萃取苯甲酸乙酯时,有机相位于分液漏斗的下层 D、蒸馏除去乙醛时,需水浴加热,实验台附近严禁火源13. 根据各物质的结构模型示意图,判断下列说法正确的是( )名称
Mg-Al合金晶胞
SF6分子结构
Na2O晶胞
干冰晶胞
结构模型示意图



 A、Mg-Al合金晶体的化学式可表示为MgAl2 B、SF6分子中各原子均达到8电子稳定结构 C、Na2O晶体中与某个阴离子紧邻的所有阳离子为顶点构成的几何体为立方体 D、干冰升华过程中破坏了共价键14. 2022年4月16日,神舟十三号返回舱成功着陆,降落伞采用芳纶纤维材料,结构片段如图。下列说法正确的是( )
A、Mg-Al合金晶体的化学式可表示为MgAl2 B、SF6分子中各原子均达到8电子稳定结构 C、Na2O晶体中与某个阴离子紧邻的所有阳离子为顶点构成的几何体为立方体 D、干冰升华过程中破坏了共价键14. 2022年4月16日,神舟十三号返回舱成功着陆,降落伞采用芳纶纤维材料,结构片段如图。下列说法正确的是( ) A、芳纶纤维与羊毛的主要化学成分相同 B、芳纶纤维完全水解产物的单个分子中,含有官能团-COOH或-NH2 C、芳纶纤维中存在氢键,氢键对该高分子的性能没有影响 D、芳纶纤维的结构简式可表示为
A、芳纶纤维与羊毛的主要化学成分相同 B、芳纶纤维完全水解产物的单个分子中,含有官能团-COOH或-NH2 C、芳纶纤维中存在氢键,氢键对该高分子的性能没有影响 D、芳纶纤维的结构简式可表示为 15. 某课题组设计一种以催化剂辅助有机物A固定CO2的方法,原理如图。下列说法错误的是( )
15. 某课题组设计一种以催化剂辅助有机物A固定CO2的方法,原理如图。下列说法错误的是( ) A、有机物A为CH3OH B、若用HOCH2CH2OH代替有机物A固定CO2 , 产物可能为
A、有机物A为CH3OH B、若用HOCH2CH2OH代替有机物A固定CO2 , 产物可能为 C、②的反应类型为加成反应
D、反应物原料中的原子100%转化为产物
C、②的反应类型为加成反应
D、反应物原料中的原子100%转化为产物
二、非选择题
-
16. 材料是人类赖以生存和发展的重要物质基础。请回答下列问题;(1)、下列金属材料的性质能用电子气理论解释的是____(填序号)A、易腐蚀 B、易导电 C、易导热 D、有延展性(2)、工业上采用氰化法提炼金的同时生成[Zn(CN)4]2- , [Zn(CN)4]2-中配位原子是C,[Zn(CN)4]2-的结构式为;其中含有的σ键与π键的数目之比为。(3)、立方氮化硼是一种超硬、耐磨、耐高温的新型材料,在机械加工行业有着广泛的应用,结构与金刚石相似,晶胞如图所示。
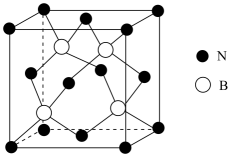
①立方氮化硼熔点比金刚石低,原因是。
②一个N原子周围紧邻的N原子有个。
③晶体中含有配位键,提供空轨道的原子是原子。
④若晶胞参数为α nm,设阿伏加德罗常数的值为NA , 则晶体的密度为g/cm3(用含α、NA的表达式表示)。
17. 有机物为解决人类面临的资源、能源、环境和健康等问题起到了重要的作用。请回答下列问题:(1)、线型结构酚醛树脂的结构简式为。(2)、 的系统命名法的名称为。 (3)、写出丙醛与银氨溶液发生银镜反应的化学方程式。(4)、0.1mol某链状经与0.2molHCl完全加成,生成的氯代烷最多还可以与0.6mol氯气反应,则该经的结构简式为。(5)、某有机化合物X经李比希法测得其中碳的质量分数为72.0%,氢的质量分数为6.67%,其余为氧元素,用质谱法分析得知X的相对分子质量为150.根据下列信息确定X的分子结构:图甲为X的核磁共振氢谱,5组峰的面积之比为1:2:2:2:3;图乙为X的红外光谱:X分子苯环上只有一个取代基,且含有两种官能团。
的系统命名法的名称为。 (3)、写出丙醛与银氨溶液发生银镜反应的化学方程式。(4)、0.1mol某链状经与0.2molHCl完全加成,生成的氯代烷最多还可以与0.6mol氯气反应,则该经的结构简式为。(5)、某有机化合物X经李比希法测得其中碳的质量分数为72.0%,氢的质量分数为6.67%,其余为氧元素,用质谱法分析得知X的相对分子质量为150.根据下列信息确定X的分子结构:图甲为X的核磁共振氢谱,5组峰的面积之比为1:2:2:2:3;图乙为X的红外光谱:X分子苯环上只有一个取代基,且含有两种官能团。
①X的分子式为。
②X中含有官能团的名称为。
③1molX与足量氢气完全反应消耗氢气的物质的量为mol。
18. 苯是重要的化工原料,可用来合成A和有机高分子材料N,一种制取A和N的流程如下图所示。
已知:

请回答下列问题
(1)、反应I的催化剂为(写化学式)。(2)、试剂C可以选用(填序号)。a.CH3COONa溶液b.NaOH溶液c.NaHCO3溶液d.Na2CO3溶液
(3)、写出B的结构简式,并用星号(*)标出其中的手性碳原子。(4)、反应II的反应类型为。(5)、反应Ⅲ的化学方程式为。(6)、符合下列条件的B的同分异构体有种(填序号,不考虑立体异构)。a.遇FeCl3溶液显紫色b.属于酯类c.苯环上有两个取代基
其中核磁共振氢谱有6组峰,且峰面积之比为1:1:2:2:2:2的同分异构体的结构简式为。
19. 联苄( )是常用的有机合成中间体,实验室可用苯和1,2-二氯乙烷为原料,在无水AlCl3催化下加热制得联苄。
)是常用的有机合成中间体,实验室可用苯和1,2-二氯乙烷为原料,在无水AlCl3催化下加热制得联苄。反应原理为:

查阅资料已知:
物质
相对分子质量
密度/(g·cm3)
熔点/℃
沸点/℃
溶解性

78
0.88
5.5
80.1
难溶于水
ClCH2CH2Cl
99
1.3
-35.5
83.5
难溶于水,可溶于苯
无水AlCl3
133.5
2.4
190
178
遇水水解,微溶于苯
联苄
182
1.0
52
284
难溶于水,易溶于苯
实验装置如图所示(加热和夹持仪器省略)

实验步骤:
①三颈烧瓶中加入100mL苯(过量)和适量无水AlCl3 , 再通过仪器a向三颈烧瓶中滴加10mL1,2-二氯乙烷。
②控制温度为60~65℃,反应约60min。
③将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和水洗涤分离,在所得产物中加入少量无水MgSO4固体,静置、过滤,先常压蒸馏,再减压蒸馏得到联苄18.2g。
请回答下列问题:
(1)、仪器a的名称为。(2)、球形干燥管中盛装无水CaCl2的作用是。(3)、步骤②中加热方式为。(4)、通过观察反应过程中溶液b中的现象变化,可以验证该反应的反应类型,则溶液b可以选用的试剂为。(填序号)A.水 B.石蕊溶液 C.硝酸银溶液 D.氢氧化钠溶液(5)、步骤③中加入无水MgSO4固体的作用是。(6)、常压蒸馏除杂时,最低温度应控制在℃。(7)、该实验的产率约为%(保留到小数点后一位)。