广东省清远市2021-2022学年高二下学期期末考试化学试题
试卷更新日期:2022-08-08 类型:期末考试
一、单选题
-
1. 化学的发展经历了漫长的历程。下列关于化学发展过程中的成就错误的是( )A、瑞典化学家贝采里乌斯是有机化学概念的提出者 B、丹麦科学家玻尔发现了元素周期律 C、德国化学家维勒首次在实验室利用合成 , 打破了无机物与有机物之间的界限 D、1965年,中国科学家首次人工合成结晶牛胰岛素2. 在北京冬奥会上,我国使用了多项高科技。下列所使用的材料不属于有机高分子材料的是( )A、火炬“飞扬”使用的高性能树脂 B、御寒服面料使用的新疆长绒棉和驼绒 C、滑雪防护镜使用的聚甲基丙烯酸甲酯 D、颁奖礼仪服饰“瑞雪祥云”使用的保温材料石墨烯3. 下列化学用语中正确的是( )A、甲烷的球棍模型为
 B、羟基的电子式为
B、羟基的电子式为 C、
C、 的系统名称为1,3-二丁烯
D、乙烷的结构式为
4. 下列说法中,正确的是( )A、不同能层的s轨道大小、形状都相同 B、最外层电子数为2的元素一定位于s区 C、电离能越大的元素,电负性也越大 D、碳原子的能量:激发态>基态5. 我国科学家开发出新型高选择性的复合催化剂,能够实现和反应脱去和 , 一步生成。下列说法正确的是( )A、为手性分子 B、能发生消去反应 C、等物质的量的、中含有的孤电子对数相等 D、高选择性的复合催化剂能提高该反应中反应物的平衡转化率6. 下列关于晶体的说法中正确的是( )A、自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体 B、晶胞中任何一个粒子都属于该晶胞 C、玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体 D、缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性7. 黄豆黄素具有诱发细胞程序性死亡、提高抗癌药效等作用,其分子结构如图所示,下列说法错误的是( )
的系统名称为1,3-二丁烯
D、乙烷的结构式为
4. 下列说法中,正确的是( )A、不同能层的s轨道大小、形状都相同 B、最外层电子数为2的元素一定位于s区 C、电离能越大的元素,电负性也越大 D、碳原子的能量:激发态>基态5. 我国科学家开发出新型高选择性的复合催化剂,能够实现和反应脱去和 , 一步生成。下列说法正确的是( )A、为手性分子 B、能发生消去反应 C、等物质的量的、中含有的孤电子对数相等 D、高选择性的复合催化剂能提高该反应中反应物的平衡转化率6. 下列关于晶体的说法中正确的是( )A、自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体 B、晶胞中任何一个粒子都属于该晶胞 C、玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体 D、缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性7. 黄豆黄素具有诱发细胞程序性死亡、提高抗癌药效等作用,其分子结构如图所示,下列说法错误的是( ) A、该物质的分子式为 B、该分子结构中含有4种官能团 C、该物质能在空气中稳定存在 D、该物质能与溶液发生显色反应8. 用下列实验装置进行的实验,能达到相应实验目的的是( )
A、该物质的分子式为 B、该分子结构中含有4种官能团 C、该物质能在空气中稳定存在 D、该物质能与溶液发生显色反应8. 用下列实验装置进行的实验,能达到相应实验目的的是( )A.制取并检验生成的乙烯
B.制取并检验生成的乙炔
C.分离乙醇和丙酮
D.比较酸性:醋酸>碳酸>苯酚



 A、A B、B C、C D、D9. HC3N是一种星际分子,分子内不含环状结构,下列有关这种星际分子的说法错误的是( )A、HC3N的结构可能为H-C≡C-C≡N B、HC3N为极性分子 C、HC3N中所含有的σ键与π键数目比为1:1 D、HC3N分子中所有原子不可能都在一条直线上10. 下列物质中一氯取代物种类最多的是( )A、
A、A B、B C、C D、D9. HC3N是一种星际分子,分子内不含环状结构,下列有关这种星际分子的说法错误的是( )A、HC3N的结构可能为H-C≡C-C≡N B、HC3N为极性分子 C、HC3N中所含有的σ键与π键数目比为1:1 D、HC3N分子中所有原子不可能都在一条直线上10. 下列物质中一氯取代物种类最多的是( )A、 B、
B、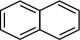 C、
C、 D、
D、 11. 设为阿伏加德罗常数的值。下列说法正确的是( )A、60g中含有C—H键的数目为4 B、1mol晶体中含有离子的数目为3 C、标准状况下,22.4LHF中含有的分子数目为 D、1mol基态Mg原子中s轨道上的电子总数为612. K3[Fe(CN)6]俗称赤血盐、赤血盐钾,化学上常用于检验亚铁离子。下列关于K3[Fe(CN)6]的说法错误的是( )A、该化合物中的Fe为+3价 B、1molK3[Fe(CN)6]中含有的σ键数目为6NA C、配体是CN- , 配位数为6 D、铁离子提供空轨道13. 下列化学方程式书写错误的是( )A、 B、 C、 D、14. X、Y、Z、R、W是原子序数依次增大的短周期主族元素,这五种元素可形成结构如图所示的物质,该物质中所有原子均满足稳定结构,W元素的原子半径在短周期主族中最大,基态Y原子的s能级上的电子数是p能级上的2倍,下列说法正确的是( )
11. 设为阿伏加德罗常数的值。下列说法正确的是( )A、60g中含有C—H键的数目为4 B、1mol晶体中含有离子的数目为3 C、标准状况下,22.4LHF中含有的分子数目为 D、1mol基态Mg原子中s轨道上的电子总数为612. K3[Fe(CN)6]俗称赤血盐、赤血盐钾,化学上常用于检验亚铁离子。下列关于K3[Fe(CN)6]的说法错误的是( )A、该化合物中的Fe为+3价 B、1molK3[Fe(CN)6]中含有的σ键数目为6NA C、配体是CN- , 配位数为6 D、铁离子提供空轨道13. 下列化学方程式书写错误的是( )A、 B、 C、 D、14. X、Y、Z、R、W是原子序数依次增大的短周期主族元素,这五种元素可形成结构如图所示的物质,该物质中所有原子均满足稳定结构,W元素的原子半径在短周期主族中最大,基态Y原子的s能级上的电子数是p能级上的2倍,下列说法正确的是( ) A、X可能位于元素周期表的p区 B、最高价氧化物对应水化物的酸性:Z>Y C、第一电离能:R>Z>Y D、R和W不能形成含有共价键的化合物15. a、b、c分别代表金属晶体中三种常见的立方晶胞结构(如图),则晶胞a、b、c中离顶点的金属原子最近且距离相等的金属原子的个数比为( )
A、X可能位于元素周期表的p区 B、最高价氧化物对应水化物的酸性:Z>Y C、第一电离能:R>Z>Y D、R和W不能形成含有共价键的化合物15. a、b、c分别代表金属晶体中三种常见的立方晶胞结构(如图),则晶胞a、b、c中离顶点的金属原子最近且距离相等的金属原子的个数比为( ) A、1:1:2 B、8:6:4 C、2:4: 3 D、4:3:616. 生姜又名百辣云,其中的辣味物质统称为“姜辣素”,生姜中的风味成分及相互转化图如图,下列说法错误的是( )
A、1:1:2 B、8:6:4 C、2:4: 3 D、4:3:616. 生姜又名百辣云,其中的辣味物质统称为“姜辣素”,生姜中的风味成分及相互转化图如图,下列说法错误的是( ) A、三种有机物都能与NaOH溶液发生反应 B、姜醇类能发生催化氧化反应生成姜酮的同系物 C、1mol姜烯酚类最多可以和5molH2发生加成反应 D、相同物质的量的上述三种有机物分别与足量溴水反应时、姜烯酚类消耗的Br2最多
A、三种有机物都能与NaOH溶液发生反应 B、姜醇类能发生催化氧化反应生成姜酮的同系物 C、1mol姜烯酚类最多可以和5molH2发生加成反应 D、相同物质的量的上述三种有机物分别与足量溴水反应时、姜烯酚类消耗的Br2最多二、综合题
-
17. 我国科学家及其合作团队研究发现,六方相(hep)Fe—H、Fe—C和Fe—O合金在地球内核温压下转变成超离子态。该研究表明地球内核并非传统认知的固态,而是由固态铁和流动的轻元素组成的超离子态。请用所学知识回答下列问题:(1)、基态铁原子最外层电子所在能级的电子云轮廓图为形。(2)、H、C、O三种元素的电负性由大到小的排序为(填元素符号)。(3)、锰和铁处于同一周期,锰、铁电离能数据如表所示:
元素
Mn
717.3
1509.9
3248
Fe
762.5
1561.9
2953
请解释的主要原因:。
(4)、H、C、O三种元素可以组成很多种物质。①、、、、中属于非极性分子的有(填化学式)。
②
 的沸点(填“大于”、“小于”或“等于”)
的沸点(填“大于”、“小于”或“等于”)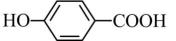 的沸点。(5)、用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。
的沸点。(5)、用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。
①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为。
②若图2中晶胞参数为apm,则该晶胞的空间利用率()为(用含π的式子表示)%。
18. 苯酚是生产某些树脂、染料、防腐剂以及药物的重要化工原料。实验室常用氯化铁溶液检验苯酚(或酚类)。某小组为研究外界条件的改变对苯酚显色反应的影响而进行下列实验。(1)、 (一)制备无水氯化铁
已知:FeCl3易潮解,100℃左右时升华。请利用下列装置制备无水FeCl3并回答下列问题。
装置C中发生反应的化学方程式为。
(2)、实验室制备无水氯化铁时,导管连接顺序为为e→ →c→d→ → → → →h。(填字母)(3)、(二)探究外界条件的改变对苯酚显色反应的影响已知:I.苯酚显色反应的原理为。
II.苯酚易溶于苯,难溶于石油醚。石油醚无色且密度小于水。
探究有机溶剂对氯化铁的苯酚紫色混合液的影响,相关实验记录如下:
序号
一定浓度的苯酚水溶液的体积/mL
溶液
加入物质
实验现象
①
x
2滴
无
溶液呈深紫色
②
2
2滴
1mL
溶液呈紫色
③
2
2滴
1mL苯
溶液分层,上层为无色,下层为浅紫色
④
2
2滴
1mL石油醚
x值为 , 结合上述实验,预测实验④中的现象为。
(4)、对比实验①②的现象,颜色变化的原因为;对比实验③④的现象,颜色变化的原因为。(5)、若想探究pH对显色反应的影响,不可加入(填“稀盐酸”、“稀硫酸”或“硝酸”)进行调节。19. 已知物质I有如图所示的转化关系,请根据所学知识回答下列问题: (1)、物质I的名称为。(2)、0.1mol物质I完全燃烧,消耗标准状况下的L。(3)、写出物质II在加热条件下与足量NaOH的乙醇溶液发生反应的化学方程式:。(4)、物质IV的结构中有3个环,则物质Ⅳ的结构简式为。(5)、若物质VI是III的同分异构体,则能与溶液反应生成气体的VI的结构有种,其中核磁共振氢谱有3组峰,且峰面积之比为9:2:1的结构简式为。(6)、写出生成V的化学方程式:。20. 治疗血栓的药物阿派沙班(VII)的合成路线如图所示,请回答下列问题:
(1)、物质I的名称为。(2)、0.1mol物质I完全燃烧,消耗标准状况下的L。(3)、写出物质II在加热条件下与足量NaOH的乙醇溶液发生反应的化学方程式:。(4)、物质IV的结构中有3个环,则物质Ⅳ的结构简式为。(5)、若物质VI是III的同分异构体,则能与溶液反应生成气体的VI的结构有种,其中核磁共振氢谱有3组峰,且峰面积之比为9:2:1的结构简式为。(6)、写出生成V的化学方程式:。20. 治疗血栓的药物阿派沙班(VII)的合成路线如图所示,请回答下列问题: (1)、已知:Sn与C同主族,则基态Sn原子的价层电子轨道表示式为。(2)、具有较强的还原性,易被氧化成 , 中Sn原子的杂化类型为 , 分子的空间结构为。(3)、写出化合物I中所有含氧官能团的名称:。(4)、II→III的反应类型为。将物质IV简记为
(1)、已知:Sn与C同主族,则基态Sn原子的价层电子轨道表示式为。(2)、具有较强的还原性,易被氧化成 , 中Sn原子的杂化类型为 , 分子的空间结构为。(3)、写出化合物I中所有含氧官能团的名称:。(4)、II→III的反应类型为。将物质IV简记为 , 则IV→V的化学方程式为。 (5)、请写出以
, 则IV→V的化学方程式为。 (5)、请写出以 和(
和( )为原料合成
)为原料合成 的路线(其他试剂任选)。
的路线(其他试剂任选)。