江西省新余市2021-2022学年高一下学期期末考试化学试题
试卷更新日期:2022-08-01 类型:期末考试
一、单选题
-
1. 2022年北京向世界呈现了一场绿色、科技的冬奥会,下列材料属于非金属单质的是( )
A
B
C
D




冰墩墩的PVC(聚氯乙烯)外壳
“飞扬”火炬中的碳纤维树脂复合材料
首钢大跳台的“钢”
颁奖礼服中的石墨烯
A、A B、B C、C D、D2. 2022年4月16日,神舟十三号飞船成功着陆,此次飞行为中国建造“天宫”空间站打下重要基石。针对空间站中有关配置说法错误的是( )A、核心舱变轨动力依靠电推发动机:相对于化学燃料更加经济与环保 B、生活舱内配备环境控制与生命保障系统:航天员主要通过Na2O获取呼吸用氧 C、可再生水循环系统:从尿液分离出纯净水,可以采用多次蒸馏的方法 D、柔性砷化镓太阳能电池阵:砷化镓属于半导体,相对于硅电池,光电转化率更高3. 下列判断正确的是( )A、CH4和CH3CH2CH3互为同系物 B、H2、D2、T2互为同素异形体 C、 和 互为同分异构体 D、 和 互为同位素4. 足量的Zn粒与0.1mol/L硫酸反应,下列措施既能加快化学反应速率,又不影响氢气总量的是( )①升高温度 ②改用18mol/L硫酸 ③加入少量CuSO4溶液 ④加入几滴浓HNO3 ⑤将Zn粒换成Zn粉 ⑥通入少量HCl气体
A、①③⑤ B、①②④ C、③④⑥ D、全部5. 现有A、B、C、D四种金属,将A与B用导线连接浸入酸性电解质溶液,形成闭合电路,B易腐蚀,将A与D用导线连接浸入酸性电解质溶液电流从D流向A,若将C浸入B的盐溶液中,有金属B析出,这四种金属的活动性顺序为( )A、C>B>A>D B、D>A>B>C C、D>B>A>C D、D>C>A>B6. 反应 , 在不同情况下测得的反应速率,其中反应速率最慢的是( )A、 B、 C、 D、7. 1mol乙烯与足量氯气发生加成反应后,所得加成产物又与足量氯气在光照的条件下发生取代反应,则理论上最多能再消耗氯气的物质的量为( )A、3mol B、4mol C、5mol D、6mol8. 用NA表示阿伏加德罗常数的值。下列与有机物的结构、性质有关的叙述正确的是( )A、28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA B、在密闭容器中加入l.5 mol H2和0.5 mol N2 , 充分反应后可得到NH3分子数为NA C、4.6 g有机物C2H6O的分子中含有的C-H键数目一定为0.5NA D、甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应9. 实验是化学研究的基础.下列关于各实验装置的叙述正确的是( )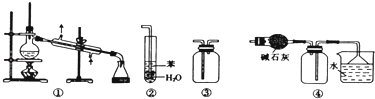 A、装置③可用于收集H2、CO2、Cl2、NH3等气体 B、装置②可用于吸收NH3或HCl气体,并防止倒吸 C、装置①常用于分离互不相溶的液体混合物 D、装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢10. 为了测定铁铜合金的组成,将15.2g铁、铜合金加入200mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体4.48L(标准状况下),并测得反应后溶液中H+的浓度为0.5mol·L-1。若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )A、反应后的溶液中可继续溶解铁铜合金质量最多为1.9g B、上述合金中铁与铜的质量之比为2:3 C、合金中,铁的质量分数为63.2% D、原硝酸的物质的量浓度为c(HNO3)=4.5mol·L-111. 下列有关实验操作、现象和解释或结论都正确的是( )
A、装置③可用于收集H2、CO2、Cl2、NH3等气体 B、装置②可用于吸收NH3或HCl气体,并防止倒吸 C、装置①常用于分离互不相溶的液体混合物 D、装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢10. 为了测定铁铜合金的组成,将15.2g铁、铜合金加入200mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体4.48L(标准状况下),并测得反应后溶液中H+的浓度为0.5mol·L-1。若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )A、反应后的溶液中可继续溶解铁铜合金质量最多为1.9g B、上述合金中铁与铜的质量之比为2:3 C、合金中,铁的质量分数为63.2% D、原硝酸的物质的量浓度为c(HNO3)=4.5mol·L-111. 下列有关实验操作、现象和解释或结论都正确的是( )选项
操 作
现 象
解释或结论
A
过量的Fe粉中加入稀HNO3 , 充分反应后,滴加KSCN溶液
溶液呈红色
稀HNO3将Fe氧化为Fe3+
B
Al箔插入稀HNO3中
无现象
Al箔表面被稀HNO3氧化,形成致密的氧化膜
C
向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口
试纸变蓝
该溶液中存在
D
向紫色石蕊试液中通入SO2
溶液褪色
SO2有漂白性
A、A B、B C、C D、D二、多选题
-
12. 某有机物的结构简式如图,下列说法正确的是( )
 A、分子式为C12H18O5 B、分子中含有2种官能团 C、能发生加成、取代、氧化等反应 D、能使溴的四氯化碳溶液褪色13. 固体氧化物燃料电池以固体氧化锆—氧化钇为电解质,在高温可以传递O2-。电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
A、分子式为C12H18O5 B、分子中含有2种官能团 C、能发生加成、取代、氧化等反应 D、能使溴的四氯化碳溶液褪色13. 固体氧化物燃料电池以固体氧化锆—氧化钇为电解质,在高温可以传递O2-。电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( ) A、多孔电极a为电池的负极 B、O2-移向多孔电极a C、b极的电极反应式:H2−2e-+O2-=H2O D、电子流动方向:b→负载→a14. 下列反应的离子方程式表达错误的是( )A、向FeBr2溶液中通入过量Cl2:2Fe2+ +Cl2=2Fe3++2Cl- B、将少量的NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO+OH-=CaCO3↓十H2O C、向NH4Cl溶液中滴入浓NaOH溶液并加热:NH+OH- NH3↑+H2O D、向氨水中通入少量SO2:NH3·H2O+SO2=NH + HSO
A、多孔电极a为电池的负极 B、O2-移向多孔电极a C、b极的电极反应式:H2−2e-+O2-=H2O D、电子流动方向:b→负载→a14. 下列反应的离子方程式表达错误的是( )A、向FeBr2溶液中通入过量Cl2:2Fe2+ +Cl2=2Fe3++2Cl- B、将少量的NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO+OH-=CaCO3↓十H2O C、向NH4Cl溶液中滴入浓NaOH溶液并加热:NH+OH- NH3↑+H2O D、向氨水中通入少量SO2:NH3·H2O+SO2=NH + HSO三、填空题
-
15. 研究氮的氧化物\碳的氧化物等大气污染物的处理责有重要意义。(1)、汽车尾气中NO生成过程中的能量变化如图所示。

生成1 mol NO(g) ( 填“吸收"或“放出") kJ 的热量。
(2)、汽车排气管内安装的催化转化器可使尾气的主要污染物(NO和CO)转化为无毒的大气循环物质。一定温度下,在恒容密闭容器中发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)。下列能判断该反应达到化学平衡状态的是____(填序号)。A、反应速率v(NO)=v(CO) B、混合气体中NO的物质的量分数保持不变 C、混合气体的密度不再改变 D、混合气体的压强不再改变(3)、用CO2和H2合成甲醇有利于减少碳排放,其反应原理为CO2(g) +3H2(g)=CH3OH(g) +H2O(g)。向甲、乙两个体积都为2.0L的恒容密闭容器中均充入1 mol CO2和3 mol H2 , 甲在T1乙在T2温度下发生上述反应,反应过程中n(CH3OH)随时间(t)的变化见下表:t/min
0
3
6
12
24
36
n甲(CH3OH)/mol
0
0.36
0.60
0.82
0.80
0.80
n乙(CH3OH)/mol
0
0.30
0.50
0.68
0.85
0.85
①T1T2(填“>”“<”或“=”)。
②甲容器中,0 ~6 min内的平均反应速率v(H2)= 。
③甲容器中CO2的平衡转化率为
(4)、一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为3CO2 +4Na=2Na2CO3+C。
①电极a为极(填“正”或“负")。
②电极b发生的电极反应为。
16. 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:(1)、据汞的原子结构示意图 , 汞在第周期。 (2)、①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积L。
, 汞在第周期。 (2)、①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积L。②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。
_Al2O3+_N2+_C—_AlN+_CO
(3)、利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:
①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有(填化学式)。
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为。
17. 海洋是一个巨大的化学资源宝库,请回答下列问题综合利用海水资源可以制备氯化铵、纯碱、金属镁等物质,其流程如图:
 (1)、反应①~⑤中,属于氧化还原反应的是(填序号)。(2)、X溶液中的主要阳离子是和。(3)、粗盐中含、、一等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
(1)、反应①~⑤中,属于氧化还原反应的是(填序号)。(2)、X溶液中的主要阳离子是和。(3)、粗盐中含、、一等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的溶液
②加入过量的溶液
③加入过量的NaOH溶液
④加入盐酸调节溶液至中性
⑤溶解
⑥过滤
⑦蒸发
正确的操作顺序是____(填字母)。
A、⑤②③①④⑥⑦ B、⑤①②③⑥④⑦ C、⑤②①③④⑥⑦ D、⑤③②①⑥④⑦(4)、实验室中需2mol/L的溶液950mL,配制时需称取的质量是g。(5)、需要的玻璃仪器有玻璃棒、烧杯、量筒,还缺少的玻璃仪器有(填写仪器名称)。(6)、若出现如下情况,其中将引起所配溶液浓度偏高的是____(填下列编号)。A、容量瓶实验前用蒸馏水洗干净,但未烘干 B、定容观察液面时俯视 C、未冷却至室温就开始定容 D、加蒸馏水时不慎超过了刻度18.(1)、I.烃A是一种重要的化工原料,标准状况下密度为1.25g/L,E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料,各物质的转化关系如下:请回答:
F的结构简式是。
(2)、D中所含官能团的名称是。(3)、B与D反应生成E的化学反应方程式是。(4)、下列说法正确的是____。A、等物质的量的A和B完全燃烧消耗氧气的质量不相等 B、F绝缘性好,耐化学腐蚀,耐寒,无毒 C、E具有香味,能使酸性溶液褪色 D、B进入人体后在酶的作用下被氧化成C,对人体造成毒害作用(5)、II.有机物G的结构简式如图,回答下列问题。
G的分子式为。
(6)、1molG与足量的Na反应,生成mol,与足量的反应,生成mol(7)、有机玻璃是一种高分子聚合物,单体是 , 写出合成有机玻璃的化学方程式。