江西省萍乡市2021-2022学年高一下学期期末考化学试题
试卷更新日期:2022-08-01 类型:期末考试
一、单选题
-
1. 2022年2月4日,第二十四届冬奥会在北京开幕,北京成为世界上首个“双奥之城”。本届冬奥会背后蕴含了很多科技成果下列说法正确的是( )A、颁奖礼服内添加了石墨烯发热材料,石墨烯和C60是同位素 B、冬奥火炬“飞扬”使用氢气作为燃料,氢能属于新能源 C、吉祥物冰墩墩的外壳使用了有机硅橡胶材料,属于硅酸盐材料 D、国家速滑馆的冰面是采用超临界二氧化碳流体跨临界直冷制冰技术打造的,该过程是化学变化2. 化学与生产生活密切相关。下列说法错误的是( )A、多糖、蛋白质都是高分子化合物,一定条件下都能水解 B、具有特殊的光学性能,可用于制作光导纤维 C、尼龙绳、羊绒衫和棉衬衣等生活用品都是由合成纤维制造的 D、不溶于水和酸,可用于胃肠X射线造影检查3. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,11.2 L乙醇中含H-O键数目为0.5NA B、常温常压下,1 mol乙烷和乙烯的混合物完全燃烧,产生的分子数目为2NA C、17.4g与40mL 10mol/L浓盐酸反应,转移电子的数目为0.2NA D、1 mol/L 溶液和1 mol/L的NaCl溶液等体积混合,的数目为4NA4. 如图是正丁烷的球棍模型,有关该结构说法正确的是( )
 A、正丁烷的分子式为 B、分子中共含有12个共价键 C、与甲烷互为同系物 D、存有多种(2种以上)同分异构体5. 下列物质相遇时,没有发生氧化还原反应的是( )A、氨遇到氯化氢时产生白烟 B、红热的木炭遇到浓硝酸产生红棕色气体 C、光亮的铁钉插入浓硫酸中,无明显现象 D、在酒精灯上灼烧后变黑的铜丝插入乙醇中,铜丝变红6. 利用固体表面催化工艺进行分解的过程如图所示。
A、正丁烷的分子式为 B、分子中共含有12个共价键 C、与甲烷互为同系物 D、存有多种(2种以上)同分异构体5. 下列物质相遇时,没有发生氧化还原反应的是( )A、氨遇到氯化氢时产生白烟 B、红热的木炭遇到浓硝酸产生红棕色气体 C、光亮的铁钉插入浓硫酸中,无明显现象 D、在酒精灯上灼烧后变黑的铜丝插入乙醇中,铜丝变红6. 利用固体表面催化工艺进行分解的过程如图所示。
下列说法错误的是( )
A、是有毒气体 B、催化剂能改变的分解速率 C、分解生成和 D、过程②释放能量,过程③吸收能量7. 下列有机反应中,属于取代反应的是( )A、 B、 C、 D、8. 如图所示的原电池装置X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( ) A、电极X为正极,发生还原反应 B、移向Y电极 C、若分别用Zn和Fe做电极材料,则电极Y为Zn D、电极Y上有氢气生成9. 在给定的条件下,下列物质间转化均能实现的是( )A、 B、 C、 D、10. 已知短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子的最外层电子数是内层电子数的3倍,Y与X能形成两种化合物,Z所在的周期序数与族序数相同,W与X同主族。下列说法正确的是( )A、Y的单质能从Z的盐溶液中置换出Z B、氢化物的热稳定性:W>X C、工业上常用电解法冶炼Z和W形成的化合物获得Z单质 D、简单离子的半径大小:W>X>Y>Z11. 一定温度下,在恒容密闭容器中发生反应: , 下列说法错误的是( )A、升高温度可以提高正、逆反应速率 B、该反应达到化学平衡状态时,、、的浓度一定相等 C、当、的浓度不再变化时,该反应达到化学平衡状态 D、在给定条件下,反应达到平衡时,氮气的转化率达到最大12. 用下图装置探究铜与硝酸的反应,实验记录如下:
A、电极X为正极,发生还原反应 B、移向Y电极 C、若分别用Zn和Fe做电极材料,则电极Y为Zn D、电极Y上有氢气生成9. 在给定的条件下,下列物质间转化均能实现的是( )A、 B、 C、 D、10. 已知短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子的最外层电子数是内层电子数的3倍,Y与X能形成两种化合物,Z所在的周期序数与族序数相同,W与X同主族。下列说法正确的是( )A、Y的单质能从Z的盐溶液中置换出Z B、氢化物的热稳定性:W>X C、工业上常用电解法冶炼Z和W形成的化合物获得Z单质 D、简单离子的半径大小:W>X>Y>Z11. 一定温度下,在恒容密闭容器中发生反应: , 下列说法错误的是( )A、升高温度可以提高正、逆反应速率 B、该反应达到化学平衡状态时,、、的浓度一定相等 C、当、的浓度不再变化时,该反应达到化学平衡状态 D、在给定条件下,反应达到平衡时,氮气的转化率达到最大12. 用下图装置探究铜与硝酸的反应,实验记录如下:装置
步骤
操作
现象
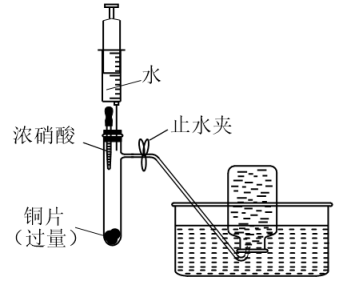
①
打开止水夹,挤压胶头,使浓硝酸滴入试管
产生红棕色气体,溶液变为绿色
②
一段时间后,关闭止水夹,推动注射器活塞使部分水进入试管
注射器内剩余的水被“吸入”试管;铜表面产生无色气泡,溶液变蓝,试管内气体逐渐变为无色
③
一段时间后, 打开止水夹,拉动注射器活塞吸取少量无色气体;拔下注射器,再拉动活塞吸入少量空气
注射器中无色气体变红棕色
下列说法错误的是( )
A、①中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2 +2NO2↑ + 2H2O B、②中注射器内剩余的水被“吸入”试管的原因可能是NO2与H2O反应导致压强减小 C、②中铜表面产生的气体可能有H2 D、③中的实验现象能证明②中反应生成了NO13. 已知与足量的10mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )A、反应中铜、硫元素的化合价发生变化 B、刺激性气味的气体可能是氨气 C、蓝色溶液中的溶质只有硫酸铜 D、162g完全反应转移0.5 mol电子14. 碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
下列说法正确的是( )
A、分离器中的物质分离操作为过滤 B、该工艺中I2和HI的相互转化体现了“碘循环” C、该工艺中HI的量没有改变,可视作该工艺的催化剂 D、碘循环工艺的总反应为 2SO2+4H2O+I2=H2+2H2SO4+2HI二、综合题
-
15. 有机化合物A的相对分子质量是28的烃,B和D都是日常生活食品中常见的有机物。它们的转化关系如图所示:

请回答下列问题:
(1)、A的结构简式为 , 可通过石油的(填“蒸馏”、“干馏”或“裂解”)获得。(2)、①的反应类型为 , D分子中所含官能团的名称为。丙烯与A互为同系物,聚丙烯的结构简式为。(3)、反应④的化学方程式为: , 该反应中,浓硫酸所起的作用是。(4)、以淀粉为原料经反应⑤、⑥也可制得B,下列说法正确的是(填字母)a.纤维素和淀粉一样也可用于生产B
b.反应⑤⑥都属于水解反应
c.淀粉属于糖类,糖类都是高分子化合物
d.淀粉水解的最终产物可用银氨溶液或新制氢氧化铜检验
16. 海洋是巨大的化学资源宝库,如图是从海水中提取溴的流程图(部分)。据图回答下列问题。 (1)、写出一种工业上海水淡化的方法:。(2)、过程1发生反应的离子方程式是。该反应可证明氧化性:(填“>”、“<”或者“=”),从原子结构角度解释原因。(3)、过程2中发生反应生成两种强酸,写出该反应的化学方程式:。(4)、上述过程2中将转化成的目的是。(5)、若过程2用溶液吸收溴,补全方程式:。
(1)、写出一种工业上海水淡化的方法:。(2)、过程1发生反应的离子方程式是。该反应可证明氧化性:(填“>”、“<”或者“=”),从原子结构角度解释原因。(3)、过程2中发生反应生成两种强酸,写出该反应的化学方程式:。(4)、上述过程2中将转化成的目的是。(5)、若过程2用溶液吸收溴,补全方程式:。3+_+_=_+_+_
若反应中转移电子的物质的量为5mol,则被还原的溴单质的质量为:。
17. 某学校化学兴趣小组对必修二课本上的两个实验活动进行分组实验。(1)、Ⅰ.第一实验小组用硫代硫酸钠与硫酸反应研究反应物浓度和温度对该反应速率的影响,设计以下三组实验。已知硫代硫酸钠与稀硫酸反应的方程式为:回答下列问题。
实验序号
反应温度(℃)
溶液
稀硫酸
产生沉淀时间
V/mL
c/(mol/L)
V/mL
c/(mol/L)
V/mL
Ⅰ
25
5
0.2
10
0.1
x
Ⅱ
25
10
0.1
10
0.2
5
Ⅲ
35
10
0.1
5
y
10
该反应所需的仪器有:量筒、烧杯、试管、药匙、试管架、胶头滴管、秒表、
(2)、对比实验Ⅰ、Ⅱ研究对该反应速率的影响,x=(3)、对比实验Ⅱ、Ⅲ研究对该反应速率的影响,y=(4)、Ⅱ.第二实验小组设计乙醇催化氧化的实验装置(加热仪器、铁架台、铁夹等均已略去)。其中A为无水乙醇(沸点78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的悬浊液。(提示:乙醛具有与葡萄糖相似的性质)
加热装置E中的固体,目的是。
(5)、为了使A中的乙醇平稳汽化成蒸气,可采用的加热方法是;D处使用碱石灰的作用是。(6)、乙醇催化氧化的化学方程式为。(7)、能证明乙醇反应后的产物的实验现象是:图中C处 , F处。三、填空题
-
18. 甲醇()是应用广泛的化工原料和前景乐观的燃料。(1)、Ⅰ.一定条件下,在5L密闭容器中充入1mol 和3 mol , 发生反应:。测得和的物质的量随时间变化如图所示。据图回答下列问题。

x=;0~3min内的平均反应速率mol/(L·min)。
(2)、下列措施能提高正反应速率的是____(填字母)。A、降低温度 B、增加的量 C、及时分离出甲醇 D、使用催化剂(3)、Ⅱ.甲醇燃料电池可使甲醇作燃料时的能量转化更高效,某种甲醇燃料电池的工作原理如图所示,其电极反应如下:
电极A的名称是(填“正极”或“负极”);甲醇从(填“b”或“c”)处通入。
(4)、甲醇燃料电池供电时的总反应方程式为(5)、当该装置消耗64g甲醇时,转移电子的数目为;若这部分电子全部用于电解水,理论上可产生标准状况下氢气L。