广西贺州市2021-2022学年高一下学期期末考试化学试题
试卷更新日期:2022-08-01 类型:期末考试
一、单选题
-
1. 化学与人类社会生产、生活有着密切联系。下列叙述中错误的是( )A、维生素C可用作水果罐头的抗氧化剂 B、温度越高,酶的催化效率越高 C、葡萄酒中添加入适量的可以起到保质的作用 D、高温、75%酒精、84消毒液(含NaClO)都可使新冠病毒蛋白质变性2. 化学用语是用来表示化学意义的符号或图示等,下列化学用语表示正确的是( )A、丙烷的结构简式: B、中子数为17的氯原子: C、氨分子的电子式:
 D、离子的结构示意图:
D、离子的结构示意图: 3. 配制一定物质的量浓度的氯化钠溶液时,下列操作规范的是( )
3. 配制一定物质的量浓度的氯化钠溶液时,下列操作规范的是( )A
B
C
D




称量
溶解
移液
定容
A、A B、B C、C D、D4. 有广告称某品牌的八宝粥(含糯米、红豆、桂圆等)不含糖,适合糖尿病患者食用。你认为下列判断错误的是( )A、不能盲从广告宣传 B、该广告有可能误导消费者 C、不含糖不等于没有糖类物质,糖尿病患者食用时需谨慎考虑 D、糖尿病患者应少吃含糖食品,该八宝粥不加糖,可以放心食用5. 北京大学和中国科学院的化学工作者已成功研制出碱金属与形成的球碳盐 , 实验测知该物质属于离子化合物,具有良好的超导性。下列有关分析错误的是( )A、中只有离子键 B、该晶体在熔融状态下能导电 C、中只含共价键 D、与金刚石互为同素异形体6. 中学生应掌握常见化学物质的保存,并具备一定的安全常识,下列做法不合理的是( )A、浓硝酸应该保存在棕色试剂瓶中,并放置在阴凉处 B、不慎将碱液沾到皮肤上,应立即用大量的水冲洗,再涂上1%的硼酸 C、实验没有用完的金属钠、钾及白磷等不能放回原瓶,统一回收丢垃圾桶 D、浓硫酸沾到皮肤上,应立即先用布擦干,用大量的水冲洗,再用3%~5%的碳酸氢钠溶液冲洗7. 用表示阿伏加德罗常数的数值,下列说法正确的是( )A、1molO质量是16g/mol B、中含有的电子数为 C、溶液中含有Cl-的数目为 D、标准状况下,11.2L乙醇所含分子数为8. 在密闭容器中加入和进行反应: , 下列说法正确的是( )A、降低温度能加快反应速率 B、充分反应后,可以生成 C、达到平衡时:v(正)=v(逆)=0 D、体积不变,充入 , 能加快反应速率9. 汽车尾气中含CO、NO等多种污染物,已成为城市空气的主要污染源。在排气管上安装三元催化装置,可以使CO、NO转化变成无毒气体。则下列说法错误的是( )A、反应方程式为 B、反应中NO为氧化剂,为还原产物 C、CO、NO属于酸性氧化物 D、因酸雨中常含有硫酸、硝酸等,所以其pH<5.610. 下列选用的试剂或方法不能达到对应实验目的的是 ( )选项
实验目的
选用试剂或方法
A
检验溶液是否含有
溶液、稀硝酸
B
除去氨气中的水蒸气
浓
C
鉴别胶体和溶液
丁达尔效应
D
检测糖尿病人尿液中含有葡萄糖
新制的
A、A B、B C、C D、D11. 利用铁元素价类二维图可以多角度研究含铁物质的性质及其转化关系,下列说法错误的是 ( ) A、铁在氧气中燃烧可以实现转化① B、在空气中可以进一步转化为 C、由图可预测高铁酸盐()具有强氧化性 D、可以通过如下反应转化为:12. 《厉害了,我的国》展示了中国在探索太空、开发深海、开发5G技术等领域取得的举世瞩目的成就。它们与化学有着密切联系,下列对应关系错误的是( )A、5G手机芯片的关键材料——二氧化硅 B、神舟飞船航天员穿的航天服的材料——多种合成纤维 C、制造“蛟龙”号载人潜水器的耐压球壳采用的钛合金——金属材料 D、神舟飞船返回舱外表面使用的高温结构陶瓷的主要成分——新型无机非金属材料13. 下列离子方程式正确的是( )A、Na与反应: B、溶液加入氨水: C、溶液中加入稀硫酸: D、澄清石灰水中通入:14. 下列各组离子,能在溶液中大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、15. 银锌电池是一种微型纽扣电池,总反应式为: , 其电极分别是Zn和 , 下列说法错误的是 ( )
A、铁在氧气中燃烧可以实现转化① B、在空气中可以进一步转化为 C、由图可预测高铁酸盐()具有强氧化性 D、可以通过如下反应转化为:12. 《厉害了,我的国》展示了中国在探索太空、开发深海、开发5G技术等领域取得的举世瞩目的成就。它们与化学有着密切联系,下列对应关系错误的是( )A、5G手机芯片的关键材料——二氧化硅 B、神舟飞船航天员穿的航天服的材料——多种合成纤维 C、制造“蛟龙”号载人潜水器的耐压球壳采用的钛合金——金属材料 D、神舟飞船返回舱外表面使用的高温结构陶瓷的主要成分——新型无机非金属材料13. 下列离子方程式正确的是( )A、Na与反应: B、溶液加入氨水: C、溶液中加入稀硫酸: D、澄清石灰水中通入:14. 下列各组离子,能在溶液中大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、15. 银锌电池是一种微型纽扣电池,总反应式为: , 其电极分别是Zn和 , 下列说法错误的是 ( ) A、锌作电源的负极 B、正极发生还原反应 C、电池工作时,电子从经导线流向Zn D、若有0.2mol电子流经导线,则可产生银21.6g16. 已知 , 则下列说法正确的是( )A、Cu在反应中失去电子,作氧化剂 B、浓硫酸在该反应中只表现出强氧化性 C、该反应中还原剂与氧化剂的物质的量之比为1∶2 D、标准状况下,每生成22.4LSO2就有2mol电子转移17. T℃时,将15molA与10molB混合后通入容积为5L的密闭容器中,发生如下反应: , 10s时反应达到平衡,此时 , 下列结论错误的是( )A、反应达平衡时,B的转化率为30% B、该反应进行到10s时,生成了6mol的C C、10s内用B表示的反应速率为 D、将容器的体积扩大至10L能使该反应的反应速率减小18. 我国药学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理学或医学奖。已知二羟甲戊酸(
A、锌作电源的负极 B、正极发生还原反应 C、电池工作时,电子从经导线流向Zn D、若有0.2mol电子流经导线,则可产生银21.6g16. 已知 , 则下列说法正确的是( )A、Cu在反应中失去电子,作氧化剂 B、浓硫酸在该反应中只表现出强氧化性 C、该反应中还原剂与氧化剂的物质的量之比为1∶2 D、标准状况下,每生成22.4LSO2就有2mol电子转移17. T℃时,将15molA与10molB混合后通入容积为5L的密闭容器中,发生如下反应: , 10s时反应达到平衡,此时 , 下列结论错误的是( )A、反应达平衡时,B的转化率为30% B、该反应进行到10s时,生成了6mol的C C、10s内用B表示的反应速率为 D、将容器的体积扩大至10L能使该反应的反应速率减小18. 我国药学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理学或医学奖。已知二羟甲戊酸(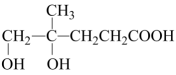 )是生物合成青蒿素的原料之一,关于二羟甲戊酸的说法错误的是( ) A、能与乙醇发生酯化反应 B、能与氢氧化钠发生中和反应 C、可以发生加成反应和取代反应 D、1mol该有机物与足量金属钠反应产生19. 除去粗盐中的杂质MgCl2、CaCl2和Na2SO4 , 过程如下:
)是生物合成青蒿素的原料之一,关于二羟甲戊酸的说法错误的是( ) A、能与乙醇发生酯化反应 B、能与氢氧化钠发生中和反应 C、可以发生加成反应和取代反应 D、1mol该有机物与足量金属钠反应产生19. 除去粗盐中的杂质MgCl2、CaCl2和Na2SO4 , 过程如下:
下列有关说法中,错误的是( )
A、除去Ca2+的主要反应:Ca2+ + CO= CaCO3↓ B、试剂①、②、③分别是NaOH、Na2CO3、BaCl2 C、加稀盐酸调节pH后,采用蒸发结晶的方法得到NaCl固体 D、检验SO是否除净的方法:取适量滤液,加稀盐酸酸化,再加BaCl2溶液20. 已知:将通入适量KOH溶液,产物中可能有KCl、KClO、 , 且产物的成分与温度高低有关。当时,下列有关说法错误的是( )A、参加反应的氯气的物质的量等于 B、改变温度,产物中的最大理论产量为 C、改变温度,反应中转移电子的物质的量n的范围是 D、某温度下,反应后 , 则溶液中二、综合题
-
21. 某研究性学习小组利用如图所示的装置制备无水氯化铁。
 (1)、装置Ⅰ中仪器A的名称是 , 写出装置Ⅰ中制备氯气的离子方程式。(2)、装置Ⅱ的作用是 , 装置Ⅲ的溶液是。(3)、写出在装置Ⅳ中发生的反应的化学方程式。(4)、实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到 , 即可证明滤液中含有。(5)、另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的装置(填序号)。
(1)、装置Ⅰ中仪器A的名称是 , 写出装置Ⅰ中制备氯气的离子方程式。(2)、装置Ⅱ的作用是 , 装置Ⅲ的溶液是。(3)、写出在装置Ⅳ中发生的反应的化学方程式。(4)、实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到 , 即可证明滤液中含有。(5)、另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的装置(填序号)。 22. 下图是元素周期表的一部分,表中序号分别代表某一元素,请回答下列问题:
22. 下图是元素周期表的一部分,表中序号分别代表某一元素,请回答下列问题: (1)、下图模型表示的分子中,不可能由①和②形成的是____(填序号)。A、
(1)、下图模型表示的分子中,不可能由①和②形成的是____(填序号)。A、 B、
B、 C、
C、 D、
D、 (2)、②的最高价氧化物的电子式为。(3)、在这些元素中,化学性质最不活泼的是(填元素符号)。(4)、W是第四周期与③同主族的元素。据此推测W不可能具有的性质是____。A、最高正化合价为+6 B、最高价氧化物对应水化物的酸性比硫酸弱 C、气态氢化物比稳定 D、单质在常温下可与氢气化合(5)、⑥的单质与氧气剧烈反应生成的淡黄色固体,其化学式为。(6)、元素③在元素周期表中的位置是。(7)、元素④、⑥、⑨的简单离子半径由大到小的顺序为(用离子符号表示)(8)、写出⑥、⑦最高价氧化物对应水化物在有水存在条件下相互反应的化学方程式。23. 工业制硫酸中的一步重要反应是的催化氧化。在2L密闭容器中,充入和 , 在催化剂、500℃的条件下发生反应。请结合下图数据,回答下列问题。
(2)、②的最高价氧化物的电子式为。(3)、在这些元素中,化学性质最不活泼的是(填元素符号)。(4)、W是第四周期与③同主族的元素。据此推测W不可能具有的性质是____。A、最高正化合价为+6 B、最高价氧化物对应水化物的酸性比硫酸弱 C、气态氢化物比稳定 D、单质在常温下可与氢气化合(5)、⑥的单质与氧气剧烈反应生成的淡黄色固体,其化学式为。(6)、元素③在元素周期表中的位置是。(7)、元素④、⑥、⑨的简单离子半径由大到小的顺序为(用离子符号表示)(8)、写出⑥、⑦最高价氧化物对应水化物在有水存在条件下相互反应的化学方程式。23. 工业制硫酸中的一步重要反应是的催化氧化。在2L密闭容器中,充入和 , 在催化剂、500℃的条件下发生反应。请结合下图数据,回答下列问题。 (1)、写出该反应的化学方程式。(2)、反应开始至20min末,以的变化表示该反应的平均速率是。(3)、下列叙述不能判断该反应达到平衡状态是____(填字母)A、容器中压强不再改变 B、的质量不再改变 C、的浓度与的浓度相等 D、单位时间内生成1mol , 同时生成1mol(4)、已知2mol与1mol的总能量比2mol的能量大196kJ。以下能正确表示催化氧化生成的能量变化过程的图示是____(填字母)A、
(1)、写出该反应的化学方程式。(2)、反应开始至20min末,以的变化表示该反应的平均速率是。(3)、下列叙述不能判断该反应达到平衡状态是____(填字母)A、容器中压强不再改变 B、的质量不再改变 C、的浓度与的浓度相等 D、单位时间内生成1mol , 同时生成1mol(4)、已知2mol与1mol的总能量比2mol的能量大196kJ。以下能正确表示催化氧化生成的能量变化过程的图示是____(填字母)A、 B、
B、 C、
C、 D、
D、 (5)、某课外活动小组利用能使酸性溶液褪色的原理测定空气中的含量,这一现象体现了的性。(6)、某企业利用下图流程综合处理工厂排放的含的烟气,以减少其对环境造成的污染。“氨气吸收塔”中发生反应的化学方程式为 , 在整个流程中可循环利用的物质为(填化学式)。
(5)、某课外活动小组利用能使酸性溶液褪色的原理测定空气中的含量,这一现象体现了的性。(6)、某企业利用下图流程综合处理工厂排放的含的烟气,以减少其对环境造成的污染。“氨气吸收塔”中发生反应的化学方程式为 , 在整个流程中可循环利用的物质为(填化学式)。 (7)、硝酸工业的尾气中含有NO,光催化氧化法脱除NO的过程如图所示。图中最终转化为的化学方程式为。
(7)、硝酸工业的尾气中含有NO,光催化氧化法脱除NO的过程如图所示。图中最终转化为的化学方程式为。 24. 已知可作果实催熟剂,其产量可作为一个国家石油化工发展水平的标志,B和D是生活中常见的有机物,其中B与金属钠可以缓慢反应生成氢气。各物质相互转换关系如图所示。
24. 已知可作果实催熟剂,其产量可作为一个国家石油化工发展水平的标志,B和D是生活中常见的有机物,其中B与金属钠可以缓慢反应生成氢气。各物质相互转换关系如图所示。 (1)、的结构简式为 , 和互为(填“同分异构体”或“同系物”)。(2)、下列能鉴别和的试剂是____(填字母)A、稀硫酸 B、溴的四氯化碳溶液 C、氢氧化钠溶液 D、酸性高锰酸钾溶液(3)、D的官能团名称是。(4)、在催化剂、加热、加压条件下与水反应生成B,其方程式为。(5)、某兴趣小组用如图所示的装置模拟反应④。请回答下列问题:
(1)、的结构简式为 , 和互为(填“同分异构体”或“同系物”)。(2)、下列能鉴别和的试剂是____(填字母)A、稀硫酸 B、溴的四氯化碳溶液 C、氢氧化钠溶液 D、酸性高锰酸钾溶液(3)、D的官能团名称是。(4)、在催化剂、加热、加压条件下与水反应生成B,其方程式为。(5)、某兴趣小组用如图所示的装置模拟反应④。请回答下列问题: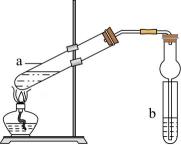
①试管a中发生反应的化学方程式为。
②图中球形干燥管除起冷凝作用外,另一个重要作用是。