广东省汕头市2021-2022学年高一下学期期末教学质量检测化学试题
试卷更新日期:2022-08-01 类型:期末考试
一、单选题
-
1. 下列化学用语表示正确的是( )A、的电子式:
 B、蔗糖的分子式:
C、乙烯的空间填充模型:
B、蔗糖的分子式:
C、乙烯的空间填充模型: D、的结构示意图:
D、的结构示意图: 2. 下列材料不属于合金的是( )
2. 下列材料不属于合金的是( )



A.制造下水井盖用的生铁
B.制作餐具用的不锈钢
C.储存和释放氢气用的储氢合金
D.制作显示屏的有机发光材料
A、A B、B C、C D、D3. 2020年12月17日凌晨,嫦娥五号携带月壤等样本成功返回地球,首次完成月球表面自动采样。下列说法错误的是( ) A、发射时使用液氢和液氧作推进剂,是利用燃烧反应提供能量 B、探测器使用的硅太阳能电池板,其主要成分是SiO2 C、“月壤”中含有珍贵的3He,3He与4He互为同位素 D、上升器用到碳纤维复合材料,主要利用其质轻、强度大和耐高温等性能4. 下列说法正确的是( )A、在无色透明溶液中,、、、能大量共存 B、在的溶液中,、、、能大量共存 C、氯化铁溶液刻蚀铜电路板的离子方程式为: D、铜与浓硝酸反应的离子方程式为:5. 2021年12月9日下午,神舟十三号“太空出差三人组”在中国空间站进行了太空授课,“太空教师”王亚平介绍了宇航员在太空中的主要氧气来源为电解水产生。下列关于电解水的说法正确的是( )A、水既是氧化剂也是还原剂 B、中的O元素被还原 C、每生成共转移2mol电子 D、电解水时产生的为氧化产物6. 设为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,含有的分子数为 B、常温常压下,0.1molCO含有的原子数为 C、溶液中的数目为 D、和含有的电子数均为7. 劳动成就梦想。下列家务劳动所涉及的化学知识错误的是( )
A、发射时使用液氢和液氧作推进剂,是利用燃烧反应提供能量 B、探测器使用的硅太阳能电池板,其主要成分是SiO2 C、“月壤”中含有珍贵的3He,3He与4He互为同位素 D、上升器用到碳纤维复合材料,主要利用其质轻、强度大和耐高温等性能4. 下列说法正确的是( )A、在无色透明溶液中,、、、能大量共存 B、在的溶液中,、、、能大量共存 C、氯化铁溶液刻蚀铜电路板的离子方程式为: D、铜与浓硝酸反应的离子方程式为:5. 2021年12月9日下午,神舟十三号“太空出差三人组”在中国空间站进行了太空授课,“太空教师”王亚平介绍了宇航员在太空中的主要氧气来源为电解水产生。下列关于电解水的说法正确的是( )A、水既是氧化剂也是还原剂 B、中的O元素被还原 C、每生成共转移2mol电子 D、电解水时产生的为氧化产物6. 设为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,含有的分子数为 B、常温常压下,0.1molCO含有的原子数为 C、溶液中的数目为 D、和含有的电子数均为7. 劳动成就梦想。下列家务劳动所涉及的化学知识错误的是( )选项
家务劳动
化学知识
A
用小苏打烘焙糕点
受热易分解
B
用铝制锅烧水、煮饭
铝的熔点较高
C
用白醋清洗水壶中的水垢
白醋可溶解碳酸钙等沉淀
D
用84消毒液对桌椅消毒
具有氧化性
A、A B、B C、C D、D8. 《史记》里有记载,大豆起源于中国,劳动人民早在两千多年前就开始利用大豆制作豆腐,下列说法错误的是( )磨豆
滤渣
煮浆
点卤



 A、“磨豆”过程中大豆蛋白发生水解生成氨基酸 B、“滤渣”步骤中使用到多层纱布,功能相当于过滤时的滤纸 C、“煮浆”主要有灭菌、蛋白质变性等作用 D、“点卤”过程添加凝固剂可选用石膏或氯化镁9. 化学与生活密切相关,下列有关说法错误的是( )A、糖尿病人尿液与新制氢氧化铜反应生成砖红色的氧化铜沉淀 B、氢氟酸可用于在玻璃器皿上刻蚀标记 C、氨易液化,汽化时会吸收大量热,可作制冷剂 D、食物油和白酒都应该密封保存10. 进行下列实验时,选用仪器或操作错误的是( )
A、“磨豆”过程中大豆蛋白发生水解生成氨基酸 B、“滤渣”步骤中使用到多层纱布,功能相当于过滤时的滤纸 C、“煮浆”主要有灭菌、蛋白质变性等作用 D、“点卤”过程添加凝固剂可选用石膏或氯化镁9. 化学与生活密切相关,下列有关说法错误的是( )A、糖尿病人尿液与新制氢氧化铜反应生成砖红色的氧化铜沉淀 B、氢氟酸可用于在玻璃器皿上刻蚀标记 C、氨易液化,汽化时会吸收大量热,可作制冷剂 D、食物油和白酒都应该密封保存10. 进行下列实验时,选用仪器或操作错误的是( )A.鉴别纯碱与小苏打
B.铁粉与水蒸气反应
C.证明易与NaOH溶液反应
D.配制0.10mo/L的硫酸



 A、A B、B C、C D、D11. “绿色冬奥”、“科技冬奥”和“人文冬奥”是总结2022年北京冬奥会的三个关键词,下列有关说法错误的是( )A、吉祥物冰墩墩的外壳材料(聚氯乙烯)是一种混合物 B、火炬“飞扬”使用氢气作为燃料,其火焰为黄色,可能是发生了焰色试验 C、礼仪服中用来保暖的石墨烯材料是一种新型有机高分子化合物 D、速滑运动员使用的速滑冰刀由不锈钢制成,其主要金属铝的工业制法为电解法12. 理论研究表明,在101kPa和298K下,异构化反应过程的能量变化如图所示。下列说法错误的是( )
A、A B、B C、C D、D11. “绿色冬奥”、“科技冬奥”和“人文冬奥”是总结2022年北京冬奥会的三个关键词,下列有关说法错误的是( )A、吉祥物冰墩墩的外壳材料(聚氯乙烯)是一种混合物 B、火炬“飞扬”使用氢气作为燃料,其火焰为黄色,可能是发生了焰色试验 C、礼仪服中用来保暖的石墨烯材料是一种新型有机高分子化合物 D、速滑运动员使用的速滑冰刀由不锈钢制成,其主要金属铝的工业制法为电解法12. 理论研究表明,在101kPa和298K下,异构化反应过程的能量变化如图所示。下列说法错误的是( ) A、HCN比HNC稳定 B、1molHCN转化为1molHNC需要吸收59.3kJ的热量 C、反应过程中断开旧化学键吸收的总能量高于形成新化学键放出的总能量 D、该异构化反应只有在加热条件下才能进行13. 一种发光二极管连接柠檬电池装置如图所示。下列说法正确的是( )
A、HCN比HNC稳定 B、1molHCN转化为1molHNC需要吸收59.3kJ的热量 C、反应过程中断开旧化学键吸收的总能量高于形成新化学键放出的总能量 D、该异构化反应只有在加热条件下才能进行13. 一种发光二极管连接柠檬电池装置如图所示。下列说法正确的是( ) A、该装置实现了电能转化为化学能 B、电子由铜线经发光二极管流向铁环 C、负极的电极反应: D、可将柠檬替换成盛装酒精的烧杯14. 一定温度下,在2L恒容密闭容器中发生反应A(g)+2B(g)⇌3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是( )
A、该装置实现了电能转化为化学能 B、电子由铜线经发光二极管流向铁环 C、负极的电极反应: D、可将柠檬替换成盛装酒精的烧杯14. 一定温度下,在2L恒容密闭容器中发生反应A(g)+2B(g)⇌3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是( )n/mol
t/min
n(A)
n(B)
n(C)
0
2
2.4
0
5
0.9
10
1.6
15
1.6
A、0~5min用A表示的平均反应速率为0.09mol·L-1 B、该反应在10min后才达平衡 C、平衡状态时,c(C)=0.6mol·L-1 D、物质B的平衡转化率为20%15. 大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物一光化学烟雾,其中部分物质的反应过程如图所示。下列说法正确的是( ) A、该过程中O2作催化剂 B、反应过程中没有电子转移 C、反应过程中氮氧化物不断被消耗 D、丙烯转化为甲醛和乙醛16. 有机物M是一种抑制生长的植物激素,可以刺激乙烯的产生,催促果实成熟,其结构简式如图所示,下列关于有机物M的性质的描述正确的是( )
A、该过程中O2作催化剂 B、反应过程中没有电子转移 C、反应过程中氮氧化物不断被消耗 D、丙烯转化为甲醛和乙醛16. 有机物M是一种抑制生长的植物激素,可以刺激乙烯的产生,催促果实成熟,其结构简式如图所示,下列关于有机物M的性质的描述正确的是( ) A、分子中所有碳原子可能共平面 B、1molM和足量的钠反应生成 C、1molM最多可以和发生加成反应 D、1molM可以和发生中和反应,且可生成17. 下列实验操作和现象所得结论正确的是( )
A、分子中所有碳原子可能共平面 B、1molM和足量的钠反应生成 C、1molM最多可以和发生加成反应 D、1molM可以和发生中和反应,且可生成17. 下列实验操作和现象所得结论正确的是( )选项
实验操作
现象
结论
A
将通入高锰酸钾溶液中
溶液褪色
二氧化硫有漂白性
B
用洁净铂丝蘸取溶液X进行焰色试验
火焰呈黄色
溶液X可能含有
C
向溶液Y中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口
试纸不变蓝
溶液Y中不含
D
取少量纯蔗糖加适量水配成溶液,向蔗糖溶液中加入3-5滴稀硫酸;将混合液煮沸几分钟,冷却;向冷却液中直接加入银氨溶液,水浴加热
没有银镜产生
蔗糖尚未水解
A、A B、B C、C D、D18. 科学家提出有关甲醇(CH3OH)的碳循环如图所示。下列说法正确的是(“碳中和”是指CO2的排放总量和减少总量相当)( ) A、图中能量转化方式只有2种 B、CO2、CH3OH均属于有机物 C、CO2和H2合成CH3OH的反应中原子利用率为100% D、利用CO2合成CH3OH燃料有利于促进“碳中和”19. 四氧化三铁磁流体既具有固体的磁性,又具有液体的流动性,采用共沉淀法可以制得黑色的分散质微粒直径介于5.5-36 nm纳米级磁流体材料。其流程如下图所示:
A、图中能量转化方式只有2种 B、CO2、CH3OH均属于有机物 C、CO2和H2合成CH3OH的反应中原子利用率为100% D、利用CO2合成CH3OH燃料有利于促进“碳中和”19. 四氧化三铁磁流体既具有固体的磁性,又具有液体的流动性,采用共沉淀法可以制得黑色的分散质微粒直径介于5.5-36 nm纳米级磁流体材料。其流程如下图所示:
下列说法错误的是( )
A、该分散系能产生丁达尔效应 B、取最后一次的洗涤液,加入氯化钡溶液,若无白色沉淀,证明沉淀已经洗涤干净 C、取溶液B加入KSCN溶液,溶液变为红色 D、FeSO4·7H2O和FeCl3·6H2O的物质的量之比最好为2∶120. 用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,记录实验据如下表:

①
②
气体体积/mL
溶液温度/℃
气体体积/mL
溶液温度/℃
0
0
22.0
0
22.0
8.5
30
24.8
50
23.8
10.5
50
26.0
-
-
下列说法错误的是( )
A、两个装置中反应均为Zn+H2SO4=ZnSO4+H2↑ B、0~8.5min内,生成气体的平均速率①<② C、时间相同时,对比两装置的溶液温度,说明反应释放的总能量①>② D、生成气体体积相同时,对比两装置的溶液温度,说明②中反应的化学能部分转化为电能二、综合题
-
21. 元素周期表是学习化学的重要工具。下表列出了①~⑩十种元素在周期表中的位置:
族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
二
①
②
三
③
④
⑤
⑥
⑦
⑧
四
⑨
⑩
请按要求回答下列问题:
(1)、元素⑦简单氢化物的化学式为。(2)、写出元素②③形成一种化合物,可在呼吸面具中作为氧气的来源,其电子式是。(3)、④、⑧、⑨三种元素的简单离子半径由大到小的顺序排列为(用元素符号表示)。(4)、元素⑥、⑦、⑧三种元素最高价氧化物对应水化物的酸性最强的为(用化学式表示)。(5)、向元素③的单质与水反应后的溶液中加入元素⑤的单质,发生反应的化学方程式为。22. 某校化学兴趣小组为研究的性质,设计如图所示装置进行实验。装置III中a为干燥的红色纸,b为湿润的红色纸。 (1)、装置I中仪器c的名称是 , 装置II的作用是 , 装置V盛放的药品是。(2)、实验室以二氧化锰和浓盐酸制备氯气的化学方程式为。(3)、实验过程中装置IV中的实验现象。(4)、实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,还需在装置II与之间添加下列装置(填序号)。
(1)、装置I中仪器c的名称是 , 装置II的作用是 , 装置V盛放的药品是。(2)、实验室以二氧化锰和浓盐酸制备氯气的化学方程式为。(3)、实验过程中装置IV中的实验现象。(4)、实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,还需在装置II与之间添加下列装置(填序号)。 (5)、该小组同学将制得的氯气配制成氯水,以探究的还原性。进行了如下实验:取一定量的溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
(5)、该小组同学将制得的氯气配制成氯水,以探究的还原性。进行了如下实验:取一定量的溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:假设1:被氧化
假设2:被氧化
请你完成下表,验证假设。
实验步骤
预期现象
结论
I.取少量黄色溶液于试管中,滴加几滴溶液
假设1正确
II.取少量黄色溶液于试管中,滴加几滴溶液
假设2正确
(6)、数字化实验是将传感器、数据采集和计算机连接起来,采集实验过程各变化数据。下图是用强光照射广口瓶中新制氯水时所获像,下列纵坐标代表的物理量与图像不相符的是____。 A、溶液的pH B、溶液中氢离子的浓度 C、瓶中氧气的体积分数 D、溶液的导电能力23.(1)、I.乙酸乙酯是一种重要的有机化工原料和工业溶剂,具有优异的溶解性、快干性,用途广泛。某乙酸乙酯的合成路线如下图I所示。已知A是石油化学工业重要的基本原料,相对分子质量为28;物质S是营养物质之一,米饭、馒头中都富含S,S在酸性条件下水解的最终产物是G。
A、溶液的pH B、溶液中氢离子的浓度 C、瓶中氧气的体积分数 D、溶液的导电能力23.(1)、I.乙酸乙酯是一种重要的有机化工原料和工业溶剂,具有优异的溶解性、快干性,用途广泛。某乙酸乙酯的合成路线如下图I所示。已知A是石油化学工业重要的基本原料,相对分子质量为28;物质S是营养物质之一,米饭、馒头中都富含S,S在酸性条件下水解的最终产物是G。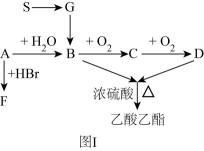

请回答下列问题:
G的名称是 , B的官能团名称为 , F的结构简式为。
(2)、下列有关B物质的性质与用途说法正确的是(填字母序号)。a.含75%的B溶液可用于杀菌消毒
b.钠与B反应生成 , 反应时钠块浮在B的上面
c.在酒精灯上灼烧后的铜丝立即插入B中,铜丝又变回亮红色
(3)、由B生成C的化学方程式为 , 反应类型是。(4)、若实验室利用如上图II装置制备乙酸乙酯,装置中溶液M为 , 球形干燥管的作用是。(5)、II.已知:乙酸乙酯在稀酸溶液中可水解。反应方程式为:某化学小组设计实验探究乙酸乙酯在不同温度、不同浓度稀硫酸中的水解速率。取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。
编号
①
②
③
温度/℃
50
50
75
乙酸乙酯/mL
3
稀溶液/mL
3
2
3
蒸馏水/mL
0
0
回答下列问题:
请完成上表,其中 , 。
(6)、实验①和实验探究温度对反应速率的影响;②试管中的酯层减少比①试管慢,说明。(7)、下列有关说法正确的是____。A、酯层体积不再改变时,说明反应停止 B、其它条件不变,将酯的用量增加1倍,则反应开始时速率提高1倍 C、时,说明反应达到平衡状态 D、时,反应达到平衡状态