山西省晋中市平遥县2022年5月中考二模化学试题
试卷更新日期:2022-07-29 类型:中考模拟
一、单选题
-
1. 化学的学习离不开实验,而实验成功的关键在于操作。下列实验操作正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、 量取5.5mL液体
C、
量取5.5mL液体
C、 过滤
D、
过滤
D、 稀释浓硫酸
2. “吃出营养、吃出健康”是人们普遍的饮食追求,下列说法错误的是( )A、人体缺乏维生素A会引起夜盲症 B、食用甲醛浸泡的食物会危害人体健康 C、不吃霉变或超过保质期的食物 D、微量元素对人体十分重要,必须大量服用3. 如图是几种微粒的结构示意图,根据图示判断以下说法错误的是( )
稀释浓硫酸
2. “吃出营养、吃出健康”是人们普遍的饮食追求,下列说法错误的是( )A、人体缺乏维生素A会引起夜盲症 B、食用甲醛浸泡的食物会危害人体健康 C、不吃霉变或超过保质期的食物 D、微量元素对人体十分重要,必须大量服用3. 如图是几种微粒的结构示意图,根据图示判断以下说法错误的是( ) A、B元素属于金属元素 B、A与C元素具有相似的化学性质 C、C原子在化学反应中容易失去两个电子形成阳离子 D、B,C,D元素位于同一周期4. 下列物质由分子构成的是( )A、氢氧化钾 B、铝 C、金刚石 D、水5. 中国政府承诺“努力争取2060年前实现碳中和”,“碳中和”是使碳排放与碳吸收达平衡,实现二氧化碳相对“零排放”。为了实现碳中和,从实际出发,以下措施不可行的是( )A、鼓励拼车或乘坐公共交通出行 B、推广垃圾分类处理,加强资源回收利用 C、禁止使用煤、石油等化石能源 D、采用物理或化学方法,捕集或吸收废气中的二氧化碳6. 下列各组离子在pH=13的溶液中能大量共存,且形成无色溶液的是( )A、K+、 、Na+、H+ B、 、K+、Cl-、 C、Na+、Ba2+、Fe3+、 D、Na+、Mg2+、Al3+、Cl-7. 分类是化学学科的基本思想方法之一。下列分类正确的是( )A、冰、干冰、氯酸钾属于氧化物 B、汞、钢、钛合金属于金属材料 C、煤、石油、氢气属于化石燃料 D、生石灰、熟石灰、石灰石属于碱8. 如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( )
A、B元素属于金属元素 B、A与C元素具有相似的化学性质 C、C原子在化学反应中容易失去两个电子形成阳离子 D、B,C,D元素位于同一周期4. 下列物质由分子构成的是( )A、氢氧化钾 B、铝 C、金刚石 D、水5. 中国政府承诺“努力争取2060年前实现碳中和”,“碳中和”是使碳排放与碳吸收达平衡,实现二氧化碳相对“零排放”。为了实现碳中和,从实际出发,以下措施不可行的是( )A、鼓励拼车或乘坐公共交通出行 B、推广垃圾分类处理,加强资源回收利用 C、禁止使用煤、石油等化石能源 D、采用物理或化学方法,捕集或吸收废气中的二氧化碳6. 下列各组离子在pH=13的溶液中能大量共存,且形成无色溶液的是( )A、K+、 、Na+、H+ B、 、K+、Cl-、 C、Na+、Ba2+、Fe3+、 D、Na+、Mg2+、Al3+、Cl-7. 分类是化学学科的基本思想方法之一。下列分类正确的是( )A、冰、干冰、氯酸钾属于氧化物 B、汞、钢、钛合金属于金属材料 C、煤、石油、氢气属于化石燃料 D、生石灰、熟石灰、石灰石属于碱8. 如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是( ) A、使a、c的饱和溶液析出晶体都可以采用降温结晶的方法 B、t1℃时,a、c两种物质的溶液溶质质量分数一定相等 C、t2℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:a>b>c D、在t2℃时,将30ga物质加入50g水中充分溶解,所得溶液质量为80g9. 为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )
A、使a、c的饱和溶液析出晶体都可以采用降温结晶的方法 B、t1℃时,a、c两种物质的溶液溶质质量分数一定相等 C、t2℃时,a、b、c三种物质的饱和溶液溶质质量分数由大到小的关系是:a>b>c D、在t2℃时,将30ga物质加入50g水中充分溶解,所得溶液质量为80g9. 为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )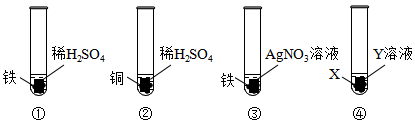 A、通过实验①、②,能验证金属活动性:Fe>Cu B、通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag C、实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu D、实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag10. 向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,下列说法错误的是( )
A、通过实验①、②,能验证金属活动性:Fe>Cu B、通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag C、实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu D、实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag10. 向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,下列说法错误的是( ) A、a点溶液中的pH<7 B、bc段(不含b、c点)反应的化学方程式为 C、c点溶液中含有两种溶质 D、整个变化过程中氯离子的数目没有改变
A、a点溶液中的pH<7 B、bc段(不含b、c点)反应的化学方程式为 C、c点溶液中含有两种溶质 D、整个变化过程中氯离子的数目没有改变二、填空题
-
11. 高铁已是我国的名片。结合如图所示信息回答问题。
 (1)、石墨作电刷通过电网给动车供电,说明它有良好的性。(2)、动车车身使用的材料中属于有机合成材料的是。(3)、动车车身表面防锈采用的方法是。(4)、制造铁轨的锰钢是一种铁合金,与纯铁相比,其硬度更(填“大”或“小”)。(5)、乘客小林的午餐有:红烧肉、米饭、青菜和矿泉水。
(1)、石墨作电刷通过电网给动车供电,说明它有良好的性。(2)、动车车身使用的材料中属于有机合成材料的是。(3)、动车车身表面防锈采用的方法是。(4)、制造铁轨的锰钢是一种铁合金,与纯铁相比,其硬度更(填“大”或“小”)。(5)、乘客小林的午餐有:红烧肉、米饭、青菜和矿泉水。①小林的午餐食品中富含维生素的是。
②空塑料矿泉水瓶应放入(填“可回收”或“不可回收”)垃圾箱中。
三、综合题
-
12. 利用催化剂可有效消除室内装修材料释放的有害气体甲醛(HCHO)。请根据下图写出反应的化学方程式。
 13. 氯化钠是日常生活的必需品,也是重要的化工原料。粗盐除了含氯化钠外,还含有少量MgCl2、CaCl2等杂质,以下是某校化学兴趣小组在实验室进行的粗盐提纯的实验操作流程。
13. 氯化钠是日常生活的必需品,也是重要的化工原料。粗盐除了含氯化钠外,还含有少量MgCl2、CaCl2等杂质,以下是某校化学兴趣小组在实验室进行的粗盐提纯的实验操作流程。 (1)、在实验室中搅拌用到的玻璃仪器是 , 在实验操作中它的作用是。(2)、“盐水精制Ⅰ”是除去盐水中的少量氯化镁,反应方程式。(3)、“盐水精制Ⅱ”是除去盐水中的杂质。(填化学式)。(4)、“加入适量盐酸”除去的杂质离子是(填离子符号)。(5)、最终得到食盐水要想得到固体食盐需进行操作。14. 纯净的臭氧(O3)在常温下是天蓝色的气体,有难闻的鱼腥臭味,不稳定,易转化为氧气。它虽然是空气质量播报中提及的大气污染物,但臭氧层中的臭氧能吸收紫外线,保护地面生物不受伤害。而且近年来臭氧的应用发展较快,很受人们的重视。
(1)、在实验室中搅拌用到的玻璃仪器是 , 在实验操作中它的作用是。(2)、“盐水精制Ⅰ”是除去盐水中的少量氯化镁,反应方程式。(3)、“盐水精制Ⅱ”是除去盐水中的杂质。(填化学式)。(4)、“加入适量盐酸”除去的杂质离子是(填离子符号)。(5)、最终得到食盐水要想得到固体食盐需进行操作。14. 纯净的臭氧(O3)在常温下是天蓝色的气体,有难闻的鱼腥臭味,不稳定,易转化为氧气。它虽然是空气质量播报中提及的大气污染物,但臭氧层中的臭氧能吸收紫外线,保护地面生物不受伤害。而且近年来臭氧的应用发展较快,很受人们的重视。生产中大量使用的臭氧通常由以下方法制得。

臭氧处理饮用水。早在19世纪中期的欧洲,臭氧已被用于饮用水处理。由于臭氧有强氧化性,可以与水中的有害化合物发生反应,处理效果好,不会产生异味。
臭氧作漂白剂。许多有机色素的分子遇臭氧后会被破坏,成为无色物质。因此,臭氧可作为漂白剂,用来漂白麻、棉、纸张等。实践证明,臭氧的漂白作用是氯气的15倍之多。
臭氧用于医用消毒。与传统的消毒剂氯气相比,臭氧有许多优点,如下表所示。
臭氧和氯气的消毒情况对比
消毒效果
消毒所需时间
(0.2mg/L)
二次污染
投资成本
(900m设备)
臭氧
可杀灭一切微生物,包括细菌、病毒、芽孢等
<5分钟
臭氧很快转化为氧气,无二次污染,高效环保
约45万元
氯气
能杀灭除芽孢以外的大多数微生物,对病毒作用弱
>30分钟
刺激皮肤,有难闻气味,对人体有害,有二次污染、残留,用后需大量水冲洗
约3至4万元
依据文章内容回答下列问题。
(1)、臭氧的相对分子质量为。(2)、臭氧处理饮用水时,利用了臭氧的(填“物理”或“化学”)性质。(3)、写出氧气转化为臭氧的化学方程式。(4)、为了快速杀灭病毒,应选择的消毒剂是。(5)、下列关于臭氧的说法中,错误的是____。A、臭氧的漂白作用比氯气强 B、工业上由氧气制得臭氧的过程中,既有物理变化也有化学变化 C、臭氧在生产生活中有很多用途,对人类有益无害 D、臭氧稳定性差,不利于储存,其应用可能会受到限制15. 下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种。 (1)、写出乙和丙的化学式:乙 , 丙。(2)、丁属于(物质类别)。(3)、图中反应①属于基本反应类型中的反应。(4)、写出下列化学方程式:甲和乙:。16. 根据下图回答有关问题:
(1)、写出乙和丙的化学式:乙 , 丙。(2)、丁属于(物质类别)。(3)、图中反应①属于基本反应类型中的反应。(4)、写出下列化学方程式:甲和乙:。16. 根据下图回答有关问题: (1)、仪器A的名称是。(2)、实验室制取并收集二氧化碳需在图中选用A、C、G与(填序号)组合;检验二氧化碳是否集满的方法是。(3)、实验室用该装置制取二氧化碳的化学方程式为。17. 某校化学兴趣小组甲、乙两组同学为探究氢氧化钙的化学性质,分别做了如下相同的四个实验:
(1)、仪器A的名称是。(2)、实验室制取并收集二氧化碳需在图中选用A、C、G与(填序号)组合;检验二氧化碳是否集满的方法是。(3)、实验室用该装置制取二氧化碳的化学方程式为。17. 某校化学兴趣小组甲、乙两组同学为探究氢氧化钙的化学性质,分别做了如下相同的四个实验:
请回答下列问题:
(1)、试管C中的现象是。(2)、以上实验中,能发生反应但无明显现象的化学方程式。(3)、【探究】实验结束后,甲、乙两组同学分别将本组A、B、C、D四支试管中的物质各倒入一个洁净的大烧杯中,充分反应后静置,发现:
①甲组烧杯底部有白色沉淀,上层清液为无色。则上层清液中一定含有的溶质是(指示剂除外)。
②乙组烧杯底部有白色沉淀,上层清液为红色,则上层清液中一定没有的离子是。
(4)、【拓展延伸】①做完实验后,甲、乙两组同学共同讨论总结了氢氧化钙的化学性质,进行了表达交流,最后得出结论,氢氧化钙能与类别的物质发生化学反应。
②甲、乙两组同学进一步分析,比较了氢氧化钙与氢氧化钠的化学性质,发现有非常相似的化学性质,从组成上原因是。
四、计算题
-
18. 今年疫情期间,小刚家买了一瓶里过氧化氢消毒液,使用时发现已开盖,标签如图所示。
产品名称:过氧化氢消毒液
主要成分:过氧化氢
……
过氧化氢含量:30~33gL
……
使用方法:用原液直接浸泡、擦拭消毒10分钟
他想利用所学化学知识测定其浓度是否还在商标所标范围内,于是他把该消毒液带到化学实验室,取10mL该消毒液于试管中,加入0.1g二氧化锰,充分反应,共收集到0.12g气体。
(1)、二氧化锰在该反应中起作用。(2)、请结合上图计算该过氧化氢消毒液的浓度是否在商标所标范围内。(写出计算过程)
-