内蒙古呼和浩特市回民区2022年中考模拟化学试题
试卷更新日期:2022-07-29 类型:中考模拟
一、单选题
-
1. 下列有关物质的性质与用途对应关系正确的是( )A、石墨质软,可用作电池电极 B、不锈钢硬度较大,可用于制作医疗器械 C、液态氧气具有助燃性,用作火箭推进燃料 D、固体氢氧化钠具有潮解性,可用作气体干燥剂2. 2021年3月20日三星堆遗址考古工作中发现了生锈的铜器,已知铜锈的成分为碱式碳酸铜[Cu2(OH)aCO3]。经查阅资料可知铜元素在元素周期表中有如图所示的信息,下列说法正确的是( )
 A、乙图中x的值可能为2 B、铜原子的中子数为29 C、碱式碳酸铜[Cu2(OH)aCO3]中a为2 D、铜为活泼金属,能与稀硫酸发生置换反应3. 空气和水都是人类宝贵的自然资源。下列说法中正确的是( )A、空气中的氧气的质量分数为21% B、空气质量指数越大空气质量级别越高 C、自来水厂生成时投入明矾进行消毒 D、硬水是含有可溶性钙、镁化合物的水,软水不含可溶性钙、镁化合物4. 下列化学用语书写正确的是( )A、氦气:He2 B、硝酸铵中-3价氮元素: C、N2:两个氮原子 D、2个亚铁离子:2Fe3+5. 有关物质的组成、构成与性质关系的说法错误的是( )A、构成一氧化碳和二氧化碳分子不同,所以它们的化学性质不同 B、稀硝酸和稀醋酸中都含有氢离子,所以它们都能与碳酸钙反应生成CO2 C、构成金刚石和石墨烯的原子相同但是排列方式不同,所以它们的性质差异很大 D、组成氧气和臭氧的元素相同,但是它们的性质不同6. 在宏观、微观和化学符号之间建立联系是化学学科的特点。工业上生成化肥尿素[CO(NH2)2]的反应微观示意图如下,下列说法错误的是( )
A、乙图中x的值可能为2 B、铜原子的中子数为29 C、碱式碳酸铜[Cu2(OH)aCO3]中a为2 D、铜为活泼金属,能与稀硫酸发生置换反应3. 空气和水都是人类宝贵的自然资源。下列说法中正确的是( )A、空气中的氧气的质量分数为21% B、空气质量指数越大空气质量级别越高 C、自来水厂生成时投入明矾进行消毒 D、硬水是含有可溶性钙、镁化合物的水,软水不含可溶性钙、镁化合物4. 下列化学用语书写正确的是( )A、氦气:He2 B、硝酸铵中-3价氮元素: C、N2:两个氮原子 D、2个亚铁离子:2Fe3+5. 有关物质的组成、构成与性质关系的说法错误的是( )A、构成一氧化碳和二氧化碳分子不同,所以它们的化学性质不同 B、稀硝酸和稀醋酸中都含有氢离子,所以它们都能与碳酸钙反应生成CO2 C、构成金刚石和石墨烯的原子相同但是排列方式不同,所以它们的性质差异很大 D、组成氧气和臭氧的元素相同,但是它们的性质不同6. 在宏观、微观和化学符号之间建立联系是化学学科的特点。工业上生成化肥尿素[CO(NH2)2]的反应微观示意图如下,下列说法错误的是( ) A、从反应原理看:反应方程式为2NH3+CO2CO(NH2)2+H2O B、从微观构成看:该反应中物质均由分子构成 C、从物质类别看:该反应只涉及一种氧化物 D、从守恒观点看:生成物质的质量比为10:37. 下列实验方案合理的是( )
A、从反应原理看:反应方程式为2NH3+CO2CO(NH2)2+H2O B、从微观构成看:该反应中物质均由分子构成 C、从物质类别看:该反应只涉及一种氧化物 D、从守恒观点看:生成物质的质量比为10:37. 下列实验方案合理的是( )选项
实验目的
所用试剂或操作方法
A
鉴别NaOH、CaCO3、NH4NO3三种白色固体
分别取样与试管中,加入适量水,搅拌
B
提纯混有少量KNO3的NaCl
高温溶解、冷却结晶、过滤
C
鉴别溶液:氯化钡溶液、氢氧化钠溶液、硫酸钠溶液、氯化铵溶液
不用其它试剂,将四种溶液分别取样,两两相互滴加,观察现象
D
除去NaCl溶液中混有的少量Na2CO3
加过量CaCl2溶液,过滤
A、A B、B C、C D、D8. 称取m g (相对分子质量为146,其中氧元素的化合价为-2)置于氮气流中加热残留固体质量随温度的变化如图所示(图中各点对应固体均为纯净物),其中发生反应:。下列说法正确的是( )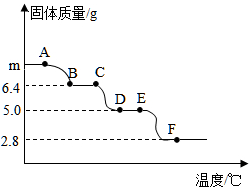 A、中碳元素的化合价为+2 B、 C、发生反应的化学方程式为 D、F点对应固体的化学式为9. 下列四个图像能正确反映对应变化关系是( )A、
A、中碳元素的化合价为+2 B、 C、发生反应的化学方程式为 D、F点对应固体的化学式为9. 下列四个图像能正确反映对应变化关系是( )A、 向AgNO3和Cu(NO3)2中混合溶液中加入锌粉至过量
B、
向AgNO3和Cu(NO3)2中混合溶液中加入锌粉至过量
B、 常温时向一定量的Ca(OH)2溶液中通入CO2至过量
C、
常温时向一定量的Ca(OH)2溶液中通入CO2至过量
C、 向一定质量的氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸至过量
D、
向一定质量的氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸至过量
D、 向等质量、溶质质量分数相同的稀盐酸中分别逐渐加入镁粉和铁粉至过量
10. 孔雀石是冶炼金属铜的主要原料,其主要成分是Cu2(OH)2CO3[可以看成是Cu(OH)2、CuCO3],还含有少量氧化铁和二氧化硅(不溶于水,也不与酸反应),以下为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。
向等质量、溶质质量分数相同的稀盐酸中分别逐渐加入镁粉和铁粉至过量
10. 孔雀石是冶炼金属铜的主要原料,其主要成分是Cu2(OH)2CO3[可以看成是Cu(OH)2、CuCO3],还含有少量氧化铁和二氧化硅(不溶于水,也不与酸反应),以下为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。
【查阅资料】
①Cu2(OH)2CO3与盐酸反应生成氯化铜、水和二氧化碳。
②铁能与氯化铁溶液反应,化学方程式为2FeCl3+Fe=3FeCl2
③氢氧化亚铁易被氧气氧化,化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3下列说法错误的是( )
A、实验室在获取NaCl晶体的操作Y中,使用的仪器有铁架台、玻璃棒、酒精灯、蒸发皿 B、盐酸与Cu2(OH)2CO3反应的方程式为Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑ C、在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有3个 D、滤液Ⅱ的溶质为FeCl2;试剂X是稀盐酸二、填空题
-
11. 化学与我们的生活息息相关。请用相关化学知识填空。(1)、广泛使用的清洁能源是;(填化学式)(2)、用于烘焙面包、糕点的盐是;(填化学式)12. 甲、乙、丙三种物质的溶解度曲线如图所示。回答下列问题
 (1)、当温度为℃时,甲、丙两种物质的溶解度相等。(2)、t3℃时甲物质的饱和溶液中,溶质和溶液的质量比为。(3)、若采用降温、恒温蒸发溶剂、加溶质的方法都能使接近饱和的溶液变成饱和溶液,则该物质是。(4)、R是甲、乙、丙三种物质中的一种,现用R做如图Ⅱ所示实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下几种说法正确的是____(填字母序号)。
(1)、当温度为℃时,甲、丙两种物质的溶解度相等。(2)、t3℃时甲物质的饱和溶液中,溶质和溶液的质量比为。(3)、若采用降温、恒温蒸发溶剂、加溶质的方法都能使接近饱和的溶液变成饱和溶液,则该物质是。(4)、R是甲、乙、丙三种物质中的一种,现用R做如图Ⅱ所示实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下几种说法正确的是____(填字母序号)。 A、R是甲物质 B、①和②的溶液中,溶质质量相等 C、①②③中,只有③的上层清液是饱和溶液 D、①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小13. 如图是人们经常使用的便捷交通工具—自行车。请回答下列问题。
A、R是甲物质 B、①和②的溶液中,溶质质量相等 C、①②③中,只有③的上层清液是饱和溶液 D、①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小13. 如图是人们经常使用的便捷交通工具—自行车。请回答下列问题。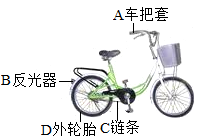 (1)、所标各部件中由金属材料制成的是(填字母)。(2)、生铁和钢都是铁的合金,其性能不同的原因是。(3)、向AgNO3溶液中加入一定量的锌和铜的混合粉末,充分反应后过滤,滤液呈蓝色,则滤出的固体中一定含有(填化学式),滤液中一定含有的金属离子是(写离子符号)。
(1)、所标各部件中由金属材料制成的是(填字母)。(2)、生铁和钢都是铁的合金,其性能不同的原因是。(3)、向AgNO3溶液中加入一定量的锌和铜的混合粉末,充分反应后过滤,滤液呈蓝色,则滤出的固体中一定含有(填化学式),滤液中一定含有的金属离子是(写离子符号)。三、综合题
-
14. 某白色粉末可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种,某科学兴趣小组为探究其成分,设计了如下实验流程。(所加试剂均足量)
 (1)、操作Ⅰ、Ⅱ的名称是。(2)、灼烧时发生反应的化学方程式是 , 得到无色气体的质量为g。(3)、固体甲的成分是(填化学式),该白色粉末中一定不含有(填化学式)。(4)、白色粉末中肯定含有的物质的总质量为g。15. 实验室制取气体时所需的一些装置如下图所示,请回答下列问题。
(1)、操作Ⅰ、Ⅱ的名称是。(2)、灼烧时发生反应的化学方程式是 , 得到无色气体的质量为g。(3)、固体甲的成分是(填化学式),该白色粉末中一定不含有(填化学式)。(4)、白色粉末中肯定含有的物质的总质量为g。15. 实验室制取气体时所需的一些装置如下图所示,请回答下列问题。 (1)、上图中仪器a的名称是。(2)、用大理石和稀盐酸制二氧化碳,发生反应的化学方程式为 , 收集二氧化碳的装置为(填字母)。(3)、加热氯酸钾和二氧化锰的固体混合物制取氧气,并对氯酸钾完全分解后的残留固体进行分离。
(1)、上图中仪器a的名称是。(2)、用大理石和稀盐酸制二氧化碳,发生反应的化学方程式为 , 收集二氧化碳的装置为(填字母)。(3)、加热氯酸钾和二氧化锰的固体混合物制取氧气,并对氯酸钾完全分解后的残留固体进行分离。①发生装置应选用(填字母)。
②KCl的溶解度曲线如下图所示。将反应后的残余固体冷却至室温,加足量水溶解后过滤,滤渣经处理得到MnO2。从滤液中获得KCl晶体的最佳方法是。
 16. 某校化学兴趣小组在探究“酸、碱、盐的化学性质时,做了如图甲的所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图乙所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。
16. 某校化学兴趣小组在探究“酸、碱、盐的化学性质时,做了如图甲的所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图乙所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。
【查阅资料】Na2SO4、NaCl溶液呈中性
(1)、【猜想与假设】猜想Ⅰ NaCl、Na2SO4
猜想Ⅱ NaCl、Na2SO4和。
猜想Ⅲ NaCl、Na2SO4和H2SO4
猜想Ⅳ NaCl、Na2SO4、H2SO4、Na2CO3
(2)、【交流讨论】小强同学认为猜想Ⅳ一定是错误的,他的理由是(用化学方程式示)。(3)、【进行实验】小明同学设计如下两个实验方案。实验步骤
实验现象
实验结论
方案一
取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液
猜想Ⅲ正确
方案二
取少量烧杯中的溶液于洁净的试管中,加入少量铁粉
【反思与总结】分析反应后溶液中溶质成分除要考虑生成物,还需考虑反应物是否过量。
四、计算题
-
17. 某课外兴趣小组同学取一定量含铜粉的氧化铜粉末,放入烧杯中,加入192g稀硫酸,搅拌,恰好完全反应后过滤(损耗忽略不计),烧杯中固体的质量随时间变化情况如图所示:
 (1)、所取粉末中氧化铜的质量为g;(2)、计算反应后所得溶液溶质质量分数。(规范写出计算过程)
(1)、所取粉末中氧化铜的质量为g;(2)、计算反应后所得溶液溶质质量分数。(规范写出计算过程)