辽宁省沈阳市大东区2022年中考二模化学试题
试卷更新日期:2022-07-29 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、水汽化 B、水沸腾 C、水分解 D、水结冰2. 多年前,沈阳市已经禁止使用含铅汽油,主要是为了( )A、提高汽油燃烧效率 B、减少铅资源损耗 C、降低汽油成本 D、减少环境污染3. 人体中化学元素含量的多少会直接影响人体健康。下列元素中,摄入过少会引起骨质疏松的是( )A、铁 B、锌 C、钙 D、硒4. 垃圾是放错地方的资源。下列物质属于可回收垃圾的是( )A、旧报纸 B、口香糖 C、过期药物 D、烂菜叶5. 下列物质中属于纯净物的是( )A、石油 B、氮气 C、煤 D、啤酒6. Fe3O4的化学名称是( )A、三铁化四氧 B、氧四化铁三 C、四氧化三铁 D、铁三化氧四7. 规范的实验操作是保证实验成功的关键。下列实验操作正确的是( )A、
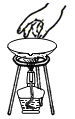 移走蒸发皿
B、
移走蒸发皿
B、 称量固体药品
C、
称量固体药品
C、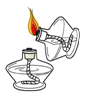 点燃酒精灯
D、
点燃酒精灯
D、 检查装置气密性
8. 在自来水生产过程中,能用于除去水中色素和异味的物质或操作是( )A、明矾 B、活性炭 C、沉淀 D、消毒9. 洗涤在生活中随处可见。下列做法中利乳化原理的是( )A、用稀盐酸清洗铁板表面的铁锈 B、用酒精洗去衣物上沾有的碘 C、用洗洁精洗去餐具上的油污 D、用水冲洗水果盘上的残渣10. 下列物质属于无机化合物的是( )A、硝酸(HNO3) B、乙炔(C2H2) C、淀粉【(C6H10O5)n】 D、尿素【CO(NH2)2】11. 下列各组混合物能用过滤方法分离的是( )A、氩气和氦气 B、蔗糖和沙子 C、食盐和水 D、木炭粉和氧化铜12. 下列生活生产中的做法,利用中和反应原理的是( )A、用含Al(OH)3的药物治疗胃酸过多 B、利用生石灰与水反应放热煮鸡蛋 C、用石灰浆吸收SO2防治酸雨 D、用干冰制造舞台云雾13. 下图表示了氯化钠的形成过程,下列叙述中错误的是( )
检查装置气密性
8. 在自来水生产过程中,能用于除去水中色素和异味的物质或操作是( )A、明矾 B、活性炭 C、沉淀 D、消毒9. 洗涤在生活中随处可见。下列做法中利乳化原理的是( )A、用稀盐酸清洗铁板表面的铁锈 B、用酒精洗去衣物上沾有的碘 C、用洗洁精洗去餐具上的油污 D、用水冲洗水果盘上的残渣10. 下列物质属于无机化合物的是( )A、硝酸(HNO3) B、乙炔(C2H2) C、淀粉【(C6H10O5)n】 D、尿素【CO(NH2)2】11. 下列各组混合物能用过滤方法分离的是( )A、氩气和氦气 B、蔗糖和沙子 C、食盐和水 D、木炭粉和氧化铜12. 下列生活生产中的做法,利用中和反应原理的是( )A、用含Al(OH)3的药物治疗胃酸过多 B、利用生石灰与水反应放热煮鸡蛋 C、用石灰浆吸收SO2防治酸雨 D、用干冰制造舞台云雾13. 下图表示了氯化钠的形成过程,下列叙述中错误的是( ) A、在该反应中,电子起到了重要作用 B、钠离子与钠原子的化学性质不同 C、氯化钠是由钠原子和氯原子构成的 D、反应中,钠原子的电子层数发生改变
A、在该反应中,电子起到了重要作用 B、钠离子与钠原子的化学性质不同 C、氯化钠是由钠原子和氯原子构成的 D、反应中,钠原子的电子层数发生改变二、填空题
-
14. 2022年新冠疫情期间,沈阳市政府想方设法满足市民对肉、蛋、奶、鱼、菜、果等生活物资的消费需求,确保市民将更多精力投入疫情防控中。(1)、下列食物中富含糖类的是____(填序号)。A、青菜 B、猪肉 C、牛奶 D、大米(2)、柑橘是一类美味的水果。
①将柑橘凑近鼻子,能闻到阵阵香气。用微粒观点解释原因。
②柑橘中富含维生素C(C6H8O6),维生素C由种元素组成。
③柑橘适宜生长在pH为6.0~6.5的土壤中,这种土壤显(填“酸”、“碱”或“中”)性。可用于测量土壤pH的实验用品是。
A.石蕊试剂 B.pH试纸 C.酚酞试剂
(3)、天然气是常用燃料。它属于(填“可再生”或“不可再生”)能源。15. 合理施肥可以增加农作物的产量、改善农产品的品质,让中国人的饭碗主要装上中国粮。“侯氏制碱法”以饱和食盐水、氨气、CO2等物质为原料同时生产纯碱和氯化铵两种产品。(1)、氯化铵(NH4Cl)是一种常用的(填“氮”、“磷”或“钾”)肥。(2)、下图为“侯氏制碱法”的原料NaCl和产品NH4Cl的溶解度曲线。
回答有关问题:
①30℃时,NaCl的溶解度约是。工业上在此温度下,将12t固体NaCl加入20t水中,充分溶解,形成的溶液是(填“饱和”或“不饱和”)溶液。
②NH4Cl溶解度随温度变化的趋势是。
③将饱和食盐水的温度提高,能继续溶解氯化钠,溶液中溶质的质量分数也会提高,有利于提高反应速率。而实际生产中往往在常温下进行,原因可能是。
④“侯氏制碱法”制得的NH4Cl中会混有少量的NaCl,根据上图分析,提纯NH4Cl可采取的方法为。
(3)、实验室有三种化肥:KCl、K2CO3与NH4Cl,因保存不当,标签脱落。某同学想鉴别它们,将三种固体编号为A、B、C,进行实验:①分别取A、B、C三种样品于研钵,各加入少量熟石灰,研磨。A、B样品无明显变化,C样品有刺激性气味产生。C为。
②取无现象的两个研钵中的固体于两支试管中,加入稀盐酸进行鉴别。用化学方程式表示鉴别依据的原理。
三、综合题
-
16. 化学是以实验为基础的科学。完成以下实验中的问题:
 (1)、图A实验得出的结论:氧气约占空气体积的。红磷燃烧的化学方程式为。(2)、图B实验可得出燃烧需要满足的条件是。(3)、图C实验中,对比(填序号),能证明铁生锈与水有关。(4)、图D实验的现象是 , 说明CO2具有的化学性质为。(5)、化学实验可按其主要目的分为:物质发生化学反应条件的探究,物质性质探究,物质含量的探究等。据此,上述实验中的(填序号)可以归为一类。17. 下图是实验室制取气体的常用装置,请回答有关问题:
(1)、图A实验得出的结论:氧气约占空气体积的。红磷燃烧的化学方程式为。(2)、图B实验可得出燃烧需要满足的条件是。(3)、图C实验中,对比(填序号),能证明铁生锈与水有关。(4)、图D实验的现象是 , 说明CO2具有的化学性质为。(5)、化学实验可按其主要目的分为:物质发生化学反应条件的探究,物质性质探究,物质含量的探究等。据此,上述实验中的(填序号)可以归为一类。17. 下图是实验室制取气体的常用装置,请回答有关问题: (1)、写出标号仪器的名称:a。(2)、写出一种用A装置制备氧气的化学方程式。实验开始时,用酒精灯对药品直接加热,可能造成的后果是。(3)、若用排空气法收集干燥的氧气,要将气体通过浓硫酸,仪器的连接顺序为A→(填序号),验满的方法为。(4)、实验室在B装置中用过氧化氢溶液制取氧气,反应的化学方程式为。用C装置收集氧气的最佳时机是。18. 金属材料的发展促进了人类社会的文明进步,回答下列有关金属的问题:(1)、下列金属制品的用途,利用导电性的是____。A、
(1)、写出标号仪器的名称:a。(2)、写出一种用A装置制备氧气的化学方程式。实验开始时,用酒精灯对药品直接加热,可能造成的后果是。(3)、若用排空气法收集干燥的氧气,要将气体通过浓硫酸,仪器的连接顺序为A→(填序号),验满的方法为。(4)、实验室在B装置中用过氧化氢溶液制取氧气,反应的化学方程式为。用C装置收集氧气的最佳时机是。18. 金属材料的发展促进了人类社会的文明进步,回答下列有关金属的问题:(1)、下列金属制品的用途,利用导电性的是____。A、 铁锅
B、
铁锅
B、 铜导线
C、
铜导线
C、 铝箔
D、
铝箔
D、 黄金首饰
(2)、高炉炼铁的原料有铁矿石、焦炭、石灰石和空气等。生产原理简要表示如图:
黄金首饰
(2)、高炉炼铁的原料有铁矿石、焦炭、石灰石和空气等。生产原理简要表示如图:
①图1中,反应I的基本反应类型是反应。
②反应Ⅲ将铁矿石的主要成分Fe2O3转化成Fe,铁元素化合价变化为。反应的化学方程式为。
③石灰石既能使SiO2转变成炉渣,同时还能提高生铁的单位时间内产量。分析加入石灰石能提高生铁产率的原因。
④图2中,利用铁水和炉渣(填物理性质)不同,两者通过不同高度的出口实现分离。
 (3)、金属的应用与金属活动性密切相关。任选试剂,设计可行的实验方案探究锌、铜的金属活动性强弱。实验方案(写出实验操作、现象及结论)。19. 家庭厨房或卫生间的管道经常堵塞,管道疏通剂能很好地解决这些烦恼。某化学研究小组购买了某品牌固态管道疏通剂进行探究。
(3)、金属的应用与金属活动性密切相关。任选试剂,设计可行的实验方案探究锌、铜的金属活动性强弱。实验方案(写出实验操作、现象及结论)。19. 家庭厨房或卫生间的管道经常堵塞,管道疏通剂能很好地解决这些烦恼。某化学研究小组购买了某品牌固态管道疏通剂进行探究。资料:固态管道疏通剂主要成分为NaOH、铝粉和缓蚀阻垢剂。
(1)、实验一:验证管道疏通剂疏通效果在实验室里,同学们取出一定量管道疏通剂,放入盛有水、毛发、脂肪的管中(如图),观察到反应剧烈,有大量气泡产生,管壁发烫,堵塞物被赶出,落入废液杯中。
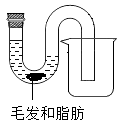
①同学们对管壁发烫的原因,提出两种猜想:一、反应放出热量;二、。
②甲同学查阅资料得知反应原理。请配平反应原理的化学方程式:2Al+2NaOH+2H2O=NaAlO2+3H2↑。
③乙同学对上述反应生成氢气的原因提出猜想:Al是活泼金属,所以能置换出NaOH中的“H”。大家认为他的观点不正确,原因是。
(2)、实验二:测定管道疏通剂中铝粉的质量分数取20g样品倒入烧杯中,然后加入200g水,直到没有固体剩余,称量剩余物质总质量为219.4g。
①反应生成氢气的质量为g。
②样品中铝粉的质量分数为。
(3)、拓展探究:同学们猜想Ca(OH)2也能制管道疏通剂,通过查阅资料了解到Ca(OH)2溶液能发生反应:。在老师的帮助下进行以下探究:
实验三:按表中数据将药品混合均匀后,分别加入20mL水,观察到有大量气泡产生,测量反应前后温度的变化(温度升高值越大,疏通效果越好)。实验数据如下:
序号
Ca(OH)2质量/g
铝粉质量/g
缓蚀阻垢剂质量/g
混合前后温度升高/℃
①
1.3
0.55
0.18
63
②
1.3
0.75
0.18
78
③
1.3
0.95
0.18
89
④
1.3
1.15
0.18
83
同学们提出猜想的依据:Ca(OH)2、NaOH两种溶液中含有相同的(写微粒符号),它们的化学性质相似。
(4)、分析上述实验,同学们认为Ca(OH)2能制管道疏通剂。他们得出结论的依据是。(5)、上述实验的另一个目的是探究。(6)、实验中,Ca(OH)2、铝粉的质量比为时疏通效果最好。对于缓蚀阻垢剂用量对疏通效果的影响,能否用Ca(OH)2代替NaOH制管道疏通剂,同学们认为还需继续查找资料、进一步开展探究。