辽宁省锦州市黑山县2022年中考一模化学试题
试卷更新日期:2022-07-29 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、甘蔗榨汁 B、自行车胎爆裂 C、炭包吸附异味 D、鲜奶制成酸奶2. 下列图示操作正确的是( )A、
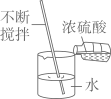 浓硫酸的稀释
B、
浓硫酸的稀释
B、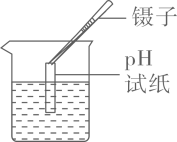 测溶液的pH
C、
测溶液的pH
C、 倾倒液体
D、
倾倒液体
D、 取用固体药品
3. 2019年3月23是第59个世界气象日,今年世界气象日的主旨是呼吁大家关注气候变化,合理利用资源,以下做法错误的是( )A、美团、网购等包装用品分类回收,综合利用 B、用LED灯作为光源照明,少用空调,温控适度 C、推广网络学习和无纸化办公 D、过期食品因为含碳,一律焚烧处理4. 夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,从化学角度分析,喷水的目的是( )A、降低养殖池内水的温度 B、增大与空气的接触面积,便于氧气溶解 C、增加观赏性 D、便于太阳照射,杀灭水中的病菌5. 面对美国的极限施压,华为“备胎芯片”全部转正,汽车上的备胎也是应对不时之需,汽车备胎中的橡胶与下表中的哪项材料类别相同( )
取用固体药品
3. 2019年3月23是第59个世界气象日,今年世界气象日的主旨是呼吁大家关注气候变化,合理利用资源,以下做法错误的是( )A、美团、网购等包装用品分类回收,综合利用 B、用LED灯作为光源照明,少用空调,温控适度 C、推广网络学习和无纸化办公 D、过期食品因为含碳,一律焚烧处理4. 夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,从化学角度分析,喷水的目的是( )A、降低养殖池内水的温度 B、增大与空气的接触面积,便于氧气溶解 C、增加观赏性 D、便于太阳照射,杀灭水中的病菌5. 面对美国的极限施压,华为“备胎芯片”全部转正,汽车上的备胎也是应对不时之需,汽车备胎中的橡胶与下表中的哪项材料类别相同( )A
B
C
D
黄铜
不锈钢
棉花
羊毛
塑料
合成纤维
玻璃钢
钢筋混凝土
A、A B、B C、C D、D6. 近期发生的火灾和爆炸事件给人们敲响了安全警钟,下列说法或做法错误的是( )A、对发生的火灾,首先要尝试用水扑灭,同时考虑其它办法 B、只要控制好燃烧和爆炸的条件,就能使之为我所用,造福人类 C、加油站、加气站内拨打电话可能引发燃烧或爆炸 D、明火附近避免喷洒空气清新剂或杀虫剂,以免引发火灾7. 对下列事实的解释错误的是( )事实
解释
A
五月槐花香浓郁,六月荷塘清久远
分子是不断运动的;不同分子性质不同
B
家中绿植枝叶生长不茂盛,叶色淡黄
缺少氮肥
C
用洗洁精洗去餐盘上的油渍
洗洁精能溶解油渍
D
常用醋酸或盐酸除水垢
醋酸和盐酸中均含有H+
A、A B、B C、C D、D8. 近期,草地贪夜蛾虫害严重威胁我国玉米产区,农药甲维盐对其有较好的防治作用。已知甲维盐的化学式为C56H81NO15 , 下列有关说法错误的是( )A、甲维盐由56个碳原子、81个氢原子、1个氮原子和15个氧原子构成 B、甲维盐中氮、氧两种元素的质量比为7:120 C、甲维盐中碳元素的质量分数最大 D、尽量避免过量施用农药9. 如图为金刚、石墨和C60的结构模型图,图中小球代表碳原子。下列说法错误的是( ) A、原子的排列方式改变,则构成的物质种类改变 B、相同元素组成的不同物质,在足量的氧气中完全燃烧,产物相同 C、相同元素组成的不同物质,化学性质相同 D、在特定的条件下,石墨既可转化为金刚石,也可转化为C6010. “宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法错误的是( )
A、原子的排列方式改变,则构成的物质种类改变 B、相同元素组成的不同物质,在足量的氧气中完全燃烧,产物相同 C、相同元素组成的不同物质,化学性质相同 D、在特定的条件下,石墨既可转化为金刚石,也可转化为C6010. “宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法错误的是( ) A、从反应价值看:该反应能获取清洁能源,延缓温室效应 B、从物质分类看:该反应涉及到2种氧化物 C、从微观构成看:四种物质均由分子构成 D、从表示方法看:该反应的化学方程式为2CO2+4H2O 2CH4+4O2
A、从反应价值看:该反应能获取清洁能源,延缓温室效应 B、从物质分类看:该反应涉及到2种氧化物 C、从微观构成看:四种物质均由分子构成 D、从表示方法看:该反应的化学方程式为2CO2+4H2O 2CH4+4O2二、填空题
-
11. 用化学用语填空。(1)、2个氩原子;(2)、锌元素;(3)、3个三氧化硫分子12. 如图中A是碘元素在元素周期表中的信息,B﹣E是四种粒子的结构示意图。 请回答。
 (1)、碘的相对原子质量是; B是碘原子的结构示意图,碘离子的符号为。(2)、B~E四种粒子中,属于同种元素的粒子是(填字母,下同),化学性质相似的粒子是。13. 水是生命之源,我们应该了解水及溶液的相关知识。(1)、生活中可用区分硬水和软水。(2)、净水时,利用活性炭的性除 去水中的色素和异味。(3)、下面是氯化钠和硝酸钾在不同温度的溶解度,请回答:
(1)、碘的相对原子质量是; B是碘原子的结构示意图,碘离子的符号为。(2)、B~E四种粒子中,属于同种元素的粒子是(填字母,下同),化学性质相似的粒子是。13. 水是生命之源,我们应该了解水及溶液的相关知识。(1)、生活中可用区分硬水和软水。(2)、净水时,利用活性炭的性除 去水中的色素和异味。(3)、下面是氯化钠和硝酸钾在不同温度的溶解度,请回答:温度/℃
10
20
30
40
50
60
溶解度/g
NaCl
35.8
36.0
36.3
36.6
37.0
37.3
KNO3
20.9
31.6
45.8
63.9
85.5
110
若NaCl中混有少量的KNO3 , 提纯NaCl的方法是。
14. 化学源于生活,生活中蕴含着许多化学知识。营养成分
蛋白质
脂肪
糖类
钠
钙
质量
3.2g
3.6g
11.9g
60mg
80mg
(1)、大枣含有蛋白质、糖类及维生素等营养素,其中起到调节人体新陈代谢、预防疾病作用的是。(2)、用锅盖盖灭着火的油锅,其灭火原理为。15. 能源紧缺、环境污染等是人类面临的重大问题。(1)、三大化石燃料包括煤、、天然气,其中天然气是比较清洁的能源,其燃烧的化学方程式。(2)、燃烧含硫化石燃料会产生二氧化硫,大量二氧化硫释放到空气中,会导雨水的pH(填“高于”或“低于”)正常值,形成酸雨。16. 钢铁是使用最多的金属材料。(1)、人类向自然界提取量最大的金属是铁,高炉炼铁的原料是铁矿石、空气、石灰石和焦炭。其中焦炭的作用。(2)、铝的活动性比铁强,但在生活中常在铁的表面涂上铝粉。其原因是。(3)、金属钴(Co)与铁具有相似的化学性质。CoCl2固体是蓝色的,CoCl2溶液是粉红色的。现将金属钴投入稀盐酸中,发生化学反应Co + 2HCl = CoCl2 + H2↑。该反应的实验现象为。三、综合题
-
17. 消毒与清洁对公共场所和家庭是至关重要的。(1)、二氧化氯(ClO2)可作水处理消毒剂,二氧化氯中氯元素的化合价是。(2)、“洁则灵”与“漂白剂”不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为。(3)、用炉具清洁剂(含有NaOH)清洗炉具时,应避免接触皮肤,其原因是。(4)、使用洗洁剂清洗餐具上的油污时,利用了洗涤剂对油污的作用。18. A、B、C、D、E五种物质均为初中化学中所涉及的常见物质,它们存在如下图的转化关系,“→”表示可以向箭头所指方向一步转化,弧线表示两种物质间可以发生反应,C是常见气体,D是常见单质,(反应条件与其他物质均已略去)。请回答下列问题:
 (1)、若A在常温下为液体,则C的化学式为;(2)、若A在常温下为气体,则C的化学式为;(3)、无论A在常温下为液体还是气体,B的化学式均为 , D的化学式为;(4)、写出E→A的化学方程式。19. 碳酸钡是工业上一种重要的化工产品,以下是某工厂用含二氧化硅杂质的碳酸钡原料来生产碳酸钡的工艺流程,请你根据流程回答下列问题(说明:操作B为洗涤,干燥)
(1)、若A在常温下为液体,则C的化学式为;(2)、若A在常温下为气体,则C的化学式为;(3)、无论A在常温下为液体还是气体,B的化学式均为 , D的化学式为;(4)、写出E→A的化学方程式。19. 碳酸钡是工业上一种重要的化工产品,以下是某工厂用含二氧化硅杂质的碳酸钡原料来生产碳酸钡的工艺流程,请你根据流程回答下列问题(说明:操作B为洗涤,干燥) (1)、生产流程中为节约成本,生成的气体B直接应用于流程中,其气体B是。(2)、操作A的名称为。(3)、流程中溶液A中含有的溶质有(写化学式)。(4)、写出反应室中有关反应的化学方程式(任意一个即可)。(5)、写出电解氯化钠溶液的化学方程式。20. 小英同学从资料中得知:质量守恒定律的发现经历了漫长、曲折的过程。(1)、【实验回顾】
(1)、生产流程中为节约成本,生成的气体B直接应用于流程中,其气体B是。(2)、操作A的名称为。(3)、流程中溶液A中含有的溶质有(写化学式)。(4)、写出反应室中有关反应的化学方程式(任意一个即可)。(5)、写出电解氯化钠溶液的化学方程式。20. 小英同学从资料中得知:质量守恒定律的发现经历了漫长、曲折的过程。(1)、【实验回顾】1756年,俄国化学家罗蒙诺索素夫将金属锡放在密闭容器里煅烧,冷却后在密闭容器里称量,发现总质量和煅烧前没有变化。
1774年,拉瓦锡将45.0份质量的氧化汞加热分解,恰好得到了41.5份质量的汞和3.5份质量的氧气,得到了与罗蒙诺索夫相同的结论,拉瓦锡还通过这个实验研究了 , 成就了化学史上的另一经典实验。
(2)、【实验重现】小英同学在老师的指导下,将铁粉、活性炭粉、食盐按一定比例加水混合后,涂在用铁片折成的连续的Z形架表面,然后放入盛满氧气的集气瓶中。通过如图所示装置对“化学反应中,反应物与生成物的质量关系”进行实验探究,实验过程中做到操作规范,准确称量和细致观察。

①证明化学反应发生且体现质量守恒定律的现象有: , 。
②此实验用氧气替代空气的主要目的是。
③实验室里现有过氧化氢溶液,二氧化锰粉末,以及下列仪器:

Ⅰ、写出编号仪器的名称:B。
Ⅱ、利用上述药品,仅器:制取少量纯净氧气,反应的化学方程式为 , 能否组装一套制氧气的装置,以控制反应的发生和停止。(填“能”或“否”),并说明理由。
(3)、【总结与反思】1663年,英国化学家波义耳将金属汞放在密闭容器里煅烧,冷却后称量时打开了盖,得出的结论是物质的总质量增加了,导致波义耳与质量守恒定律失之交臂,你认为质量增大的原因是:。
四、计算题
-
21. 如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克。称得反应后烧杯内物质的总质量为64.3克。

请计算:
(1)、反应完成后生成气体的质量为g。(2)、反应后烧杯中溶液的质量和胃药中NaHCO3的质量分数。