辽宁省鞍山市铁西区2022年中考二模化学试题
试卷更新日期:2022-07-29 类型:中考模拟
一、单选题
-
1. 我国防控“新冠”疫情成绩显著。下列防疫相关措施中发生了化学变化的是( )A、裁切无纺布制作口罩 B、对消毒液加水稀释 C、合成抗病毒药物 D、水银温度计测体温2. 下列符号:2N、N2、H2O 、2CO、SO2中,数字“2”的意义能用来表示分子个数的有()A、2个 B、1个 C、4个 D、5个3. 空气中含量较多,化学性质比较活泼的气体是( )A、氮气 B、氧气 C、二氧化碳 D、水4. 关于分子和原子的说法正确的是( )A、分子大,原子小 B、分子是不断运动的,原子是静止的 C、分子能构成物质,原子不能 D、化学变化中分子可分,原子不可分5. 保鲜膜的主要成分是聚乙烯(化学式为[]。聚乙烯属于( )A、金属材料 B、合成材料 C、无机非金属材料 D、复合材料6. 下列实验操作正确的是( )A、
 点燃酒精灯
B、
点燃酒精灯
B、 倾倒液体
C、
倾倒液体
C、 闻气体气味
D、
闻气体气味
D、 加热液体
7. 下列做法中,不利于保护金属资源的是( )A、回收易拉罐 B、过度开采金属矿物 C、防止金属的腐蚀 D、寻找金属代用品8. 日常生活中除去油污的方法很多,下列现象不属于乳化的是( )A、修车工用汽油洗去手上的油污 B、洗发精洗去头发上的油脂 C、用沐浴露洗澡 D、洗洁精洗去餐具上的油污9. 下列变化不能通过一步反应实现的是( )A、Cu→Cu(OH)2 B、Zn→Ag C、CaCl2→CaCO3 D、Na2CO3→NaOH10. 下列说法符合“人与自然和谐共生”这一理念的是( )A、任意使用农药和化肥 B、大量开采煤和石油 C、提倡使用可降解塑料 D、随意丢弃废旧电池11. 下表列举了四组待鉴别的物质和对应的鉴别方法,其中不可行的是( )
加热液体
7. 下列做法中,不利于保护金属资源的是( )A、回收易拉罐 B、过度开采金属矿物 C、防止金属的腐蚀 D、寻找金属代用品8. 日常生活中除去油污的方法很多,下列现象不属于乳化的是( )A、修车工用汽油洗去手上的油污 B、洗发精洗去头发上的油脂 C、用沐浴露洗澡 D、洗洁精洗去餐具上的油污9. 下列变化不能通过一步反应实现的是( )A、Cu→Cu(OH)2 B、Zn→Ag C、CaCl2→CaCO3 D、Na2CO3→NaOH10. 下列说法符合“人与自然和谐共生”这一理念的是( )A、任意使用农药和化肥 B、大量开采煤和石油 C、提倡使用可降解塑料 D、随意丢弃废旧电池11. 下表列举了四组待鉴别的物质和对应的鉴别方法,其中不可行的是( )待鉴别的物质
鉴别方法
A
蒸馏水、食盐水
加入硝酸银溶液,观察有无沉淀产生
B
硫酸铵、氯化钾
加水后,观察是否溶于水
C
羊毛纤维、棉花纤维
灼烧,闻燃烧产生的气味,观察燃烧后的灰烬
D
氧气、二氧化碳、空气
用燃着的木条检验,观察木条燃烧情况
A、A B、B C、C D、D12. 可用金属活动性,对下列现象和事实做出合理解释的是( )①相同质量的镁和铝与足量稀盐酸反应产生的氢气质量不同:②不能用铜与稀硫酸反应制取氢气:③用硫酸铜、石灰乳配置农药波尔多液时,不能用铁制容器;④银的导电性强于铜。
A、①②③④ B、①③④ C、①②③ D、②③13. 运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )A、水沸腾时可冲起壶盖,说明温度升高分子会变大 B、水和过氧化氢的组成元素相同,则两者的化学性质相同 C、同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率 D、Na+、Cl﹣的最外层电子数均为8,由此得出离子的最外层电子数均为814. 下列溶液中无色,且在pH=1时能大量共存的是A、CuSO4 NaCl KNO3 B、NaOH NaCl NaNO3 C、Na2SO4 KCl ZnCl2 D、K2SO4 AgNO3 NaCl15. 我国科学家制作出一种新型“纳米纸”,在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中的亚硝酸盐浓度高低。则下列说法正确的是( )A、萘胺是混合物 B、萘胺中C,H,N三种元素的质量比为10:9:1 C、萘胺的相对分子质量是143 D、萘胺中C元素的质量分数为50%二、填空题
-
16. 在“明矾、碳酸氢铵、乙醇、不锈钢”中选择适当的物质填空。(1)、用于制造医疗器械、炊具的是。(2)、在农业上作为铵态氮肥的是。(3)、可以代替汽油用作汽车燃料的是。(4)、净化水时可作絮凝剂的是。17. 锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示
 (1)、锶属于元素(填“金属”或“非金属”)。(2)、锶元素的原子序数为 , 相对原子质量为。(3)、如图所表示的粒子的化学符号是。18. 铁是生产生活中应用最广泛的一种金属。(1)、在酱油中加入铁强化剂,是我国为解决(填“甲状腺肿大”、“贫血”或“骨质疏松”)而实施的项目。(2)、铁元素与地壳中含量最多的元素组成化合物的化学式为(写一种)。一般的,生铁和钢含碳量较高的是。(3)、常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。请将下列脱氧中的主要反应的化学方程式补充完整:。19. 如图是KNO3与KCl的溶解度曲线,回答下列问题:
(1)、锶属于元素(填“金属”或“非金属”)。(2)、锶元素的原子序数为 , 相对原子质量为。(3)、如图所表示的粒子的化学符号是。18. 铁是生产生活中应用最广泛的一种金属。(1)、在酱油中加入铁强化剂,是我国为解决(填“甲状腺肿大”、“贫血”或“骨质疏松”)而实施的项目。(2)、铁元素与地壳中含量最多的元素组成化合物的化学式为(写一种)。一般的,生铁和钢含碳量较高的是。(3)、常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。请将下列脱氧中的主要反应的化学方程式补充完整:。19. 如图是KNO3与KCl的溶解度曲线,回答下列问题: (1)、t1℃时,两物质中溶解度较大的是。(2)、t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是的溶液。(3)、t2℃时,将100g水加入盛有50gKCl的烧杯中,充分溶解后,得到KCl的(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,KCl溶液的溶质的质量分数(填“变大”、“不变”或“变小”)。20. 亚硝酸钠(NaNO2)是常用的防腐剂。结合如图“小资料”回答问题:
(1)、t1℃时,两物质中溶解度较大的是。(2)、t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是的溶液。(3)、t2℃时,将100g水加入盛有50gKCl的烧杯中,充分溶解后,得到KCl的(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,KCl溶液的溶质的质量分数(填“变大”、“不变”或“变小”)。20. 亚硝酸钠(NaNO2)是常用的防腐剂。结合如图“小资料”回答问题: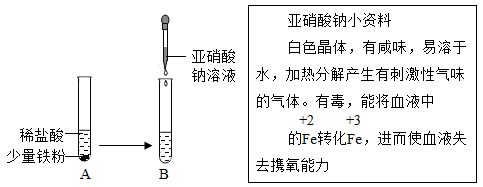 (1)、标出亚硝酸钠中氮元素的化合价。(2)、针对资料,小明设计如下实验:实验B观察到的现象是。(3)、亚硝酸钠加热分解放出的气体可能是____(填字母)。A、NO2 B、NH3 C、N2 D、SO221. 现有水、木炭粉、氧化铁粉末、氯化铁溶液、氢氧化钾溶液五种物质,请按下列要求写出相应的化学方程式。(每种物质不能重复使用)(1)、有红褐色沉淀生成的反应。(2)、分解反应。(3)、置换反应。22. 请将体现下列实验操作目的的符合题意选项,填在对应的横线上。
(1)、标出亚硝酸钠中氮元素的化合价。(2)、针对资料,小明设计如下实验:实验B观察到的现象是。(3)、亚硝酸钠加热分解放出的气体可能是____(填字母)。A、NO2 B、NH3 C、N2 D、SO221. 现有水、木炭粉、氧化铁粉末、氯化铁溶液、氢氧化钾溶液五种物质,请按下列要求写出相应的化学方程式。(每种物质不能重复使用)(1)、有红褐色沉淀生成的反应。(2)、分解反应。(3)、置换反应。22. 请将体现下列实验操作目的的符合题意选项,填在对应的横线上。A.防止药品污染 B.防止试管破裂 C.防止实验误差 D.防止液体溅出
(1)、加热试管时,先均匀加热,后集中加热。(2)、滴管使用后,及时清洗并放在试管架上。(3)、过滤时,混合液沿玻璃棒慢慢倒入漏斗中。(4)、量取液体时,视线与凹液面最低处保持平视。23. 同学们通过某金属和稀硫酸反应来探究影响化学反应速率的因素。取相同质量的同种金属与相同质量稀硫酸(足量)反应,实验记录如下表:序号
金属状态
硫酸浓度(%)
溶液温度(℃)
金属消失时间(S)
反应前
反应后
1
丝
5
20
34
500
2
粉末
5
20
35
50
3
粉末
5
30
45
40
4
丝
8
20
35
200
5
粉末
8
20
36
25
(1)、实验1和2表明,对反应速率有影响,反应速率越快,能表明同一规律的实验还有(填实验序号)。(2)、仅能表明反应物浓度对反应速率产生影响的实验有(填实验序号)。(3)、本实验中影响反应速率的其他因素还有 , 其实验序号是。(4)、由题中数据还可看出,该反应是反应(填“放热”或“吸热”)。实验中的所有反应,反应前后溶液的温度变化约15℃,推测其原因。三、综合题
-
24. A~H均为初中化学中的常见物质,已知A可用于制肥皂、造纸等工业:B是常用的食品干燥剂,A、C可以发生中和反应。C的溶质由两种元素组成,D、E、F、G、H都含有碳元素,B、F、H是氧化物。A~H之间的转化关系如图所示,框图中“一”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去)。
 (1)、写出下列物质的化学式:B;G。(2)、写出下列转化的化学反应方程式:D→A。C-E。25. 实验室通常采用下面装置制取少量氢气,请根据要求回答:
(1)、写出下列物质的化学式:B;G。(2)、写出下列转化的化学反应方程式:D→A。C-E。25. 实验室通常采用下面装置制取少量氢气,请根据要求回答: (1)、写出上图中带标号仪器的名称:① , ②。(2)、实验室使用稀盐酸和金属锌制取氢气的化学方程式为 , 这种方法制得的氢气往往含有少量和水蒸气,要除去杂质气体可将气体依次通过(写接口字母)并采用装置收集氢气。
(1)、写出上图中带标号仪器的名称:① , ②。(2)、实验室使用稀盐酸和金属锌制取氢气的化学方程式为 , 这种方法制得的氢气往往含有少量和水蒸气,要除去杂质气体可将气体依次通过(写接口字母)并采用装置收集氢气。四、计算题
-
26. 某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明做了如下实验:准确称取样品12g,向其中加入57.9g稀盐酸,恰好完全反应,共产生气体4.4g,请回答下列问题
纯碱样品中的碳酸钠的质量分数是?(精确到0.1%)求反应后所得溶液中氯化钠的质量分数是?