浙教版科学九年级上册第1章 物质及其变化 单元检测
试卷更新日期:2022-07-27 类型:同步测试
一、单选题
-
1. 世界充满了变化、下列过程中,发生了化学变化的是( )A、雕琢玉石
 B、丝线织锦
B、丝线织锦
 C、葡萄制酒
C、葡萄制酒
 D、瓷盘破碎
D、瓷盘破碎
 2. 甲烷是天然气的主要成分,下列对甲烷性质的描述属于化学性质的是( )A、极难溶于水 B、标准状况下,密度比空气小 C、具有可燃性 D、通常为无色、无味的气体3. 下列各组物质反应,所得溶液能使酚酞溶液变红的是( )A、一定量的稀盐酸与适量的氢氧化钠溶液恰好完全反应 B、相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸混合后充分反应 C、将硫酸钠溶液滴入氢氧化钡溶液中恰好完全反应 D、将二氧化碳气体通入氢氧化钙溶液中恰好完全反应4. 不同品牌的洗手液pH一般不同,25 ℃时四种洗手液的pH如图所示。下列说法错误的是( )
2. 甲烷是天然气的主要成分,下列对甲烷性质的描述属于化学性质的是( )A、极难溶于水 B、标准状况下,密度比空气小 C、具有可燃性 D、通常为无色、无味的气体3. 下列各组物质反应,所得溶液能使酚酞溶液变红的是( )A、一定量的稀盐酸与适量的氢氧化钠溶液恰好完全反应 B、相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸混合后充分反应 C、将硫酸钠溶液滴入氢氧化钡溶液中恰好完全反应 D、将二氧化碳气体通入氢氧化钙溶液中恰好完全反应4. 不同品牌的洗手液pH一般不同,25 ℃时四种洗手液的pH如图所示。下列说法错误的是( ) A、洗手液a的酸性比b强 B、洗手液b用蒸馏水稀释后pH减小 C、洗手液c能使酚酞试液变红 D、洗手液d和a混合液的pH可能等于75. 小科学习了《物质的酸碱性》课程后,决定用 pH 试纸测定一些物质的 pH,下列做法能达到实验目的是( )A、用湿润的pH试纸测定稀硫酸的pH B、用干燥的pH试纸测定浓硫酸的pH C、用pH试纸浸入矿泉水测得pH为7.2 D、用干燥的pH试纸测出胃液的pH为26. 要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是(( )
A、洗手液a的酸性比b强 B、洗手液b用蒸馏水稀释后pH减小 C、洗手液c能使酚酞试液变红 D、洗手液d和a混合液的pH可能等于75. 小科学习了《物质的酸碱性》课程后,决定用 pH 试纸测定一些物质的 pH,下列做法能达到实验目的是( )A、用湿润的pH试纸测定稀硫酸的pH B、用干燥的pH试纸测定浓硫酸的pH C、用pH试纸浸入矿泉水测得pH为7.2 D、用干燥的pH试纸测出胃液的pH为26. 要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是(( )
①锌和稀硫酸;②石灰石和稀盐酸;③氧化铁和硫酸;④生石灰和水。
A、①② B、①②③ C、①②④ D、①②③④7. 稀盐酸滴入镁粉中即产生气体,现向一定质量的稀盐酸中加入镁粉至过量,若图像中横坐标表示镁粉的质量,则纵坐标表示 ( ) A、生成气体的质量 B、稀盐酸的质量 C、氯化镁的质量 D、溶液的质量8. 要使如图所示装置中的气球明显鼓起来,则使用的固体和液体可以是( )
A、生成气体的质量 B、稀盐酸的质量 C、氯化镁的质量 D、溶液的质量8. 要使如图所示装置中的气球明显鼓起来,则使用的固体和液体可以是( )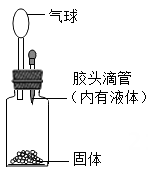
①锌和稀硫酸 ②石灰石和稀盐酸
③氧化铁和稀硫酸 ④氢氧化钠和水
A、① B、①②③ C、①②④ D、①②③④9. 下列4种物质,把他们长期露置在空气中,其中会发生化学变化且质量增加的是( )A、浓盐酸 B、烧碱 C、浓硫酸 D、碳酸钠晶体10. 如图,在滴有酚酞的氢氧化钠溶液中持续加入稀盐酸,对该过程描述正确的是( ) A、温度计读数持续上升 B、测其 pH 逐渐变小 C、溶液呈红色时,反应没发生 D、溶液呈无色时,溶液中的溶质一定只有氯化钠11. 如图所示的pH变化曲线是盐酸与氢氧化钠反应得到的结果,则下列说法正确的是( )
A、温度计读数持续上升 B、测其 pH 逐渐变小 C、溶液呈红色时,反应没发生 D、溶液呈无色时,溶液中的溶质一定只有氯化钠11. 如图所示的pH变化曲线是盐酸与氢氧化钠反应得到的结果,则下列说法正确的是( ) A、横坐标是滴加的盐酸体积 B、向a点的溶液中加入硫酸铜溶液产生蓝色沉淀 C、向b点的溶液中加入紫色石蕊试液变红色 D、C点溶液中的阴离子只有Cl-12. 酸碱中和反应在生活中有广泛应用.下列应用不属于中和反应的是( )A、用盐酸除铁锈 B、服用含有氢氧化镁的药物治疗胃酸过多 C、用熟石灰改良酸性土壤 D、用硫酸处理印染厂含碱废水13. 向盛有50mL稀硫酸的烧杯中,缓慢滴加一定溶质质量分数的氢氧化钡溶液至过量。随着氢氧化钡溶液的滴加,某些量变化趋势正确的是( )A、
A、横坐标是滴加的盐酸体积 B、向a点的溶液中加入硫酸铜溶液产生蓝色沉淀 C、向b点的溶液中加入紫色石蕊试液变红色 D、C点溶液中的阴离子只有Cl-12. 酸碱中和反应在生活中有广泛应用.下列应用不属于中和反应的是( )A、用盐酸除铁锈 B、服用含有氢氧化镁的药物治疗胃酸过多 C、用熟石灰改良酸性土壤 D、用硫酸处理印染厂含碱废水13. 向盛有50mL稀硫酸的烧杯中,缓慢滴加一定溶质质量分数的氢氧化钡溶液至过量。随着氢氧化钡溶液的滴加,某些量变化趋势正确的是( )A、 B、
B、 C、
C、 D、
D、 14. 向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是( )
14. 向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是( ) A、a点,向溶液中滴加稀盐酸,无白色沉淀 B、c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生 C、d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2 D、e点,过滤后得到的固体中只含有2种物质15. 小滨对某无色溶液所含溶质的记录,合理的是( )A、HCl、NaOH、Na2SO4 B、KNO3、ZnCl2、FeCl2 C、AgNO3、H2SO4、NaCl D、NaOH、Na2CO3、NaCl
A、a点,向溶液中滴加稀盐酸,无白色沉淀 B、c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生 C、d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2 D、e点,过滤后得到的固体中只含有2种物质15. 小滨对某无色溶液所含溶质的记录,合理的是( )A、HCl、NaOH、Na2SO4 B、KNO3、ZnCl2、FeCl2 C、AgNO3、H2SO4、NaCl D、NaOH、Na2CO3、NaCl二、填空题
-
16. 一款名为“史莱姆”的水晶泥玩具,其主要成分是普通胶水、硼砂晶体和水。查阅资料知道:
①硼砂晶体(Na2B4O7·10H2O)是一种易溶于水的白色固体,可用作清洁剂、杀虫剂。
②人体若摄入过多的硼,会引发多脏器的蓄积性中毒。
(1)、硼砂晶体(Na2B4O7·10H2O)中硼(B)元素的化合价为。(2)、请至少写出一条关于硼砂晶体的物理性质。17. 小明在凉拌紫甘蓝时,加入一些白醋,发现紫甘蓝变红了。他又向其他不同试剂中滴加紫甘蓝汁,记录实验现象如表。请回答:试剂
稀盐酸
氢氧化钠溶液
蒸馏水
白醋
纯碱溶液
滴加2滴紫甘蓝汁后的颜色
红色
绿色
紫色
红色
绿色
(1)、在石灰水中滴加紫甘蓝汁,溶液可能显示的颜色是。(2)、用pH试纸测定上述部分溶液的酸碱度,具体操作方法是。18. 浓H2SO4稀释时,要让沿着烧杯壁缓缓倒入烧杯里的已有液体中,否则将会使液滴飞溅,造成危险。浓硫酸可以干燥H2或O2 , 是由于它有性。19. 根据酸的化学性质回答下列问题。(1)、酸溶液有相似化学性质的原因是溶液中都含有(填离子符号)(2)、图中反应③属于基本反应类型中的反应;(3)、请写出符合性质②,反应后能生成蓝色溶液的一个反应的化学方程式。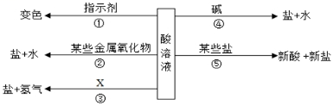 20. 某同学利用A~D四个透明塑料杯和导管设计“塔杯变色”趣味实验:四个杯子分别盛有盐酸、碳酸钠、氯化钙、酚酞中的某一种溶液。往A杯加入适量的氢氧化钠溶液后,溶液变红色。当上一杯液体达到一定量时会自动流入下一杯,出现的现象如图所示。回答问题:
20. 某同学利用A~D四个透明塑料杯和导管设计“塔杯变色”趣味实验:四个杯子分别盛有盐酸、碳酸钠、氯化钙、酚酞中的某一种溶液。往A杯加入适量的氢氧化钠溶液后,溶液变红色。当上一杯液体达到一定量时会自动流入下一杯,出现的现象如图所示。回答问题: (1)、B杯溶液变成无色,反应的化学方程式为。(2)、从B杯流出的溶液中溶质有。(3)、C杯中产生气泡的化学方程式为。21. 用符合下列要求的物质的字母填空。
(1)、B杯溶液变成无色,反应的化学方程式为。(2)、从B杯流出的溶液中溶质有。(3)、C杯中产生气泡的化学方程式为。21. 用符合下列要求的物质的字母填空。a.稀盐酸 b.氢氧化钠 c.熟石灰 d.碳酸氢钠 e.氯化钾
(1)、用于去除铁锈的是;(2)、用于治疗胃酸过多的是;(3)、用于增强作物抗倒伏能力的是;(4)、用于改良酸性土壤的是。22. 扑克是生活中用来休闲的娱乐项目之一,聪明的小华发明了一种扑克新玩法-“化学扑克”。“化学扑克”的玩法是:上家出牌,如果下家牌中的物质能与上家的发生反应,即可出牌,按此规则,出完牌的为赢家。下图表示的是某局牌的最后一轮。桌面上是一张图甲的“盐酸”牌,ABCD四位玩家手中都剩下一张牌(如图)。 (1)、如果本局每一位玩家的牌都能出掉,则四位玩家的出牌顺序为:(填标号)甲→;(2)、如果本局只有一位玩家的牌出不掉,他们的出牌顺序为:(填标号)甲→。23. 某化学反应的微观示意图如图所示,根据图示填空:
(1)、如果本局每一位玩家的牌都能出掉,则四位玩家的出牌顺序为:(填标号)甲→;(2)、如果本局只有一位玩家的牌出不掉,他们的出牌顺序为:(填标号)甲→。23. 某化学反应的微观示意图如图所示,根据图示填空: (1)、反应还生成其他物质,补充完整图示中反应后微粒的化学式;(2)、写出此化学反应的基本类型是。24. 亚硝酸钠是工业用盐,因有咸味、外观酷似食盐而常被误食。亚硝酸盐能致癌,因有良好的着色防腐作用,广泛用于肉类食品添加剂,但用量严格限制,亚硝酸钠易溶于水,其水溶液呈碱性,暴露于空气中能与氧气反应生成硝酸钠。加热至320℃以上或遇强酸则分解出红棕色有毒、有刺激性气味的二氧化氮气体。请根据信息回答:(1)、亚硝酸钠的保存方式是 , 原因是;(2)、试设计出1种区别亚硝酸钠和食盐的简单方案(简单叙述即可): 。25. 利用数据传感技术可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。某同学倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。
(1)、反应还生成其他物质,补充完整图示中反应后微粒的化学式;(2)、写出此化学反应的基本类型是。24. 亚硝酸钠是工业用盐,因有咸味、外观酷似食盐而常被误食。亚硝酸盐能致癌,因有良好的着色防腐作用,广泛用于肉类食品添加剂,但用量严格限制,亚硝酸钠易溶于水,其水溶液呈碱性,暴露于空气中能与氧气反应生成硝酸钠。加热至320℃以上或遇强酸则分解出红棕色有毒、有刺激性气味的二氧化氮气体。请根据信息回答:(1)、亚硝酸钠的保存方式是 , 原因是;(2)、试设计出1种区别亚硝酸钠和食盐的简单方案(简单叙述即可): 。25. 利用数据传感技术可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。某同学倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。 (1)、碳酸钙与稀盐酸反应的化学方程式。(2)、传感器应是采集数据来反应碳酸钙与稀盐酸反应的速率。(3)、下列有关说法正确的是 (填字母序号)。A、对比分析a、b点可知,曲线①表示块状碳酸钙与稀盐酸反应 B、对比分析c、d点可知,相同的气压时,碳酸钙粉末与稀盐酸反应速率更快 C、碳酸钙粉末产生的CO2质量多
(1)、碳酸钙与稀盐酸反应的化学方程式。(2)、传感器应是采集数据来反应碳酸钙与稀盐酸反应的速率。(3)、下列有关说法正确的是 (填字母序号)。A、对比分析a、b点可知,曲线①表示块状碳酸钙与稀盐酸反应 B、对比分析c、d点可知,相同的气压时,碳酸钙粉末与稀盐酸反应速率更快 C、碳酸钙粉末产生的CO2质量多三、实验探究题
-
26. 下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。

滴管甲
烧杯①
滴管乙
烧杯②
试剂
H2O
生石灰
稀盐酸
Mg
(1)、若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞溶液变红,说明分子具有的性质是 。(2)、若甲中吸有水,乙中吸有稀硫酸,烧杯①中做有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应采取的实验操作是。(3)、按照上面表格中有关内容,若先将甲中的液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起。气球鼓起是因为装置内气压增大,两次气压增大的原因依次是、。27. 在学习完中和反应相关知识后,某化学学习小组同学对实验室的两份溶液展开了相关探究,记录如下:在甲图中,A、B、C、D四点分别表示溶质质量分数均为10%的氢氧化钠溶液和稀盐酸的混合物,图乙表示各溶液混合后的最高温度(所有溶液的起始温度均为22℃)。试回答下列问题: (1)、该探究过程中的主要化学反应方程式为;(2)、D点对应的混合物反应完全后所得溶液中离子有 , 在C点对应的溶液中加入紫色石蕊试液,溶液呈色;(3)、下列反应中微观本质与该小组探究反应本质相同的是(填序号)。
(1)、该探究过程中的主要化学反应方程式为;(2)、D点对应的混合物反应完全后所得溶液中离子有 , 在C点对应的溶液中加入紫色石蕊试液,溶液呈色;(3)、下列反应中微观本质与该小组探究反应本质相同的是(填序号)。①小苏打治疗胃酸过多 ②熟石灰改良酸性土壤 ③硫酸与火碱反应
28. 一次用餐中,小丽同学对“固体酒精”产生好奇,于是她决定买回一袋,对其进行研究.
【收集资料】
通过阅读标签及查阅资料,她获得如下信息:
⑴该固体酒精中含有酒精、氯化钙、氢氧化钠三种物质;
⑵酒精的化学式为 C2H5OH; (3)氯化钙、氯化钡的水溶液均呈中性.
【提出问题】
⑶酒精的化学式与 NaOH 相比,都有“OH”,那么酒精的水溶液是不是显碱性?
⑷固体酒精中的氢氧化钠是否变质及变质的程度如何?
(1)、【实验探究】实验一:她取少量酒精溶液于试管中,滴加硫酸铜溶液,未观察到蓝色沉淀,说明酒精溶液(填“显”或“不显”)碱性.
(2)、实验二:她先取少量固体酒精于烧杯中,加入足量水溶解后静置,发现烧杯底部有白色沉淀,再取沉淀于试管中加稀盐酸,观察到 , 说明氢氧化钠已变质.请写出氢氧化钠在空气中变质的化学方程式 .(3)、她取上述烧杯中上层清液于试管中,先滴加足量澄清石灰水,发现生成白色沉淀,再滴入几滴无色酚酞溶液,液体呈红色,她认为氢氧化钠部分变质.老师发现后,提示她由该实验得出的结论不可靠.你认为只要将上述实验中的澄清石灰水变为(填化学式)溶液, 即可得到氢氧化钠部分变质的结论.(4)、【拓展应用】除去部分变质的氢氧化钠溶液中的杂质,方法是(用化学方程式表示).
29. 为了研究氢氧化钠溶液与盐酸反应是吸热还是放热,科学兴趣小组进行了如下实验: (1)、图甲中,需要插入(填器材),通过测量来判断氢氧化钠和盐酸反应是吸热还是放热。(2)、氢氧化钠和盐酸恰好完全反应的评判标准是;(3)、随着盐酸不断滴入,烧杯中溶液温度变化如坐标图乙所示,由此判断氢 氧化钠溶液与盐酸反应是(选填“吸热”或“放热”);(4)、实验过程中,测得某时溶液的温度是 32℃,则 a、b 两点的溶液中,相 同的溶质是(不包括酚酞)。30. 小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.
(1)、图甲中,需要插入(填器材),通过测量来判断氢氧化钠和盐酸反应是吸热还是放热。(2)、氢氧化钠和盐酸恰好完全反应的评判标准是;(3)、随着盐酸不断滴入,烧杯中溶液温度变化如坐标图乙所示,由此判断氢 氧化钠溶液与盐酸反应是(选填“吸热”或“放热”);(4)、实验过程中,测得某时溶液的温度是 32℃,则 a、b 两点的溶液中,相 同的溶质是(不包括酚酞)。30. 小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,
说明Na2CO3溶液显性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含 .
(选填答案:A、稀盐酸 B、澄清石灰水 C、碳酸钠溶液)
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH; ③NaCl Na2CO3和NaOH; ④…
【实验验证】(提示:CaCl2溶液显中性)
实验操作
实验现象
实验结论
取少量滤液于试管中,加入足量CaCl2溶液
猜想③成立
【反思评价】有同学提出CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立。小刚同学认为不正确,其理由是:。
四、解答题
-
31. 钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。


[提示]①食醋的主要成分是醋酸(HAc),醋酸和碳酸钙反应的化学方程式为:
CaCO3+ 2HAc =Ca(Ac)2+H2O+CO2↑
②鱼骨中其它成分与食醋反应生成的气体可忽略不计。
(1)、由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是 (填“变大”“变小”或“不变”")。(2)、根据图中的数据计算鱼骨中碳酸钙的质量分数。(3)、生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明: 。32. 将体积为V1 , 质量分数为3.65% 的HCl溶液逐滴滴入盛有体积为V2未知浓度的NaOH溶液的烧杯中(如图甲),测量并记录溶液的pH变化(如图乙)和温度变化(如图丙)。(实验中始终保持V1+V2=50.0mL且各种溶液密度均为1.0g/mL) (1)、图乙中的pH=7时,此时滴入的HCl溶液的体积V1=mL。(2)、通过该实验给出的判断,其中正确的是 。A、进行该实验时环境温度为22℃ B、该实验中的反应放出热量 C、该实验表明有水生成的反应都是放热反应 D、溶液由碱性转变为中性,再转变为酸性且酸性不断减弱(3)、实验中所用NaOH溶液的溶质质量分数为多少?33. 家庭食用碱的主要成分是Na2CO3 , 为测定该食用碱中Na2CO3的质量分数,某同学进行了以下实验。取48g食用碱,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见如表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl2溶液产生沉淀)。请分析表中数据回答并计算。
(1)、图乙中的pH=7时,此时滴入的HCl溶液的体积V1=mL。(2)、通过该实验给出的判断,其中正确的是 。A、进行该实验时环境温度为22℃ B、该实验中的反应放出热量 C、该实验表明有水生成的反应都是放热反应 D、溶液由碱性转变为中性,再转变为酸性且酸性不断减弱(3)、实验中所用NaOH溶液的溶质质量分数为多少?33. 家庭食用碱的主要成分是Na2CO3 , 为测定该食用碱中Na2CO3的质量分数,某同学进行了以下实验。取48g食用碱,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见如表(假设该食用碱中不含难溶性杂质且杂质均不与CaCl2溶液产生沉淀)。请分析表中数据回答并计算。实验一
实验二
实验三
实验四
食用碱的质量
12g
12g
12g
12g
加入CaCl2溶液的质量
20g
40g
60g
80g
生成沉淀的质量
4g
m
10g
10g
(1)、m=g。(2)、该食用碱中Na2CO3的质量分数是多少? (写出计算过程,答案精确到0.1%)(3)、根据表中实验数据以及适当的计算,请画出实验四中生成沉淀的质量↓沉淀/g和加入CaCl2溶液的质量的坐标关系图,请标出拐点数据。34. 在化学实验中,有时药品的滴加顺序不同会导致实验现象不同。某同学使用图甲所示实验装置进行实验,广口瓶内气球的体积变化与滴加药品体积的关系如图乙所示,其中 A 点表示开始滴加某种药品,B 点表示开始滴加另一种药品(不考虑由于滴入液体的体积,及反应导致的温度变化对集气瓶内气压的影响)。据图回答: (1)、实验中首先加入试剂是。(2)、试从加入药品的种类、顺序及发生的化学反应等角度来解释气球体积的变化情况。
(1)、实验中首先加入试剂是。(2)、试从加入药品的种类、顺序及发生的化学反应等角度来解释气球体积的变化情况。五、综合说理题
-
35. 敞口放置的氢氧化钠溶液易变质,现向一定质量且部分变质的氢氧化钠溶液中滴加入稀盐酸并振荡。(酸的浓度尽可能的低,滴入时尽量缓慢)请在下面坐标图中画出表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况并说明原因。(A代表起点,已画好)