浙教版科学九年级上册1.2物质的酸碱性 同步练习
试卷更新日期:2022-07-27 类型:同步测试
一、单选题
-
1. 下表为人体内的部分体液正常pH的范围,其中酸性最强的是( )
种类
唾液
胃液
胰液
肠液
pH
6.6-7.1
0.9-1.8
7.8-8.0
8.0-9.0
A、唾液 B、胃液 C、胰液 D、肠液2. 下列物质跟水混合后,能使紫色石蕊试液变蓝的是( )A、Fe2O3 B、Na2CO3 C、Cu(OH)2 D、HCl3. 如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作。下列说法正确的是( )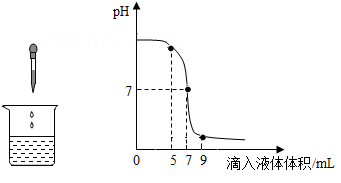 A、该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中 B、当滴入液体体积为5mL时,所得溶液呈酸性 C、当滴入液体体积为9mL时,所得溶液中的溶质只有NaCl D、当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应4. 氢氧化钠和氢氧化钙都是常见的碱,我们之所以认为它们是碱,是因为它们( )A、溶液的pH都大于7 B、都能使酚酞试液变红 C、都能与非金属氧化物反应 D、电离产生的阴离子只有OH-5. 小明在实验室发现一瓶无色溶液,由于标签残缺不全。下列对这瓶溶液的分析正确的是( )
A、该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中 B、当滴入液体体积为5mL时,所得溶液呈酸性 C、当滴入液体体积为9mL时,所得溶液中的溶质只有NaCl D、当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应4. 氢氧化钠和氢氧化钙都是常见的碱,我们之所以认为它们是碱,是因为它们( )A、溶液的pH都大于7 B、都能使酚酞试液变红 C、都能与非金属氧化物反应 D、电离产生的阴离子只有OH-5. 小明在实验室发现一瓶无色溶液,由于标签残缺不全。下列对这瓶溶液的分析正确的是( ) A、其pH值一定为7 B、不可能是硫酸铜溶液 C、这瓶液体可能是碱 D、其中一定含有金属元素6. 某校九年级甲、乙两班同学进行常见酸和碱与指示剂反应的实验,使用的试剂如下图所示。实验后废液分别集中到废液缸中。某研究小组对此废液进行了检测,结果如下:
A、其pH值一定为7 B、不可能是硫酸铜溶液 C、这瓶液体可能是碱 D、其中一定含有金属元素6. 某校九年级甲、乙两班同学进行常见酸和碱与指示剂反应的实验,使用的试剂如下图所示。实验后废液分别集中到废液缸中。某研究小组对此废液进行了检测,结果如下:废液来源
检测方法和结果
甲班
观察废液呈无色
乙班
观察废液呈红色

请你根据实验现象判断,对该废液的溶质的说法错误的是( )
A、甲班废液中可能含有盐酸 B、甲班废液中只有氯化钠和氯化钙 C、乙班废液的成分中肯定没有盐酸 D、乙班废液中可能含有氢氧化钠7. 四只烧杯中分别盛有稀盐酸,并滴加了数滴紫色石蕊试液。现分别向这四只烧杯中不断加入下列物质,直至过量,其中能使溶液最后呈紫色的物质是( )A、CaO B、NaOH C、Mg(OH)2 D、AgNO38. 烧杯中盛有x 溶液,逐滴加入(或通入)y 物质,烧杯内液体的 pH 变化如图所示.则符合该变化的一组物质是( )
x
y
A
NaOH溶液
稀HCl(过量)
B
稀H2SO4
BaCl2溶液(少量)
C
Ca(OH)2
CO2(适量)
D
稀NaOH
H2O
A、A B、B C、C D、D9. 某同学在实验室测定了几种液体的pH,其结果如下表所示:溶液
盐酸
CuCl2 溶液
Na2SO4溶液
水
Na2CO3溶液
NaOH溶液
pH
<7
<7
=7
=7
>7
>7
该同学由此得出的结论正确的是( )
A、pH<7一定是酸溶液 B、pH>7一定是碱溶液 C、pH=7一定是盐溶液 D、盐溶液可能显酸性、碱性或中性10. 用酒精和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显红色,遇碱性溶液显黄色。下列说法正确的是( )A、蝴蝶兰花的溶液与酸作用显红色是物理变化 B、能使蝴蝶兰花的溶液显黄色的一定是碱溶液 C、将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色。 D、往氢氧化镁中滴加蝴蝶兰花的溶液呈黄色11. 黑枸杞浸泡在不同pH值的溶液中,溶液呈现的颜色情况如图所示。下列与黑枸杞浸泡会呈现蓝绿色的液体是( )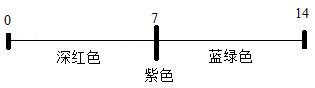 A、纯碱溶液 B、稀盐酸 C、食盐水 D、蒸馏水12. 体液的pH能够反映人体的健康状况,下表是四种体液的正常pH范围。据表可知,体液在正常pH范围都呈碱性的是( )
A、纯碱溶液 B、稀盐酸 C、食盐水 D、蒸馏水12. 体液的pH能够反映人体的健康状况,下表是四种体液的正常pH范围。据表可知,体液在正常pH范围都呈碱性的是( )体液
唾液
胃液
血液
尿液
正常pH范围
6.6-7.1
0.8-1.5
7.35-7.45
4.6-8.0
A、唾液 B、胃液 C、血液 D、尿液13. 某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是( )A、该物质可能是氢氧化铜 B、该物质一定是纯碱的水溶液 C、可以将pH试纸放入该物质的稀溶液中测其pH D、向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小14. 不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( ) A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于715. 黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )A、食盐水(pH≈7) B、牙膏(pH≈9) C、肥皂(pH≈10) D、米醋(pH≈3)
A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于715. 黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )A、食盐水(pH≈7) B、牙膏(pH≈9) C、肥皂(pH≈10) D、米醋(pH≈3)二、填空题
-
16. 构建知识网络是重要的学习方法。小明在学了物质转化的规律后,构建了如图知识网络。
 (1)、若图中金属是Ca,则图中相应的碱的化学式为。(2)、若图中金属氧化物是 CuO,可以利用 CO 具有性,使它反应发生②号转化。17. 请根据下表回答有关问题(用序号填写)
(1)、若图中金属是Ca,则图中相应的碱的化学式为。(2)、若图中金属氧化物是 CuO,可以利用 CO 具有性,使它反应发生②号转化。17. 请根据下表回答有关问题(用序号填写)序号
①
②
③
④
物质
醋酸
高锰酸钾
熟石灰
纯碱
化学式
CH3COOH
KMnO4
Ca(OH)2
Na2CO3
(1)、上表中的物质属于碱的是。(2)、若要测定纯碱溶液的酸碱性强弱,可选用下列选项中的。①无色酚酞试液②紫色石蕊试液③pH试纸
18. 金属锂(元素符号为Li)在通讯和航空航天领域中具有极其重要的用途。它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,具有强碱性和腐蚀性。(1)、写出氢氧化锂的物理性质。(2)、氢氧化锂和氢氧化钠一样,具有碱性,我们可以使用pH试纸检验其碱性强弱,具体步骤为。(3)、氢氧化锂能与盐酸反应,其反应微观实质是。19. 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示: (1)、在滴加的过程中,烧杯中溶液的 pH 逐渐(填“增大”、“减小”或“不变”)(2)、由图可知,稀盐酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”) 反应。20. 学校为预防“手足口病”采取了多种措施,其中包括使用“84消毒液”对学校环境进行消毒。“84消毒液”的有效成分是次氯酸钠(NaClO)。(1)、NaClO属于盐,其中的阴离子符号;(2)、“84消毒液”溶液呈碱性,则其pH7(填“>”、“<”或“=”);(3)、“84消毒液”长期敞口放置会变质失效,这一过程是变化(填“物理”或“化学”)21. 通过两个多月的学习,我们认识了许多“奇妙的酸”和“神奇的碱”,请回答下列问题:(1)、如图表示的是一些物质在常温下的近似pH,回答下列问题:
(1)、在滴加的过程中,烧杯中溶液的 pH 逐渐(填“增大”、“减小”或“不变”)(2)、由图可知,稀盐酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”) 反应。20. 学校为预防“手足口病”采取了多种措施,其中包括使用“84消毒液”对学校环境进行消毒。“84消毒液”的有效成分是次氯酸钠(NaClO)。(1)、NaClO属于盐,其中的阴离子符号;(2)、“84消毒液”溶液呈碱性,则其pH7(填“>”、“<”或“=”);(3)、“84消毒液”长期敞口放置会变质失效,这一过程是变化(填“物理”或“化学”)21. 通过两个多月的学习,我们认识了许多“奇妙的酸”和“神奇的碱”,请回答下列问题:(1)、如图表示的是一些物质在常温下的近似pH,回答下列问题:

①酸雨的酸性比正常雨水的酸性(填“强”或“弱”)。
②测量苹果汁pH时,先用蒸馏水润湿pH试纸,会使pH偏(“大”或“小”)。
(2)、焊接工业上常用稀盐酸清洗铁锈,写出用稀盐酸除铁锈的化学方程式为。22. “有一些花的颜色是红的、蓝的或紫的。这些花里含的色素叫‘花青素’,花青素遇到酸就变红,遇到碱就变蓝……”小勇阅读此段文字后,做了如下家庭实验.将一朵紫色喇叭花泡在肥皂水中,喇叭花很快变成了蓝色;将另一朵紫色喇叭花泡在厨房的某种调味品中,喇叭花变成了红色。请你根据以上实验现象回答。(1)、小勇选用的调味品最有可能是 (选填“食醋”“酱油” 或“纯碱”);(2)、下列各组物质的溶液,仅用喇叭花不能鉴别的一组是 (填序号)。A、HCl、NaOH B、HCl、NaCl C、NaOH、NaCl D、Na2CO3、NaOH23. 某科学兴趣小组为验证硫酸的部分化学性质,使用氢氧化钠、碳酸钠、金属铝和另外一种不同类别的物质A进行了相关实验。(1)、实验时观察到稀硫酸与A反应有蓝色溶液生成,则A物质是。(2)、稀硫酸与氢氧化钠溶液反应时没有明显现象,为了证明二者发生了反应,该组同学设计了如图一所示实验,传感器测定的pH和温度随溶液质量变化的情况见图二、图三。则B溶液是溶液。 24. 某学习小组用黑枸杞提取液作了以下实验:
24. 某学习小组用黑枸杞提取液作了以下实验:实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH
1
2
3
4
5
6
7
8
9
10
11
12
13
14
颜色
粉红
粉红
粉红
浅紫
浅紫
紫
紫
蓝
蓝
深蓝
深蓝
灰绿
黄
黄棕
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。
实验结果如下:
物质
稀盐酸
牛奶
蒸馏水
炉具清洁剂
颜色
粉红
紫
紫
黄
回答下列问题:
(1)、炉具清洁剂的pH为。(2)、若某氢氧化钠溶液的pH为12,向其中加3滴黑枸杞提取液,再滴入稀盐酸至过量,观察到的实验现象为。25. 如图所示,表示的是一些物质在常温下的近似pH值,回答下列问题: (1)、厨房清洁剂显性。(2)、测苹果汁pH值时,先用蒸馏水润湿pH试纸,会使pH值偏(填“大”或“小”)。
(1)、厨房清洁剂显性。(2)、测苹果汁pH值时,先用蒸馏水润湿pH试纸,会使pH值偏(填“大”或“小”)。三、实验探究题
-
26. 在学习了酸碱盐知识后,某科学兴趣小组用黑枸杞提取液作了以下实验:
实验一:室温时,将蒸馏水和不同出的硫酸、氢氧化钠溶液,分别装在14支试管中、并向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
试管
1
2
3
4
5
6
7
8
9
10
11
12
13
14
pH
1
2
3
4
5
6
7
8
9
10
11
12
13
14
颜色
粉红
粉红
粉红
浅紫
浅紫
紫
紫
蓝
蓝
深蓝
深蓝
灰绿
黄
黄棕
实验二:室温时,向4支试管中分别加入相同体积的以下4种物质,各滴加3滴黑枸杞提取液。实验结果表中所示:
物质
稀盐酸
稀硫酸
牛奶
炉具清洁剂
颜色
粉红
浅紫
紫
黄
根据实验,回答下列问题:
(1)、实验一中试管中所装的为蒸馏水(选填编号)。(2)、实验二所用的稀盐酸的酸性比稀硫酸的酸性。(3)、根据实验现象分析,炉具清洁剂适合清除类污溃(选填“酸性”或“碱性”)。(4)、小科认为,黑枸杞提取液也可以作为酸碱指示剂、你认为他的观点是否正确、并说明理由。27. 叶绿素中富含微量元素铁,是天然的造血原料,又具有解毒抗病强身作用。叶绿素呈绿色,被破坏后变成黄褐色。小联同学为探究影响叶绿素稳定性的因素,在室温进行了四组实验,实验记录 如下:组号
叶绿素溶液(毫升)
pH值
处理时间(秒)
溶液颜色
1
3
10
10
绿色
2
3
8
10
绿色
3
3
6
10
黄褐色
4
3
4
10
黄褐色
(1)、本次实验需要的测量工具有。(2)、小联得出结论当pH<7时,叶绿素被破坏。小盟认为这样得出的结论还不够严谨,理由是。(3)、小盟还想探究温度是否会影响叶绿素的稳定性,请你帮他设计实验方案,以文字或表格形式呈现,具体数值参考上表。28. 往一定量的酸(或碱)溶液中逐滴加入某碱(或酸)溶液至恰好完全中和时,溶液的pH随滴加的某溶液质量的变化而变化的关系如图1所示.请回答: (1)、有同学根据图中的曲线判断实验中采用了B装置的操作,该同学判断的依据是。(2)、在以上实验中用了酚酞作指示剂,能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是(3)、若没有恰好完全反应,怎么判断氢氧化钠有剩余.(4)、取5滴恰好完全反应后的溶液于玻璃片上,待液体蒸发后,玻璃片上的物质是(填名称)29. 兴趣小组根据所学的酸碱指示剂的知识,准备自制酸碱指示剂:她们分别用蓝紫色牵牛花、大红色、月季花、紫萝卜花、丝瓜花提取指示剂。
(1)、有同学根据图中的曲线判断实验中采用了B装置的操作,该同学判断的依据是。(2)、在以上实验中用了酚酞作指示剂,能够说明盐酸和氢氧化钠溶液恰好完全中和的实验现象是(3)、若没有恰好完全反应,怎么判断氢氧化钠有剩余.(4)、取5滴恰好完全反应后的溶液于玻璃片上,待液体蒸发后,玻璃片上的物质是(填名称)29. 兴趣小组根据所学的酸碱指示剂的知识,准备自制酸碱指示剂:她们分别用蓝紫色牵牛花、大红色、月季花、紫萝卜花、丝瓜花提取指示剂。【步骤1】分别在研钵中将上述物质倒烂,加乙醇溶液(乙醇和水的体积比为1∶1)浸泡10分钟。
(1)、用研钵捣烂的目的是;(2)、乙醇在其中起到的作用是 。A、催化剂 B、参加化学反应 C、溶质 D、溶剂(3)、【步骤2】将步骤1得到的混合物,用纱布过滤;过滤的目的是。
(4)、【步骤3】将步骤2中得到的浸取液,分别滴入到澄清石灰水和食醋中。花名称
花颜色
浸取液颜色
在不同溶液中所呈颜色
澄清石灰水
食醋
牵牛花
蓝紫
红棕
黄绿
粉红
月季花
大红
玫瑰红
橙黄
粉红
萝卜花
紫
紫红
黄绿
粉红
丝瓜花
黄绿
黄绿
黄
黄
上述四种浸取液,最不适合用作酸碱指示剂的(填名称)。
(5)、将月季花的浸取液滴入稀盐酸中,溶液呈色。30. 某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。(1)、在空地上确定5~6个位置进行取样测定土壤酸碱度。以下三种取样位置设定合理的是。 (2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7。查阅资料,常见作物最适生长的土壤pH范围如下表,则这块空地上适合种植的作物是。
(2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7。查阅资料,常见作物最适生长的土壤pH范围如下表,则这块空地上适合种植的作物是。作物
大蒜
丝瓜
茄子
沙枣
最适pH范围
5.6~6.0
6.0~6.5
6.8~7.3
8.0~8.7
四、解答题
-
31. 硝酸铵(NH4NO3)是常用的一种氮肥,对促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量等有作用。(1)、向土壤中施肥时要注意土壤与化肥的酸碱性,否则容易降低肥效。向硝酸铵溶液中加入紫色石蕊试液,试液变红色,硝酸铵溶液显 (填“酸性”、“碱性”或“中性”)(2)、化肥中的氮含量多少对植物的生长影响较大。硝酸铵中氮元素的质量分数为 。(3)、硝酸铵不能与碱性肥料一起施用,因为铵盐能与碱发生反应而失效.化学方程式为NH4NO3+NaOH NaNO3+X↑+H2O,其中的X化学式为。32. 某同学用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该溶液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如下图所示。
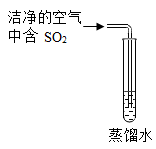
 (1)、在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,但却看到溶液有气泡产生,说明滤液中的溶质除含有CaCl2外,还含有(填化学式)。(2)、Na2CO3溶液从0加到5克的过程中,溶液pH如何变化?(填“变大”“变小”或“不变”)。(3)、计算Na2CO3溶液中溶质的质量分数。33. 2021年6月份公布的《2020年温州市环境状况公报》显示近5年我市酸雨率逐年降低,这与电动汽车的使用有一定的关系。自然降水因空气含二氧化碳而呈酸性,燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体,从而使降水的pH降低,pH小于5.6的降水称为酸雨。(1)、自然降水呈酸性的原因是。(2)、使用纯电动汽车减少排放,符合环保。(3)、小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,你认为下一步的实验操作是:。
(1)、在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,但却看到溶液有气泡产生,说明滤液中的溶质除含有CaCl2外,还含有(填化学式)。(2)、Na2CO3溶液从0加到5克的过程中,溶液pH如何变化?(填“变大”“变小”或“不变”)。(3)、计算Na2CO3溶液中溶质的质量分数。33. 2021年6月份公布的《2020年温州市环境状况公报》显示近5年我市酸雨率逐年降低,这与电动汽车的使用有一定的关系。自然降水因空气含二氧化碳而呈酸性,燃油汽车的使用会产生二氧化碳、氮氧化物等酸性气体,从而使降水的pH降低,pH小于5.6的降水称为酸雨。(1)、自然降水呈酸性的原因是。(2)、使用纯电动汽车减少排放,符合环保。(3)、小明想通过如图所示的实验寻找蒸馏水变成酸雨的证据,你认为下一步的实验操作是:。