天津市红桥区2022年中考二模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 生活中充满着变化,下列变化属于化学变化的是( )A、葡萄酿酒 B、玻璃破碎 C、酒精挥发 D、蜡烛熔化2. 为了防止身体贫血,人体需要摄入的元素是( )A、Fe B、Na C、Ca D、Cl3. 纳米医学上可用四氯金酸(HAuCl4)制备包裹药物的外壳,四氯金酸中氯元素的化合价为-1价,则金元素的化合价为( )A、+2 B、+3 C、+4 D、+54. 实验是化学学习的基本方法,下列化学实验操作正确的是( )A、熄灭酒精灯
 B、称量氢氧化钠
B、称量氢氧化钠  C、滴加溶液
C、滴加溶液  D、稀释浓硫酸
D、稀释浓硫酸  5. 下列食物主要为人体提供蛋白质的是( )A、米饭 B、鸡蛋 C、牛油 D、蔬菜6. 下列有关燃烧和灭火说法正确的是( )A、油锅着火后向锅中放入菜叶目的是降低油的着火点 B、家用煤加工成蜂窝煤是力了增大煤与氧气的接触面积 C、高层建筑物起火立即乘电梯撤离 D、不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火7. 氮化镓是生产5G芯片的关键材料之一、氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是( )
5. 下列食物主要为人体提供蛋白质的是( )A、米饭 B、鸡蛋 C、牛油 D、蔬菜6. 下列有关燃烧和灭火说法正确的是( )A、油锅着火后向锅中放入菜叶目的是降低油的着火点 B、家用煤加工成蜂窝煤是力了增大煤与氧气的接触面积 C、高层建筑物起火立即乘电梯撤离 D、不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火7. 氮化镓是生产5G芯片的关键材料之一、氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是( ) A、镓是金属元素 B、氮原子的核内质子数为7 C、镓元素的相对原子质量是69.72g D、氮化镓中氮元素的化合价为-3价8. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A、镓是金属元素 B、氮原子的核内质子数为7 C、镓元素的相对原子质量是69.72g D、氮化镓中氮元素的化合价为-3价8. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生气泡,Y不反应;如果把Y和Z分别放入硝酸银溶液中,在Y表面有银白色物质析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
A、X、Y、Z B、Z、Y、X C、Y、X、Z D、X、Z、Y9. 下列有关实验现象的描述,正确的是( )A、打开浓盐酸的瓶盖,瓶口冒白烟 B、木炭燃烧生成二氧化碳 C、铁丝伸入盛有氧气的集气瓶中剧烈燃烧 D、硫燃烧生成有刺激性气味的气体10. 现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B的质量比是( )A、20:11 B、20:7 C、5:4 D、16:1111. 我国发明的新型钛合金,为“奋斗者”号下潜万米海底、从事科考任务解决了材料难题。工业制取金属钛的主要反应式是:①;②。下列说法合理的是( )A、FeTiO3属于氧化物 B、钛合金是一种金属单质 C、反应②属于置换反应 D、TiCl4中钛元素和氯元素的质量比为96:7112. 将一定量的铝粉投入到含溶质为Mg(NO3)2、Cu(NO3)2、AgNO3的溶液中,充分反应后过滤,滤液无色;向滤渣中滴加稀盐酸,无明显现象。下列说法错误的是( )A、滤渣中一定有Ag、Cu B、滤渣中一定有Ag,可能有Cu,没有Mg C、滤液中一定没有Cu(NO3)2、AgNO3 D、滤液中一定有Al(NO3)3、Mg(NO3)2二、多选题
-
13. 下列说法正确的是( )A、由不同种元素组成的物质一定是混合物 B、某物质能与碱反应生成盐和水,则该物质一定是酸 C、金属与盐溶液发生置换反应后,溶液的质量不一定增加 D、同一温度下,某物质的饱和溶液一定比其不饱和溶液的溶质质量分数大14. 下列各选项中,实验操作一定能够达到相应的实验目的的是( )
选项
实验目的
实验操作
A
验证氧气能支持燃烧
把带火星的木条伸到盛有氧气的集气瓶中
B
验证二氧化碳与水反应生成碳酸
向收集满二氧化碳的集气瓶中加入约1/3体积的滴有酚酞的水,振荡
C
探究稀硫酸与氢氧化钠溶液恰好完全反应
向稀硫酸与氢氧化钠溶液反应后所得的溶液中滴加硝酸钡溶液
D
探究人体吸入的空气与呼出的气体中二氧化碳含量的不同
常温下,同时分别向同体积的盛有空气样品和呼出气体样品的集气瓶中滴加相同滴数的饱和澄清石灰水,振荡
A、A B、B C、C D、D15. 某样品,可能含有、、、NaCl中的几种杂质,取该样品6.9g,加入50g稀盐酸中,恰好完全反应得到无色溶液,同时产生2.2g气体。下列判断错误的是( )A、反应后得到无色溶液,说明样品中一定没有 B、NaCl不与盐酸反应,说明样品中一定没有NaCl C、所加稀盐酸中溶质的质量分数为7.3% D、和都能和稀盐酸反应生成气体,说明样品中一定有、三、填空题
-
16. 请从下列物质中选择合适的物质,用相应序号填空。
①氧气 ②氢气 ③小苏打 ④碳酸钙 ⑤氯化钠 ⑥硝酸钾
(1)、最清洁的燃料是。(2)、属于复合肥料的是。(3)、可用作补钙剂的是。(4)、厨房里常用的调味品是。17. 构成物质的粒子之间的关系如图所示。回答下列问题: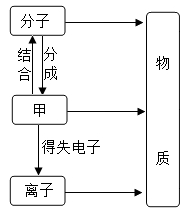 (1)、甲是;(2)、在水,汞和氯化钠三种物质中,由离子构成的物质是保持水化学性质的最小粒子是。(3)、图一为五种粒子的结构示意图。
(1)、甲是;(2)、在水,汞和氯化钠三种物质中,由离子构成的物质是保持水化学性质的最小粒子是。(3)、图一为五种粒子的结构示意图。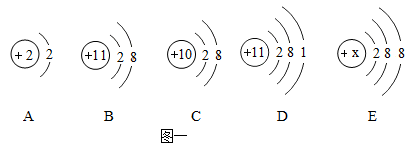
①A~D四种粒子中属于同种元素的是(填字母序号,下同),具有相对稳定结构的原子是。
②若E为某原子得到一个电子形成的离子,则x的数值是。
(4)、碳化硅(SiC)广泛应用于功能陶瓷。在高温下,可以用二氧化硅()和石墨粉反应制取碳化硅,同时生成一种可燃性气体,该反应的化学方程式为。18. 构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络(其中A、B表示反应物,C表示生成物)。请完成下列问题:
 (1)、如用湿润的pH试纸测定盐酸的pH,则结果会(填“偏大”“偏小”或“无影响”)。(2)、图1中①的现象是。(3)、世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的(填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的(填序号“②”“③”④”或“⑤”)化学性质。(4)、小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是(用符号表示),该反应的微观实质可表示为 , 依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为。(5)、图1中⑤的性质可用于除铁锈,反应的化学方程式为。19. 写出下列反应的化学方程式:(1)、硫在氧气中燃烧;(2)、锌片浸入硫酸铜溶液中;(3)、过氧化氢溶液中加入少量二氧化锰制取氧气。20. 数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
(1)、如用湿润的pH试纸测定盐酸的pH,则结果会(填“偏大”“偏小”或“无影响”)。(2)、图1中①的现象是。(3)、世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的(填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的(填序号“②”“③”④”或“⑤”)化学性质。(4)、小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是(用符号表示),该反应的微观实质可表示为 , 依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为。(5)、图1中⑤的性质可用于除铁锈,反应的化学方程式为。19. 写出下列反应的化学方程式:(1)、硫在氧气中燃烧;(2)、锌片浸入硫酸铜溶液中;(3)、过氧化氢溶液中加入少量二氧化锰制取氧气。20. 数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:温度/℃
0
10
20
30
40
50
60
70
溶解度/g
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
118
KCl
17.6
31.1
34.0
37.0
40.0
42.6
45.5
48.3
(1)、20℃时,KCl的溶解度为:;(2)、分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度,则温度取值范围是。(3)、40℃时,将140gKCl的饱和溶液恒温蒸发10g水后,析出KCl晶体的质量为g。(4)、要使KNO3物质的不饱和溶液转化为饱和溶液,方法是。(5)、30℃时,将40gKCl加到100g水中所形成溶液的溶质质量分数为。(6)、将60℃时KNO3和KCl的饱和溶液降温至20℃,析出晶体质量关系为。
A.KNO3>KCl B.KNO3<KCl C.KNO3=KCl D.无法确定21. 取一定质量的CaCO3高温灼烧一定时间,测得反应后剩余固体质量为8g,其中钙元素质量分数为50%,则反应放出CO2的质量为g。22. 李兰娟院士的研究团队发现:达芦那韦(化学式C27H37N3O7S)能显著抑制新冠肺炎病毒复制。按要求计算:(1)、达芦那韦属于(“无机化合物”或“有机化合物”);(2)、达芦那韦中氮元素与氧元素的质量比;(3)、g达芦那韦(化学式C27H37N3O7S)含氮元素的质量为21g。四、综合题
-
23. 图中的物质均为初中化学常见的物质。其中甲、乙、丙、丁、戊均为单质,丙是一种黄绿色有毒气体,是由17号元素组成的双原子分子,丁是黑色固体,G为体内胃酸主要成分,戊是紫红色金属;常温下A是液态,农业上常用F改良酸性土壤(图中部分反应条件已略)回答问题:
 (1)、D的俗称为;B为(填化学式);(2)、H和E反应生成C和戊的化学方程式为:;(3)、G和H发生反应生成A和J的反应类型为反应;(4)、工业上常用丙和F制漂白粉[CaCl2和Ca(ClO)2],同时生成A.请写出该反应的化学方程式。(5)、D和A反应热量。(填“吸收”或“放出”)24. 根据下列实验装置图,按要求回答有关问题:
(1)、D的俗称为;B为(填化学式);(2)、H和E反应生成C和戊的化学方程式为:;(3)、G和H发生反应生成A和J的反应类型为反应;(4)、工业上常用丙和F制漂白粉[CaCl2和Ca(ClO)2],同时生成A.请写出该反应的化学方程式。(5)、D和A反应热量。(填“吸收”或“放出”)24. 根据下列实验装置图,按要求回答有关问题: (1)、写出图中带有标号仪器的名称:a。(2)、实验室用大理石和稀盐酸制取并收集二氧化碳应选用的装置(填序号),化学方程式为 , 检验二氧化碳已经收集滴的方法是。(3)、实验室用加热氯酸钾和二氧化锰混合物的方法制取并收集较干燥的氧气时,应选用的收集装置是(填序号),反应的化学方程式为;若实验室用加热高锰酸钾的方法制取并用排水法收集氧气,停止加热时,应先将导管移出水面。然后再。25. 某校毕业班同学准备进行化学技能操作考试实验时,发现实验台上摆放的药品中,有一装有溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究。
(1)、写出图中带有标号仪器的名称:a。(2)、实验室用大理石和稀盐酸制取并收集二氧化碳应选用的装置(填序号),化学方程式为 , 检验二氧化碳已经收集滴的方法是。(3)、实验室用加热氯酸钾和二氧化锰混合物的方法制取并收集较干燥的氧气时,应选用的收集装置是(填序号),反应的化学方程式为;若实验室用加热高锰酸钾的方法制取并用排水法收集氧气,停止加热时,应先将导管移出水面。然后再。25. 某校毕业班同学准备进行化学技能操作考试实验时,发现实验台上摆放的药品中,有一装有溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究。
(提出问题)这瓶溶液是什么溶液?
(1)、(交流讨论)根据受损标签的情况判断,这瓶溶液不可能是___________(填序号)。A、酸溶液 B、碱溶液 C、盐溶液(获得信息)
(2)、Ⅰ、酸、碱、盐的性质实验中用到含钠元素的物质是氯化钠、氢氧化钠、碳酸钠和碳酸氢钠。Ⅱ、室温(20℃)时,四种物质的溶解度数据如下表:
物质
NaCl
NaOH
Na2CO3
NaHCO3
溶解度/g
36
109
215
9.6
Ⅲ、NaCl、BaCl2的水溶液呈中性。
(提出猜想)这瓶溶液可能是:
猜想一:氯化钠溶液
猜想二:碳酸钠溶液
猜想三:氢氧化钠溶液
猜想四:碳酸氢钠溶液
经过讨论,大家认为猜想不合理,理由是。
(3)、(实验推断)①小丽用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则这瓶溶液不可能是 , 理由是。
②小明取样滴加过量的BaCl2溶液并不断振荡,观察到有沉淀产生,该反应的化学方程式为 , 静置后,取少许上层清液,滴入酚酞溶液,振荡后无明显现象。则这瓶溶液的原溶液可能是。
(4)、(实验反思)实验室中,存取液体药品应注意(写一点即可)。五、计算题
-
26. 纯碱样品中含有少量的氯化钠,某同学为测定该纯碱样品中碳酸钠的含量,他取该纯碱样品11g,全部溶解在100g水中,再加入150.7g氯化钡溶液,恰好完全反应,过滤,得到19.7g沉淀(不考虑过程中物质质量的损失).请计算:(1)、纯碱样品中碳酸钠的质量;(2)、所加氯化钡溶液的溶质质量分数:(计算结果保留到0.1%)(3)、反应后所得溶液中溶质的质量分数.