天津市河西区2022年中考一模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 天津博物院馆藏丰富。下列文物制作过程中一定发生化学变化的是( )A、玉石雕琢 B、合金造币 C、青铜冶炼 D、笔墨作画2. 下列人体常用抗酸剂中,属于氧化物的是( )A、Al(OH)3 B、CaCO3 C、NaHCO3 D、MgO3. 下列食品中富含蛋白质的是( )A、菠菜 B、馒头 C、鸡蛋 D、西红柿4. 下列物质中,属于纯净物的是( )A、液氮 B、食盐水 C、功能饮料 D、清洁空气5. 月季花瓣可制酸碱指示剂,用于检验白醋的酸碱性。下列实验操作正确的是( )A、研磨花瓣
 B、浸取色素
B、浸取色素  C、取用白醋
C、取用白醋  D、检验白醋
D、检验白醋  6. 如图为某品牌矿泉水标签的部分内容。下列说法错误的是( )
6. 如图为某品牌矿泉水标签的部分内容。下列说法错误的是( ) A、“钾、钠、锶”指的是元素 B、该矿泉水显中性 C、H2SiO3属于酸 D、该矿泉水是混合物7. 下列说法中,正确的是( )A、油锅着火可用水灭火 B、农药本身有毒,应该全面禁止使用 C、稀释浓硫酸时,将水注入浓硫酸中 D、污染的酸性废水可以加入熟石灰中和8. 下列有关实验现象的描述错误的是( )A、细铁丝在空气中剧烈燃烧,生成黑色固体 B、红磷在空气中燃烧产生大量的白烟 C、木炭在氧气中燃烧,生成能使澄清石灰水变浑浊的气体 D、镁条在空气中燃烧发出耀眼的白光,生成白色固体9. 下列事实的微观解释中,错误的是( )A、品红在水中扩散——分子在不断地无规则运动 B、氧气和液氧都能支持燃烧——分子相同,其化学性质相同 C、蔗糖放入水中溶解——蔗糖分子在水中分解 D、氮气用作焊接金属时的保护气——氮气分子的化学性质稳定10. 氨气与氧气一定条件下生成 X 和 Y,反应前后微观示意图如图所示。下列说法正确的是( )
A、“钾、钠、锶”指的是元素 B、该矿泉水显中性 C、H2SiO3属于酸 D、该矿泉水是混合物7. 下列说法中,正确的是( )A、油锅着火可用水灭火 B、农药本身有毒,应该全面禁止使用 C、稀释浓硫酸时,将水注入浓硫酸中 D、污染的酸性废水可以加入熟石灰中和8. 下列有关实验现象的描述错误的是( )A、细铁丝在空气中剧烈燃烧,生成黑色固体 B、红磷在空气中燃烧产生大量的白烟 C、木炭在氧气中燃烧,生成能使澄清石灰水变浑浊的气体 D、镁条在空气中燃烧发出耀眼的白光,生成白色固体9. 下列事实的微观解释中,错误的是( )A、品红在水中扩散——分子在不断地无规则运动 B、氧气和液氧都能支持燃烧——分子相同,其化学性质相同 C、蔗糖放入水中溶解——蔗糖分子在水中分解 D、氮气用作焊接金属时的保护气——氮气分子的化学性质稳定10. 氨气与氧气一定条件下生成 X 和 Y,反应前后微观示意图如图所示。下列说法正确的是( )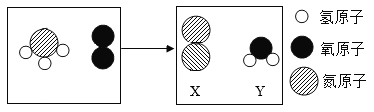 A、该反应属于复分解反应 B、化学变化中分子和原子均可再分 C、反应后生成 X 和 Y 的分子个数比是 1:1 D、若消耗 6.8g 氨气,生成 Y 的质量 10.8g11. 下列物质鉴别方法不可行的是( )A、肥皂水鉴别硬水与软水 B、稀硫酸鉴别黑色的氧化铜与铁粉 C、用燃烧的木条鉴别 N2与 CO2 D、用灼烧闻气味的方法鉴别羊毛和棉线12. 钛合金有良好的耐热强度、低温韧性。生产金属钛的步骤主要有:①在高温下,向金红石(含 TiO2)与焦炭的混合物中通入氯气,得到 TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用 Mg 与 TiCl4反应得到 Ti 和 MgCl2。下列说法错误的是( )A、①中的反应为 B、反应②中稀有气体的作用是防止 Mg 与空气反应 C、可用反应①产生的气体冶炼金属 D、反应①、②中的钛元素化合价未发生改变13. 物质可按单质、氧化物、酸、碱、盐、有机物分类。下图中甲、乙、丙、丁是四种不同类别的物质,短线相连物质之间均能发生化学反应。下列说法中符合图示要求的是( )
A、该反应属于复分解反应 B、化学变化中分子和原子均可再分 C、反应后生成 X 和 Y 的分子个数比是 1:1 D、若消耗 6.8g 氨气,生成 Y 的质量 10.8g11. 下列物质鉴别方法不可行的是( )A、肥皂水鉴别硬水与软水 B、稀硫酸鉴别黑色的氧化铜与铁粉 C、用燃烧的木条鉴别 N2与 CO2 D、用灼烧闻气味的方法鉴别羊毛和棉线12. 钛合金有良好的耐热强度、低温韧性。生产金属钛的步骤主要有:①在高温下,向金红石(含 TiO2)与焦炭的混合物中通入氯气,得到 TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用 Mg 与 TiCl4反应得到 Ti 和 MgCl2。下列说法错误的是( )A、①中的反应为 B、反应②中稀有气体的作用是防止 Mg 与空气反应 C、可用反应①产生的气体冶炼金属 D、反应①、②中的钛元素化合价未发生改变13. 物质可按单质、氧化物、酸、碱、盐、有机物分类。下图中甲、乙、丙、丁是四种不同类别的物质,短线相连物质之间均能发生化学反应。下列说法中符合图示要求的是( ) A、当甲、乙、丙分别为酸、碱、盐时,丁可以为 CuO B、当甲为硫酸铜时,丁可以为氢氧化钠 C、当丁为氧气时,甲、乙、丙可以为白磷、葡萄糖、一氧化碳 D、当丁为稀硫酸时,甲、乙、丙可以为碳、硝酸银、氢氧化钙
A、当甲、乙、丙分别为酸、碱、盐时,丁可以为 CuO B、当甲为硫酸铜时,丁可以为氢氧化钠 C、当丁为氧气时,甲、乙、丙可以为白磷、葡萄糖、一氧化碳 D、当丁为稀硫酸时,甲、乙、丙可以为碳、硝酸银、氢氧化钙二、多选题
-
14. 下列除杂方法(括号内为杂质)中正确的是( )
选项
实验组别
实验方案
A
溶液:硝酸铜(硝酸银)
加入足量的铁粉,过滤
B
气体:一氧化碳(二氧化碳)
先通入足量的氢氧化钠溶液,再通入足量的浓硫酸
C
固体:碳酸钙(氯化钙)
加入足量的水溶解,过滤、洗涤、干燥
D
金属:铁(铜)
加入过量的稀盐酸、过滤、洗涤、干燥
A、A B、B C、C D、D15. 下列说法中正确的是( )A、常温下将 5.6 g 生石灰溶解在 94.4 g水中,所得溶液中溶质质量分数等于7.4% B、等质量的质量分数均为 4% 氢氧化钠溶液与稀盐酸充分反应,所得溶液显酸性 C、将 6 g 碳放在盛有 12 g 氧气的密闭容器中燃烧,两者充分反应后,密闭容器中的气体物质是纯净物 D、将某镁铝合金和足量的稀盐酸反应生成H2为 0.4 g,则该合金的质量可能是 4 g三、填空题
-
16. 化学就在我们身边,人类的生活离不开化学。现有①维生素 C ②钛合金 ③二氧化碳 ④碳酸氢钠 ⑤医用酒精 ⑥点燃的蜡烛,选择适当的物质填空(填序号)。(1)、健康:食用预防坏血病; 可用擦拭皮肤消毒。(2)、医疗:可用治疗胃酸过多;可用制造人造骨骼。(3)、安全:常用灭火急救; 可用探查废弃地窖。17. 化学是在分子、原子层次上研究物质的科学。(1)、从微观上看,石墨、金刚石都是由(填“分子”、“原子”或“离子”或“元素”)构成;宏观上性质二者差异很大,有优良的导电性能。(2)、袁隆平成功培育出了适宜在盐碱地上种植富含硒“海水稻”。元素周期表中硒元素的有关信息如右下图所示,下列说法正确的是____(填字母)。
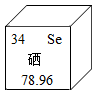 A、硒是金属元素 B、硒的原子序数是 34 C、硒的相对原子质量是 78.96g D、硒原子中的中子数是 34(3)、下列示意图表示的粒子中,元素的化学性质相似的是(填字母);属于同种元素的是(填字母);D 与 A 可以形成化合物 M,M 是学校、家庭常用的消毒药品,D 与 A 二种元素质量比为 71:64,则 M 是(填化学式)。
A、硒是金属元素 B、硒的原子序数是 34 C、硒的相对原子质量是 78.96g D、硒原子中的中子数是 34(3)、下列示意图表示的粒子中,元素的化学性质相似的是(填字母);属于同种元素的是(填字母);D 与 A 可以形成化合物 M,M 是学校、家庭常用的消毒药品,D 与 A 二种元素质量比为 71:64,则 M 是(填化学式)。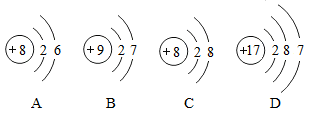 18. 习近平总书记在推进南水北调工程座谈会上强调:水是生存之本、文明之源。(1)、水(填“属于”、“不属于”)六大营养素。(2)、如图是电解水的实验示意图,试管(填“a”或“b”)中的气体可以做气体燃料,电解水的化学方程式为。
18. 习近平总书记在推进南水北调工程座谈会上强调:水是生存之本、文明之源。(1)、水(填“属于”、“不属于”)六大营养素。(2)、如图是电解水的实验示意图,试管(填“a”或“b”)中的气体可以做气体燃料,电解水的化学方程式为。 (3)、天然水净化为自来水的主要流程如下图所示:
(3)、天然水净化为自来水的主要流程如下图所示:
① “沉淀池”中可用明矾作絮凝剂,化学式为 KAl(SO4)n•12H2O,n 的值为。
② “吸附池”中常用(填物质名称)吸附色素和异味。
③ “消毒池”中常用液氯作消毒剂,发生了反应:。若用自来水直接配制硝酸银溶液,会产生沉淀(填化学式)。
④次氯酸(HClO)可除去废水中的 NH3 , 产物有盐酸和单质气体生成,该气体常用作食品保鲜填充气,该气体为(填化学式)。
19. 溶液与人类生产、生活密切相关。(1)、在盛有水的烧杯中加入以下物质,能形成无色溶液的是____(填序号)。A、氯化铁 B、小苏打 C、硫酸铜 D、高锰酸钾(2)、下列各组白色固体不能用水区分的是____(填序号)。A、氯化银、硫酸钡 B、生石灰、石灰石 C、淀粉、白糖 D、氯化钠、硝酸铵(3)、甲、乙、丙三种固体物质的溶解度曲线如下图所示,回答下列问题。
① 在 t1℃时,甲和丙两种物质的溶解度都是g。
② t2℃时分别把 10g 甲、乙、丙加入50g 水中,能形成饱和溶液的是。
③ t2℃时,从 50g 甲的饱和溶液中取出 10g,加 10g 水,此时所得溶液的溶质与溶液质量比。
④ 甲中混有少量的乙,提纯甲可采用的方法是。
⑤ 将 t2℃时等质量的甲、乙、丙三种物质的饱和溶液分别降温到 t1℃,对所得溶液的分析正确的是(填序号)。
A.溶解度 乙>甲>丙 B.溶剂质量 甲=丙=乙
C.溶液质量 丙>乙>甲 D.溶质质量分数 甲=丙<乙
20. 金属在生产、生活中有非常广泛的应用。(1)、我国三星堆遗址发掘现场出土了华丽的鸟型薄片金饰,是因为金具有良好的;(填“延展性”、“导电性”、“导热性”);钢是铁碳合金,钢属于材料(填“金属”、“合成”或“非金属”)。(2)、钢铁产量中国已多年位居世界第一、写出氧化铁与一氧化碳在高温下反应的化学方程式。(3)、向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤,得到滤渣和滤液。①在滤液中加入一枚洁净的铁钉,发现铁钉表面无明显现象,则滤液中一定大量含有的阳离子是(填离子符号)。
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有(填化学式)。
(4)、将 3.8g 锌、铝、铁的混合物与一定质量的溶质质量分数为 25%的稀硫酸恰好完全反应,将反应后的混合物蒸干得到固体(无结晶水)11g,则反应中生成的氢气质量是g。21. 天然气(主要成分为CH4)是一种重要的清洁燃料,我国“西气东输”工程利于能源和产业结构调整,极大改善了沿线居民生活质量。(1)、CH4完全燃烧的化学方程式是;该过程(填“释放”或“吸收”)能量。(2)、天然气使用可有效减少煤燃烧时形成的酸雨,下列现象与酸雨无关的是____。A、石刻文物被腐蚀 B、全球海平面上升 C、土壤酸化严重(3)、工业上以CH4为原料生产H2 , 制取原理如下图所示: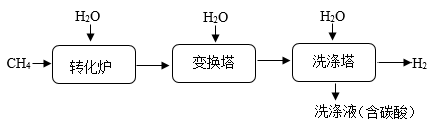
已知:变换塔中发生的反应:
①“转化炉”中有H2产生,参加反应的CH4与H2O的质量比。(填最简比)
②“洗涤塔”中水的作用。
四、综合题
-
22. 写出下列反应方程式。(1)、实验室制取二氧化碳;(2)、硫在氧气中燃烧;(3)、加热氯酸钾和二氧化锰混合物制氧气。23. 下图是实验室常用的某些实验装置,请回答下列问题。
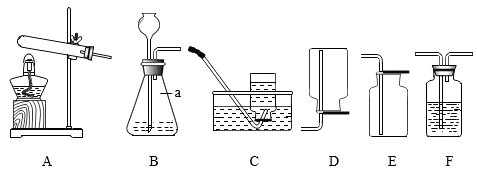 (1)、图中仪器a的名称为。(2)、用装置B制取氧气,反应的化学方程式为;若用此法制备并收集干燥的氧气,则装置的连接顺序为B→F→ , F中盛放的试剂是(填试剂名称)。(3)、若用装置A、F进行碳还原氧化铜的实验,并检验反应的产物。装置F中应盛放的试剂是溶液(填化学式),反应过程中,装置A内的现象为。24. 取敞口放置在空气中一段时间的氢氧化钠溶液于烧杯中,加入一定量的稀硫酸充分反应后得溶液M。某实验小组为探究反应后M溶液的成分,进行了如下实验:(所加试剂均足量、BaCl2溶液呈中性)
(1)、图中仪器a的名称为。(2)、用装置B制取氧气,反应的化学方程式为;若用此法制备并收集干燥的氧气,则装置的连接顺序为B→F→ , F中盛放的试剂是(填试剂名称)。(3)、若用装置A、F进行碳还原氧化铜的实验,并检验反应的产物。装置F中应盛放的试剂是溶液(填化学式),反应过程中,装置A内的现象为。24. 取敞口放置在空气中一段时间的氢氧化钠溶液于烧杯中,加入一定量的稀硫酸充分反应后得溶液M。某实验小组为探究反应后M溶液的成分,进行了如下实验:(所加试剂均足量、BaCl2溶液呈中性) (1)、气体B是(填化学式)。(2)、固体甲与硝酸反应的化学方程式是。(3)、溶液M的溶质是。(4)、滤液A中氯化钠的质量g。
(1)、气体B是(填化学式)。(2)、固体甲与硝酸反应的化学方程式是。(3)、溶液M的溶质是。(4)、滤液A中氯化钠的质量g。五、计算题
-
25. 按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管。环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。(1)、纤维素是一种(选填“有机物”或“无机物”)。(2)、纤维素分子中,氢、氧原子的个数比为。(3)、计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?26. 为了测定铜锌样品中铜的质量分数,取20g该样品向其中加入一定量的10%的稀硫酸,恰好完全反应,产生氢气0.2g。计算:(1)、该合金样品中铜的质量分数;(2)、反应后所得溶液中溶质的质量分数。(结果保留到0.1%)