天津市东丽区2022年中考二模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、食物腐败 B、西瓜榨汁 C、冰雪融化 D、湿衣晾干2. 空气成分中,体积分数最大的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体3. 下列物质中,属于单质的是( )A、H2O B、Fe2O3 C、Na2CO3 D、O24. 下列图示的操作中错误的是( )A、
 闻气体气味
B、
闻气体气味
B、 称固体质量
C、
称固体质量
C、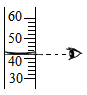 读液体体积
D、
读液体体积
D、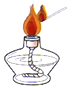 点燃酒精灯
5. 2021年10月16日神舟十三号载人飞船发射成功,开始中国迄今为止时间最长的载人飞行。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2 , 已知NiFe2O4中Fe为+3价,则Ni的化合价为( )A、+1 B、+2 C、+3 D、+46. 厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生,这种气体是()A、二氧化碳 B、氧气 C、氢气 D、二氧化硫7. 化学反应往往伴随着一定的现象,下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、铁丝在空气中燃烧,火星四射,生成黑色固体 C、向氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 D、硫在空气中燃烧产生明亮的蓝紫色火焰8. 生活中某些物质的pH范围如下,其中碱性最强的是( )A、酱油4~5 B、蛋清7~8 C、牙膏8~9 D、肥皂水10~119. 铼被广泛应用于航空航天领域。如图是元素周期表中铼元素的信息示意图,对图中信息理解错误的是( )
点燃酒精灯
5. 2021年10月16日神舟十三号载人飞船发射成功,开始中国迄今为止时间最长的载人飞行。太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2 , 已知NiFe2O4中Fe为+3价,则Ni的化合价为( )A、+1 B、+2 C、+3 D、+46. 厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生,这种气体是()A、二氧化碳 B、氧气 C、氢气 D、二氧化硫7. 化学反应往往伴随着一定的现象,下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、铁丝在空气中燃烧,火星四射,生成黑色固体 C、向氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 D、硫在空气中燃烧产生明亮的蓝紫色火焰8. 生活中某些物质的pH范围如下,其中碱性最强的是( )A、酱油4~5 B、蛋清7~8 C、牙膏8~9 D、肥皂水10~119. 铼被广泛应用于航空航天领域。如图是元素周期表中铼元素的信息示意图,对图中信息理解错误的是( ) A、质子数为75 B、元素符号为Re C、核外电子数为186.2 D、元素名称为铼10. 某纯净物R常温下即可分解,生成NH3、H2O和CO2。根据这一事实,下列的推理中,错误的是( )A、R中一定含有氮元素 B、R中一定含有水 C、R一定为化合物 D、R的化学性质不稳定11. 证据推理是化学学科核心素养的重要内容。下列推理正确的是( )A、酸雨的pH<7,所以pH<7的雨水一定是酸雨 B、单质只含有一种元素,则只含有一种元素的物质一定是单质 C、碱性溶液能使无色酚酞试液变红色,所以碳酸钠溶液也能使无色酚酞试液变红色 D、中和反应能够生成盐和水,所以能够生成盐和水的反应一定是中和反应
A、质子数为75 B、元素符号为Re C、核外电子数为186.2 D、元素名称为铼10. 某纯净物R常温下即可分解,生成NH3、H2O和CO2。根据这一事实,下列的推理中,错误的是( )A、R中一定含有氮元素 B、R中一定含有水 C、R一定为化合物 D、R的化学性质不稳定11. 证据推理是化学学科核心素养的重要内容。下列推理正确的是( )A、酸雨的pH<7,所以pH<7的雨水一定是酸雨 B、单质只含有一种元素,则只含有一种元素的物质一定是单质 C、碱性溶液能使无色酚酞试液变红色,所以碳酸钠溶液也能使无色酚酞试液变红色 D、中和反应能够生成盐和水,所以能够生成盐和水的反应一定是中和反应二、多选题
-
12. 下列不属于氢氧化钠俗称的是。( )A、纯碱 B、火碱 C、苛性钠 D、小苏打13. 下列实验方法能达到实验目的的是( )
选项
实验目的
实验操作或试剂
A
除去CuSO4溶液中的少量Na2SO4
加入适量的BaCl2溶液
B
提纯含有少量NaCl的KNO3
冷却热的饱和溶液,过滤、洗涤、干燥
C
比较人体吸入气体和呼出气体中CO2的含量
将带火星的木条分别插入两种气体中
D
检验氢氧化钠是否部分变质
滴加CaCl2溶液
A、A B、B C、C D、D14. 甲、乙、丙、丁四种物质间的反应如下图所示“—”表示相连的物质间在一定条件下可以反应,下列选项符合图示反应关系的是( )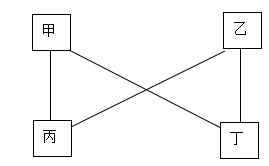
选项
甲
乙
丙
丁
A
Fe
CO
H2SO4
O2
B
Na2SO4
HCl
Ba(OH)2
BaCl2
C
Ca(OH)2
NaOH
CO2
CuCl2
D
C
CO
CuO
O2
A、A B、B C、C D、D15. 下列说法正确的是( )A、质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈酸性 B、质量比为2:1的K2HPO4和K2SO4中所含钾元素的质量分数相等 C、硝酸镁样品(含有一种杂质)14.8g,溶于水,与足量的NaOH溶液充分反应生成沉淀5.5g,则样品中可能含有的杂质是MgSO4 D、向一定量的氧化铁与氧化铜的混合物中加入100g质量分数为9.8%稀硫酸,恰好完反应,则原混合物中氧元素的质量是1.6g三、填空题
-
16. 化学就在我们身边。现有①不锈钢②干冰③KNO3④石墨⑤氦气⑥硫酸铜,选择适当的物质填空(填序号)。(1)、可用作电池电极的是。(2)、可用于制造电光源的是。(3)、可用于制炊具的是。(4)、可用于配制波尔多液的是。(5)、可用于人工降雨的是。(6)、属于复合肥料的是。17. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。(1)、图一为构成物质的粒子之间的关系。

图一中字母a代表 , 字母b代表。
(2)、结构决定性质,请根据下列粒子结构示意图给出的信息回答:
其中属于同种元素是(填序号),属于阴离子是(填序号),化学性质相似的是(填序号)
18. 水是维持生命活动最重要的物质。请完成下列问题。(1)、如图所示,试管b中产生的气体是(填化学式),电解水的化学方程式为。 (2)、硬水给生活和生产带来很多麻烦,生活中可用来区分硬水和软水。(3)、消防队员用高压水枪灭火,此措施依据的灭火原理是____(填序号)。A、降温到着火点以下 B、隔绝空气 C、清除可燃物(4)、二氧化氯(ClO2)是新一代饮用水的消毒剂,工业上制取二氧化氯的化学方程式为: ,其中X的化学式为。(5)、粗盐中含有少量CaCl2、MgCl2、Na2SO4和泥沙,某同学将该粗盐样品进行提纯。
(2)、硬水给生活和生产带来很多麻烦,生活中可用来区分硬水和软水。(3)、消防队员用高压水枪灭火,此措施依据的灭火原理是____(填序号)。A、降温到着火点以下 B、隔绝空气 C、清除可燃物(4)、二氧化氯(ClO2)是新一代饮用水的消毒剂,工业上制取二氧化氯的化学方程式为: ,其中X的化学式为。(5)、粗盐中含有少量CaCl2、MgCl2、Na2SO4和泥沙,某同学将该粗盐样品进行提纯。①将样品加适量水溶解,在粗盐溶液中依次加入稍过量的BaCl2溶液、NaOH溶液和溶液(填化学式)。
②充分反应后经过除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯净的氯化钠溶液。
19. 写出下列反应的化学方程式(1)、硫在氧气中燃烧。(2)、氢氧化镁和盐酸反应。(3)、实验室用过氧化氢溶液和二氧化锰制氧气。20. 溶液与人们的生产、生活密切相关。(1)、将下列物质放入水中,充分振荡,能形成溶液的是____(填序号)。A、植物油 B、碳酸钙 C、蔗糖 D、面粉(2)、用洗洁精洗刷碗筷油污,是利用了洗洁精的作用。(3)、如图是NaCl、KNO3的溶解度曲线。

①60℃时,NaCl的溶解度是g.
②向烧杯中加入100g水和49.0gKNO3固体配成40℃的溶液,再冷却到10℃,烧杯中析出的固体的质量为g。
③在60℃时,分别取XgNaCl和XgKNO3固体进行如下实验。加入甲烧杯中的固体是(填“NaCl”或“KNO3”),X的取值范围是。
(4)、在实验室中,欲配制溶质质量分数为16%的氯化钠溶液150g,需要称量氯化钠固体的质量为g,将上述150g氯化钠溶液稀释成溶质质量分数为12%的溶液,需要加入蒸馏水的质量为g。21. 人类生产、生活离不开化学。(1)、我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。①现阶段的能源结构仍以化石燃料为主,化石燃料包括、石油和天然气。
②下列燃料在O2中燃烧时,不会产生CO2的是(填序号)。
A.天然气 B.氢气 C.肼(N2H4)
③保护环境,实现碳达峰、碳中和,应从降低生活中的碳排放开始。下列做法不符合“低碳”要求的是(填序号)。
A.随手关闭电源 B.分类投放垃圾 C.随意露天烧烤 D.践行“光盘行动”
(2)、端午节吃粽子是我国的传统习俗,制作粽子的原料有:①糯米②大枣③瘦肉④加碘食盐等,原料中富含蛋白质的是(填序号)。(3)、工业燃煤会产生大气污染物二氧化硫,为减少空气污染,工业上将产生的二氧化硫与氧化钙、氧气共同反应生成硫酸钙,写出其反应的化学方程式。(4)、我国科学家将CO2合成淀粉。合成过程中碳原子变化:CO2→C1(有机物X)→C3→C6→Cn(即淀粉)其中CO2与H2反应制备有机物X的微观过程如图。下列有关说法错误的是____(填序号)。 A、图中单质的化学式为H2 B、反应前后原子的种类、数目、质量均不变 C、两种生成物都属于化合物 D、图中A物质由1个碳原子和2个氧原子构成22. 金属在生产、生活和航天发展中应用非常广泛。(1)、铜块能制成铜丝是利用了铜的性(填“导电”或“延展”)。(2)、近一百多年里,铝被广泛应用,原因之一是常温下铝具有很好的抗腐蚀性能,请解释原因(用化学方程式表示)。(3)、铝合金中包含铝、镁、铜三种金属,为验证这三种金属的活动性顺序,以下药品选择方法可行的是____(填序号)。A、铝、镁、铜、盐酸 B、铝、铜、氯化镁溶液 C、硫酸铝溶液、镁、铜 D、硫酸铝溶液、硫酸镁溶液、铜(4)、将一定质量的锌粉、铁粉混合物加入到Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤:①若滤液为无色,则滤渣中一定含有的金属为;②若向滤渣中滴加稀盐酸无气泡冒出,则滤液中至少含有种阳离子。(5)、已知氧化铁、氧化铜、氧化锌都在高温的条件下能和一氧化碳反应生成金属和二氧化碳。现有氧化铁、氧化铜、氧化锌的固体混合物粉末ag,在高温的条件下用足量的一氧化碳得到金属混合物4.82g,将生成的二氧化碳气体用足量的澄清石灰水吸收后,产生10g白色沉淀。则a的数值为g。
A、图中单质的化学式为H2 B、反应前后原子的种类、数目、质量均不变 C、两种生成物都属于化合物 D、图中A物质由1个碳原子和2个氧原子构成22. 金属在生产、生活和航天发展中应用非常广泛。(1)、铜块能制成铜丝是利用了铜的性(填“导电”或“延展”)。(2)、近一百多年里,铝被广泛应用,原因之一是常温下铝具有很好的抗腐蚀性能,请解释原因(用化学方程式表示)。(3)、铝合金中包含铝、镁、铜三种金属,为验证这三种金属的活动性顺序,以下药品选择方法可行的是____(填序号)。A、铝、镁、铜、盐酸 B、铝、铜、氯化镁溶液 C、硫酸铝溶液、镁、铜 D、硫酸铝溶液、硫酸镁溶液、铜(4)、将一定质量的锌粉、铁粉混合物加入到Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤:①若滤液为无色,则滤渣中一定含有的金属为;②若向滤渣中滴加稀盐酸无气泡冒出,则滤液中至少含有种阳离子。(5)、已知氧化铁、氧化铜、氧化锌都在高温的条件下能和一氧化碳反应生成金属和二氧化碳。现有氧化铁、氧化铜、氧化锌的固体混合物粉末ag,在高温的条件下用足量的一氧化碳得到金属混合物4.82g,将生成的二氧化碳气体用足量的澄清石灰水吸收后,产生10g白色沉淀。则a的数值为g。四、综合题
-
23. 实验室利用下图实验装置进行有关实验。请根据装置回答下列问题:
 (1)、写出图中仪器①的名称。(2)、实验室用高锰酸钾制取并收集氧气,应选用的装置为(填序号,在A~E中选取),反应的化学方程式为。(3)、实验室用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式为;若用装置F收集二氧化碳,验满时,燃着木条应放在(填“a”或“b”)端。24. 某固体混合物可能含有氢氧化钠、硝酸钠、氯化钠、硫酸钠、碳酸钠中的一种或几种。为了所究该混合物的成分,某同学按如图流程进行了实验《名步均恰好完全反应)。
(1)、写出图中仪器①的名称。(2)、实验室用高锰酸钾制取并收集氧气,应选用的装置为(填序号,在A~E中选取),反应的化学方程式为。(3)、实验室用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式为;若用装置F收集二氧化碳,验满时,燃着木条应放在(填“a”或“b”)端。24. 某固体混合物可能含有氢氧化钠、硝酸钠、氯化钠、硫酸钠、碳酸钠中的一种或几种。为了所究该混合物的成分,某同学按如图流程进行了实验《名步均恰好完全反应)。 (1)、过滤时,需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和(填仪器名称)。(2)、反应④的化学方程式为。(3)、根据图中实验现象推断,该混合物中一定有的物质是。①中加入适量稀盐酸后所得溶液中一定有的离子是。(4)、该同学为了进一步确定固体混合物的组成,取样品41.8g(其中含钠元素质量为13.8g),按上述流程图进行实验,产生23.3g白色沉淀A和4.4g气体W。通过计算,确定该混合物中还含有的物质是(填化学式)。
(1)、过滤时,需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和(填仪器名称)。(2)、反应④的化学方程式为。(3)、根据图中实验现象推断,该混合物中一定有的物质是。①中加入适量稀盐酸后所得溶液中一定有的离子是。(4)、该同学为了进一步确定固体混合物的组成,取样品41.8g(其中含钠元素质量为13.8g),按上述流程图进行实验,产生23.3g白色沉淀A和4.4g气体W。通过计算,确定该混合物中还含有的物质是(填化学式)。五、计算题
-
25. 2021年中国在全球范围内首次实现从一氧化碳到蛋白质的合成,并已形成万吨级工业产能。蛋白质是由多种氨基酸构成的极为复杂的化合物,丙氨酸(C3H7NO2)是多种氨基酸中的一种,(1)、丙氨酸由种元素组成的(填数字):(2)、丙氨酸中C、H、N、O的原子个数比为。(3)、丙氨酸中氮元素的质量分数为。(计算结果保留0.1%)26. 现有氯化钠和氯化镁混合物12.8g,向其中加入83g水,完全溶解后加入一定质量的氢氧化钠溶液,至恰好完全反应后,过滤,得到5.8g沉淀,所得滤液中溶质的质量分数为10%。计算:
混合物中氯化镁的质量;氢氧化钠溶液中溶质的质量分数(计算结果精确到0.1%)。