北京市燕山地区2022年中考二模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 空气中体积分数约为21%的气体是()A、氧气 B、氮气 C、二氧化碳 D、水蒸气2. 下列H2的性质中,属于化学性质的是( )A、难溶于水 B、无色气体 C、能燃烧 D、熔点低3. 下列金属活动性最强的是( )A、Cu B、Zn C、Fe D、Mg4. 75%的酒精溶液可杀灭“新冠病毒”,酒精溶液中的溶剂是( )A、水 B、乙醇 C、酒精 D、白酒5. 下列物质属于纯净物的是( )A、雪碧 B、牛奶 C、干冰 D、食醋6. 奶制品、豆类、虾皮等食物中含钙丰富,这里的“钙”是指( )A、钙元素 B、钙原子 C、钙离子 D、钙单质7. 下列实验操作中,错误的是( )A、
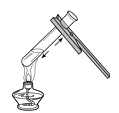 加热液体
B、
加热液体
B、 稀释浓硫酸
C、
稀释浓硫酸
C、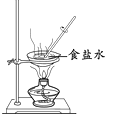 蒸发食盐水
D、
蒸发食盐水
D、 检查装置气密性
8. 下列图标中,表示“禁止烟火”的是( )A、
检查装置气密性
8. 下列图标中,表示“禁止烟火”的是( )A、 B、
B、 C、
C、 D、
D、 9. 下列物质在氧气中燃烧,产生大量白烟的是( )A、红磷 B、木炭 C、铁丝 D、氢气10. 下列做法不利于保护环境的是( )A、垃圾分类处理 B、乘坐公共交通工具 C、污水处理达标后排放 D、使用一次性塑料餐盒11. 下列符号中,表示2个氯原子的是( )
9. 下列物质在氧气中燃烧,产生大量白烟的是( )A、红磷 B、木炭 C、铁丝 D、氢气10. 下列做法不利于保护环境的是( )A、垃圾分类处理 B、乘坐公共交通工具 C、污水处理达标后排放 D、使用一次性塑料餐盒11. 下列符号中,表示2个氯原子的是( )
A、Cl2 B、2Cl2 C、2Cl D、2Cl-12. 下列化肥中,属于钾肥的是( )A、K2SO4 B、NH4NO3 C、CO(NH2)2 D、Ca(H2PO4)213. 下列化学反应中,属于置换反应的是( )A、 B、 C、 D、14. 下列物质中含氧分子的是( )A、H2O2 B、KMnO4 C、SO2 D、液态氧15. 如图为电解水的实验装置,下列说法正确的是( ) A、该实验可用于研究水的组成 B、正极所连的电极上产生的是氢气 C、a 中产生的气体可支持燃烧 D、实验过程中球形漏斗内液面高度不变16. 下列灭火方法错误的是( )A、电器起火—用水浇灭 B、森林起火—砍伐树木形成隔离带 C、油锅起火—用锅盖盖灭 D、图书起火—用二氧化碳灭火器灭火17. 下列关于N2 + O22NO的说法错误的是( )A、表示氮气和氧气在放电条件下反应生成一氧化氮 B、反应前后分子的数目不变 C、反应前后原子的种类、数目均不变 D、参加反应的氮气与生成的一氧化氮的质量比为14∶1518. 配制50g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )A、蒸发皿 B、玻璃棒 C、烧杯 D、量筒19. 某同学制作的试剂标签如下。其中化学式书写错误的是( )A、
A、该实验可用于研究水的组成 B、正极所连的电极上产生的是氢气 C、a 中产生的气体可支持燃烧 D、实验过程中球形漏斗内液面高度不变16. 下列灭火方法错误的是( )A、电器起火—用水浇灭 B、森林起火—砍伐树木形成隔离带 C、油锅起火—用锅盖盖灭 D、图书起火—用二氧化碳灭火器灭火17. 下列关于N2 + O22NO的说法错误的是( )A、表示氮气和氧气在放电条件下反应生成一氧化氮 B、反应前后分子的数目不变 C、反应前后原子的种类、数目均不变 D、参加反应的氮气与生成的一氧化氮的质量比为14∶1518. 配制50g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )A、蒸发皿 B、玻璃棒 C、烧杯 D、量筒19. 某同学制作的试剂标签如下。其中化学式书写错误的是( )A、 B、
B、 C、
C、 D、
D、 20. 下列物质的用途中,利用其化学性质的是( )A、铁用于制作铁锅 B、稀硫酸用于除铁锈 C、食盐用作调味品 D、稀有气体用于制造电光源21. 钛是一种广泛应用于航天和航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( )A、4 B、22 C、26 D、4822. 下列实验设计不能达到实验目的的是( )
20. 下列物质的用途中,利用其化学性质的是( )A、铁用于制作铁锅 B、稀硫酸用于除铁锈 C、食盐用作调味品 D、稀有气体用于制造电光源21. 钛是一种广泛应用于航天和航海工业的金属。已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( )A、4 B、22 C、26 D、4822. 下列实验设计不能达到实验目的的是( )选项
A
B
C
D
实验设计




实验目的
探究温度对分子运动速率的影响
验证CO2密度大于空气、不燃烧不支持燃烧
比较高锰酸钾在水和汽油中的溶解性
验证水是否是铁生锈的因素
A、A B、B C、C D、D23. 下列实验方法一定能达到实验目的的是( )A、鉴别硬水和软水——观察透明度 B、硬水软化成软水——用活性炭吸附 C、鉴别氧气和二氧化碳——伸入燃着的木条 D、除去硫酸铜溶液中的硫酸——加入铜粉24. KNO3的溶解度曲线如图所示。下列说法错误的是( ) A、0~60 ℃,KNO3的溶解度随温度升高而增大 B、60 ℃时,100 g 水中最多溶解110 g KNO3 C、20 ℃时,KNO3饱和溶液中溶质质量分数为31.6% D、将20 ℃的KNO3饱和溶液升温至60℃,溶液中溶质质量不变25. 北京冬奥会火种灯的火种燃料为丙烷。丙烷燃烧前后分子种类变化微观示意图如下、下列说法错误的是( )
A、0~60 ℃,KNO3的溶解度随温度升高而增大 B、60 ℃时,100 g 水中最多溶解110 g KNO3 C、20 ℃时,KNO3饱和溶液中溶质质量分数为31.6% D、将20 ℃的KNO3饱和溶液升温至60℃,溶液中溶质质量不变25. 北京冬奥会火种灯的火种燃料为丙烷。丙烷燃烧前后分子种类变化微观示意图如下、下列说法错误的是( ) A、乙为单质 B、丙的相对分子质量为44 C、生成丙与丁的分子个数比为3:4 D、丙烷由3个碳原子、8个氢原子构成
A、乙为单质 B、丙的相对分子质量为44 C、生成丙与丁的分子个数比为3:4 D、丙烷由3个碳原子、8个氢原子构成二、填空题
-
26. 松花蛋,是我国的特有食品。制作皮蛋的主要原料有新鲜鸭蛋、生石灰、食盐、纯碱、草木灰等。(1)、制作过程中生石灰与水发生反应的化学方程式为。(2)、纯碱的化学式是。(3)、用皮蛋可制成各种美食,皮蛋中主要含有的营养素是____(填序号)。A、蛋白质 B、糖类 C、水27. 填空:(1)、“碳达峰”、“碳中和”中的“碳”是指(填“碳元素”或“碳单质”)。(2)、化石燃料的燃烧是 CO2 的重要来源,化石燃料包括、石油和天然气。(3)、长征运载火箭使用了液氢和液氧作为推进剂,从微观的角度分析,氢气变为液氢时,变化的是。氢气燃烧的化学方程式。28. 如图为汽车安全气囊构造图,请回答下列问题。
 (1)、电子点火器中用铜作导线,利用了铜的延展性和性。(2)、安全气囊内的叠氮化钠 (NaN3) 受热分解产生两种单质,该化学方程式是。29. 硝酸(HNO3)是一种重要的化工原料,工业制硝酸的主要转化过程如下:
(1)、电子点火器中用铜作导线,利用了铜的延展性和性。(2)、安全气囊内的叠氮化钠 (NaN3) 受热分解产生两种单质,该化学方程式是。29. 硝酸(HNO3)是一种重要的化工原料,工业制硝酸的主要转化过程如下: (1)、①中反应的微观示意图如下,参加反应的 H2和 N2的质量比为。
(1)、①中反应的微观示意图如下,参加反应的 H2和 N2的质量比为。 (2)、上述制硝酸的主要转化过程中涉及到的氧化物有。(3)、硝酸(HNO3)中氮元素的化合价是。30. 下图是去除粗盐中难溶性杂质实验的三步操作。
(2)、上述制硝酸的主要转化过程中涉及到的氧化物有。(3)、硝酸(HNO3)中氮元素的化合价是。30. 下图是去除粗盐中难溶性杂质实验的三步操作。 (1)、三步操作的正确顺序是(填序号)。(2)、B中,用璃棒不断搅拌的目的是。31. 利用对比实验探究相关物质的性质。如图所示,充满二氧化碳气体的三个相同的软塑料瓶,分别加入等体积的三种不同物质,迅速盖紧瓶盖,振荡。
(1)、三步操作的正确顺序是(填序号)。(2)、B中,用璃棒不断搅拌的目的是。31. 利用对比实验探究相关物质的性质。如图所示,充满二氧化碳气体的三个相同的软塑料瓶,分别加入等体积的三种不同物质,迅速盖紧瓶盖,振荡。
资料:一:通常状况下,1 体积水约能溶解 1 体积二氧化碳。
二:20℃时,氢氧化钠的溶解度是 109g,氢氧化钙的溶解度是 0.173g。
(1)、实验中三个软塑料瓶变瘪的程度由大到小的顺序是。(填序号)(2)、B 瓶的现象:1 软塑料瓶变瘪 2。(3)、对比 A、C 瓶的现象证明。A 瓶中反应的化学方程式为。三、科普阅读题
-
32. 阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一
石墨是制铅笔芯的原料之一,在 16 世纪被发现后,曾被误认为是含铅的物质。直到 18世纪,化学家将石墨与 KNO3 共熔后产生 CO2,才确定了它是含碳的物质。
石墨烯一层层叠起来就是石墨,厚 1 毫米的石墨大约包含 300 万层石墨烯,具有优良的导电和光学性能。
碳纤维既有碳材料的本质特性,又有纺织纤维的柔软可加工性。目前把碳纤维应用于纸的制作,主要在功能纸上、研究人员通过实验研究了碳纤维含量与耐破度的关系,结果如图1 所示。
碳气凝胶也是新型碳材料,具有优良的吸附性能,在环境净化中发挥重要作用。科研人员在不同温度下制备了三种碳气凝胶样品,比较其对 CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图2。图中选择性值越高,表明碳气凝胶对 CO2的选择性吸附性能越好。


随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题。
(1)、石墨烯属于____(填序号)。A、非金属单质 B、有机化合物 C、金属单质(2)、石墨与 KNO3共熔,能发生如下反应,配平该反应的化学方程式:。(3)、配平化学方程式的理论依据是。(4)、判断下列说法的对错(填“对”或“错”)。①在实验研究的范围内,随着碳纤维含量的增大,无涂布纸耐破度增大。
②在一定条件下,石墨、石墨烯分别在氧气中充分燃烧,产物相同。
(5)、对比图 2 中三条曲线,得到的实验结论是。四、综合题
-
33. 回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下。

已知:
(1)、氧化铁与 A 反应的化学方程式为。(2)、固体 D 属于(填“纯净物”或“混合物”)。(3)、过程 III 的化学方程式是。34. 根据下图回答问题。 (1)、实验室用装置A制氧气,反应的化学方程式是。能用装置D收集氧气的原因是。(2)、实验室用装置B制二氧化碳,反应的化学方程式是。用装置C收集二氧化碳,验满的操作是。35. 用如图实验验证可燃物燃烧的条件。资料:红磷着火点为240 ℃,白磷着火点为40 ℃。
(1)、实验室用装置A制氧气,反应的化学方程式是。能用装置D收集氧气的原因是。(2)、实验室用装置B制二氧化碳,反应的化学方程式是。用装置C收集二氧化碳,验满的操作是。35. 用如图实验验证可燃物燃烧的条件。资料:红磷着火点为240 ℃,白磷着火点为40 ℃。 (1)、一段时间后,a处红磷不燃烧,b处白磷燃烧。
(1)、一段时间后,a处红磷不燃烧,b处白磷燃烧。①反应的化学方程式是。
②可验证可燃物燃烧的条件是。
(2)、要验证可燃物燃烧的另一个条件,c处的物质是。36. 管道疏通剂可以有效地疏通由毛发、油脂等各种原因引起的下水管道堵塞。某小组欲探究某品牌固体管道疏通剂中 Ca(OH)2、铝粉、缓蚀阻垢剂的用量对疏通效果的影响,寻找三者的最佳质量比;并探究该品牌管道疏通剂对下水管道的腐蚀情况。【查阅资料】Ca(OH)2与铝粉混合遇水后发生化学反应,放出大量热和气体,可加快疏通毛发等物质。反应的化学方程式为:。
【进行实验 1】按表中数据将各固体物质混合均匀后,加入 20 mL 水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
序号
Ca(OH)2质量/g
铝粉质量/g
缓蚀阻垢剂质量/g
混合前后温度升高值/℃
①
1.3
0.55
0.18
63
②
1.3
0.75
0.18
78
③
1.3
0.95
0.18
89
④
1.3
1.15
0.18
83
⑤
1.3
0.95
0.04
86
⑥
1.3
0.95
0.09
87
⑦
1.3
0.95
0.27
87
【解释与结论】
(1)、Ca(OH)2溶液的 pH7(填“<”、“>”或“=”)。(2)、Ca(AlO2)2中含有的金属元素是。(3)、实验①~④的目的是。(4)、欲探究缓蚀阻垢剂的用量对疏通效果的影响,需对比的实验是⑤、⑥、⑦和(填实验序号)。(5)、由实验 1 可知,Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为 1.3∶∶。(6)、【进行实验 2】在其他条件相同时。改变下水管道材料,测定管道疏通剂对各材料的腐蚀率。实验结果记录如下:材料
塑料
铜
铁
钢
铝
铝合金
腐蚀率
0.1%
0.4%
0.5%
0.3%
100%
80%
【解释与结论】
进行实验 2 时,除了控制下水管道材料的形状、大小相同,水的体积相同,腐蚀时间相同,还需要控制相同的是。
(7)、由实验 2 可得到的结论是。五、计算题
-
37. 在锌的冶炼方法中,主要反应之一。若参加反应的 ZnO的质量 81kg,计算制得 Zn 的质量(写出计算过程及结果)。
-