北京市顺义区2022年中考一模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 下列生产过程中,只发生物理变化的是( )A、酿酒
 B、炼铁
B、炼铁 C、伐薪
C、伐薪 D、烧炭
D、烧炭 2. 下列气体中,能供给动植物呼吸的是( )A、O2 B、H2 C、N2 D、CO23. 下列属于纯净物的是( )A、五氧化二磷 B、大理石 C、加碘食盐 D、食醋4. 下列物质的性质,属于化学性质的是( )A、颜色 B、密度 C、可燃性 D、导热性5. 下列食物富含蛋白质的是( )A、西瓜 B、鸡蛋 C、馒头 D、黄油6. 人体主要由C、H、O、N四种元素组成,它们的本质区别是( )A、质子数不同 B、电子数不同 C、中子数不同 D、最外层电子数不同7. 配制一定溶质质量分数的溶液,下列仪器不需要的是( )A、量筒
2. 下列气体中,能供给动植物呼吸的是( )A、O2 B、H2 C、N2 D、CO23. 下列属于纯净物的是( )A、五氧化二磷 B、大理石 C、加碘食盐 D、食醋4. 下列物质的性质,属于化学性质的是( )A、颜色 B、密度 C、可燃性 D、导热性5. 下列食物富含蛋白质的是( )A、西瓜 B、鸡蛋 C、馒头 D、黄油6. 人体主要由C、H、O、N四种元素组成,它们的本质区别是( )A、质子数不同 B、电子数不同 C、中子数不同 D、最外层电子数不同7. 配制一定溶质质量分数的溶液,下列仪器不需要的是( )A、量筒 B、胶头滴管
B、胶头滴管 C、烧杯
C、烧杯 D、漏斗
D、漏斗 8. 下列物质由离子构成的是( )A、Cu B、CO2 C、H2O D、NaCl9. 化学肥料对粮食增产起着重要作用,下列能作磷肥的是( )A、NH4HCO3 B、CO(NH2)2 C、Ca(H2PO4)2 D、KNO310. 下列关于物质用途的描述错误的是()A、氧气可用作燃料 B、二氧化碳可用作气体肥料 C、干冰可用于人工降雨 D、铜丝可用作导线11. 下列微粒中,能表示2个氢分子的是( )A、2H B、2H+ C、H2O D、2H212. 下列关于空气的说法正确的是( )A、空气由空气分子构成 B、N2、O2等均匀混合 C、N2、O2不再保持各自的化学性质 D、N2、O2的体积比约为5:113. 下列实验操作正确的是( )A、
8. 下列物质由离子构成的是( )A、Cu B、CO2 C、H2O D、NaCl9. 化学肥料对粮食增产起着重要作用,下列能作磷肥的是( )A、NH4HCO3 B、CO(NH2)2 C、Ca(H2PO4)2 D、KNO310. 下列关于物质用途的描述错误的是()A、氧气可用作燃料 B、二氧化碳可用作气体肥料 C、干冰可用于人工降雨 D、铜丝可用作导线11. 下列微粒中,能表示2个氢分子的是( )A、2H B、2H+ C、H2O D、2H212. 下列关于空气的说法正确的是( )A、空气由空气分子构成 B、N2、O2等均匀混合 C、N2、O2不再保持各自的化学性质 D、N2、O2的体积比约为5:113. 下列实验操作正确的是( )A、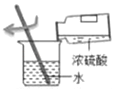 稀释浓硫酸
B、
稀释浓硫酸
B、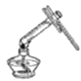 加热液体
C、
加热液体
C、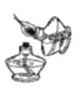 点燃酒精灯
D、
点燃酒精灯
D、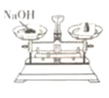 称量NaOH固体
14. 下列做法,不利于节约用水的是( )A、洗菜水直接倒掉 B、收集雨水用于浇花 C、农业灌溉将漫灌改为滴灌 D、及时修理跑漏的水龙头15. 下列图标中,表示“禁止燃放鞭炮”的是( )A、
称量NaOH固体
14. 下列做法,不利于节约用水的是( )A、洗菜水直接倒掉 B、收集雨水用于浇花 C、农业灌溉将漫灌改为滴灌 D、及时修理跑漏的水龙头15. 下列图标中,表示“禁止燃放鞭炮”的是( )A、 B、
B、 C、
C、 D、
D、 16. 下列物质中,用于改良酸性土壤的是( )A、NaHCO3 B、Ca(OH)2 C、NaOH D、NaCl17. 下列化学方程式书写正确的是( )A、3CO+Fe2O3=3CO2+2Fe B、2NaOH + H2SO4=Na2SO4 + H2O C、2H2O22 H2O +O2 D、CaO+H2O=Ca(OH)218. 下列物质必须密封保存的是( )
16. 下列物质中,用于改良酸性土壤的是( )A、NaHCO3 B、Ca(OH)2 C、NaOH D、NaCl17. 下列化学方程式书写正确的是( )A、3CO+Fe2O3=3CO2+2Fe B、2NaOH + H2SO4=Na2SO4 + H2O C、2H2O22 H2O +O2 D、CaO+H2O=Ca(OH)218. 下列物质必须密封保存的是( )
A、木炭 B、浓盐酸 C、石灰石 D、氯化钠19. 净水滤芯中活性炭的主要作用是( )A、过滤 B、吸附 C、消毒 D、絮凝20. 浓硫酸敞口放置一段时间溶质质量分数变小,说明浓硫酸具有( )A、吸水性 B、腐蚀性 C、挥发性 D、酸性21. 氨气是一种无色、有强烈刺激性气味的气体,密度比空气小,极易溶于水。若要收集氨气,下列装置中最好选用( )A、 B、
B、 C、
C、 D、
D、 22. 甲醇俗称“木精”,是重要的化工原料。一种合成甲醇的微观过程如下:
22. 甲醇俗称“木精”,是重要的化工原料。一种合成甲醇的微观过程如下:
下列说法错误的是( )
A、甲是一种清洁能源 B、乙有毒 C、丙中碳、氢元素质量比为1:4 D、反应中甲和乙的质量比为1:723. 下列实验操作不能达到实验目的的是( )选项
实验目的
实验操作
A
除去粗盐中的泥沙
溶解、过滤、蒸发
B
鉴别硬水和软水
加入肥皂水,振荡
C
鉴别O2和CO2
伸入带火星的木条
D
除去NaOH溶液中的Na2CO3
加入稀盐酸
A、A B、B C、C D、D24. 用如图所示装置探究空气中氧气含量。将注射器中10mL热水滴在白磷上,下列说法错误的是(注:白磷的着火点为40oC,集气瓶容积为250mL)( ) A、热水用以点燃白磷 B、白磷燃烧产生大量白烟 C、冷却到50o时打开止水夹 D、最终量筒内液面降至大约60mL处25. 20℃时,向盛有100g水的烧杯中加入40gKCl进行如下实验,依据实验和溶解度曲线分析,下列说法错误的是( )
A、热水用以点燃白磷 B、白磷燃烧产生大量白烟 C、冷却到50o时打开止水夹 D、最终量筒内液面降至大约60mL处25. 20℃时,向盛有100g水的烧杯中加入40gKCl进行如下实验,依据实验和溶解度曲线分析,下列说法错误的是( )
 A、充分搅拌后,甲中固体全部溶解 B、乙溶液中溶质质量分数比甲大 C、甲、乙均为饱和溶液 D、乙中溶液质量为140g
A、充分搅拌后,甲中固体全部溶解 B、乙溶液中溶质质量分数比甲大 C、甲、乙均为饱和溶液 D、乙中溶液质量为140g二、填空
-
26. 从两题中任选一个作答。
Na2CO3的俗称是
Na2CO3的用途之一是
27. 人类的生产生活需要各种材料(1)、下列所用材料属于合成有机高分子材料的是____。A、陶瓷冰墩墩 B、全钢大跳台
B、全钢大跳台 C、碳纤维火炬外壳
C、碳纤维火炬外壳 D、橡胶冰球
D、橡胶冰球 (2)、国家速滑馆的“天幕”用国产高钒封闭索编织而成。钒在元素周期表中的信息如图所示,下列关于钒元素的说法正确的是____。
(2)、国家速滑馆的“天幕”用国产高钒封闭索编织而成。钒在元素周期表中的信息如图所示,下列关于钒元素的说法正确的是____。 A、原子核内有23个质子 B、元素符号为“V” C、相对原子质量为50.94g D、属于金属元素(3)、“手撕钢”的厚度不足0.02mm,用于“折叠屏手机”屏。将钢板轧成“手撕钢”,利用了金属的性。28. 人类的生产生活离不开能源。(1)、目前使用的燃料大多来自化石燃料,包括、石油、天然气。天然气完全燃烧的化学方程式为。(2)、电解水得到的氢气被称为“绿氢”。生产“绿氢”过程中发生反应的化学方程式为。(3)、如图为我国能源结构发展情况对比图,分析数据,得出的结论是。
A、原子核内有23个质子 B、元素符号为“V” C、相对原子质量为50.94g D、属于金属元素(3)、“手撕钢”的厚度不足0.02mm,用于“折叠屏手机”屏。将钢板轧成“手撕钢”,利用了金属的性。28. 人类的生产生活离不开能源。(1)、目前使用的燃料大多来自化石燃料,包括、石油、天然气。天然气完全燃烧的化学方程式为。(2)、电解水得到的氢气被称为“绿氢”。生产“绿氢”过程中发生反应的化学方程式为。(3)、如图为我国能源结构发展情况对比图,分析数据,得出的结论是。
三、科普阅读题
-
29. 阅读下面科普短文。
人类历史上最早使用的制冷剂是C4H10O(乙醚)。19世纪,CO2、NH3(氨气)、SO2和C2H6O(甲醚)相继被用作制冷剂。
20世纪30年代开始,氟利昂普遍被空调等制冷行业用作制冷剂。1970年代中期,臭氧层变薄浮出水面,人们发现氟利昂释放的氯原子导致了大气平流层中臭氧层的严重破坏。氟利昂还是温室气体,其温室效应是CO2的3400倍以上、氟利昂在多个行业都有应用(如图1),我国预在2030年全面禁止使用氟利昂。


NH3和CO2是较早开发,至今仍在使用的制冷剂。
NH3有爆燃的可能,存在一定安全隐患。
CO2是一种天然绿色制冷剂。2022年北京冬奥会采用CO2跨临界直冷制冰技术打造出冬奥历史上“最快的冰”。该技术将制冰过程吸收的热量回收,用于奥运场馆供热、供电(如图2),每年可节约200多万度电。
依据文章内容回答下列问题:
(1)、乙醚由元素组成(2)、19世纪所用的制冷剂中,属于氧化物的是。(3)、使用氟利昂作制冷剂带来的主要问题是。(4)、氟利昂在各行业中应用占比最高的是。(5)、CO2跨临界直冷技术制冰过程中,微观上制冷管道内发生改变的是。(6)、下列说法正确的是____。A、氨气是一种安全的制冷剂 B、氟利昂的温室效应比二氧化碳强 C、制冷剂选择应考虑安全、环保等因素四、综合题
-
30. 以硫铁矿(主要成分FeS2)为原料生产硫酸的工业流程如下图所示(反应条件略):
 (1)、步骤②发生反应的化学方程式为。(2)、上述过程中发生的反应,属于化合反应的是(填序号)。31. 硫铁矿烧渣是用硫铁矿生产硫酸过程中产生的工业废渣。主要成分为氧化铁,还有少量其他物质。用该烧渣制取铁红(氧化铁)的部分过程如下:
(1)、步骤②发生反应的化学方程式为。(2)、上述过程中发生的反应,属于化合反应的是(填序号)。31. 硫铁矿烧渣是用硫铁矿生产硫酸过程中产生的工业废渣。主要成分为氧化铁,还有少量其他物质。用该烧渣制取铁红(氧化铁)的部分过程如下: (1)、烧渣的主要成分在酸浸槽中发生反应的化学方程式为。(2)、沉淀池中用氨水调节pH至5.4,此时溶液显(填“中性”、“酸性”或“碱性”)。(3)、焙烧炉中,铁元素化合价发生的变化为。32. 用下图装置进行实验(夹持仪器略去)。
(1)、烧渣的主要成分在酸浸槽中发生反应的化学方程式为。(2)、沉淀池中用氨水调节pH至5.4,此时溶液显(填“中性”、“酸性”或“碱性”)。(3)、焙烧炉中,铁元素化合价发生的变化为。32. 用下图装置进行实验(夹持仪器略去)。
 (1)、仪器a的名称是。(2)、实验I试管内发生反应的化学方程式为。(3)、实验I干燥管内观察到的现象是。(4)、实验II用以探究燃烧的条件,由此得出的结论是。33. 用两只相同的软塑料瓶探究CO2的性质,装置如图所示。
(1)、仪器a的名称是。(2)、实验I试管内发生反应的化学方程式为。(3)、实验I干燥管内观察到的现象是。(4)、实验II用以探究燃烧的条件,由此得出的结论是。33. 用两只相同的软塑料瓶探究CO2的性质,装置如图所示。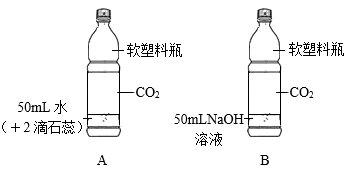 (1)、A瓶观察到的现象是。(2)、B瓶中发生反应的化学方程式为。(3)、证明NaOH能与CO2反应的现象是。34. 用下列两组实验研究Na2CO3和NaHCO3的性质。
(1)、A瓶观察到的现象是。(2)、B瓶中发生反应的化学方程式为。(3)、证明NaOH能与CO2反应的现象是。34. 用下列两组实验研究Na2CO3和NaHCO3的性质。
 (1)、甲组步骤一得出的结论是。(2)、甲组步骤二的目的是。(3)、乙实验可得出“Na2CO3的热稳定性比NaHCO3强”的结论,证据是。35. 在如图所示点滴板的①~⑥孔穴内分别放有①铁片②铜片③铁片④酚酞溶液⑤Na2CO3溶液和⑥Ca(OH)2溶液; 向①中滴加ZnSO4溶液,其他孔穴滴加稀盐酸。
(1)、甲组步骤一得出的结论是。(2)、甲组步骤二的目的是。(3)、乙实验可得出“Na2CO3的热稳定性比NaHCO3强”的结论,证据是。35. 在如图所示点滴板的①~⑥孔穴内分别放有①铁片②铜片③铁片④酚酞溶液⑤Na2CO3溶液和⑥Ca(OH)2溶液; 向①中滴加ZnSO4溶液,其他孔穴滴加稀盐酸。 (1)、孔穴⑤中发生反应的化学方程式为。(2)、六个实验中无明显现象的是(填序号)。(3)、由上述实验得出有关金属的活动性顺序是。36. 课外小组同学用实验测定20oC时食盐的溶解度,请完善实验过程。(1)、配制饱和溶液:取20oC的蒸馏水20g放入小烧杯中,。(2)、测定饱和食盐水及所含溶质的质量:将(1)所得溶液倒入质量为m1的蒸发皿中,。(3)、计算:经测定20oC饱和食盐水中溶质的质量分数为26.5%,则100克水最多溶解食盐的质量为(写计算式)。37. 化学小组的同学在学习了铁生锈的条件后,对暖宝宝的成分(如图1)感到好奇,请参与他们的探究活动。
(1)、孔穴⑤中发生反应的化学方程式为。(2)、六个实验中无明显现象的是(填序号)。(3)、由上述实验得出有关金属的活动性顺序是。36. 课外小组同学用实验测定20oC时食盐的溶解度,请完善实验过程。(1)、配制饱和溶液:取20oC的蒸馏水20g放入小烧杯中,。(2)、测定饱和食盐水及所含溶质的质量:将(1)所得溶液倒入质量为m1的蒸发皿中,。(3)、计算:经测定20oC饱和食盐水中溶质的质量分数为26.5%,则100克水最多溶解食盐的质量为(写计算式)。37. 化学小组的同学在学习了铁生锈的条件后,对暖宝宝的成分(如图1)感到好奇,请参与他们的探究活动。 (1)、【查阅资料】
(1)、【查阅资料】①暖宝宝的发热原理是铁粉腐蚀过程中放出热量;加入活性炭能形成微电池,反应更快。
②铁的腐蚀分为析氢腐蚀和吸氧腐蚀两种:
a.铁在硫酸等酸性条件下发生析氢腐蚀。反应的化学方程式为。
b.铁吸氧腐蚀的总反应为4Fe+3O2+=4Fe(OH)3 , 请补全反应的化学方程式。
(2)、【提出问题】哪些因素会影响铁吸氧腐蚀的速率
【设计实验】
小组同学设计了图2所示的实验装置,进行如下5组实验。

【实验记录】
每组实验加入铁炭总质量为24g,食盐水体积为7.5mL,恰好能将固体润湿。
因素
序号
铁炭质量比
食盐水浓度/%
示数差3cm
所用时间/s
10分钟时
温度升高值/oC
1
2:1
26
90
7.8
2
4:1
26
170
4.2
3
6:1
26
190
3.3
4
2:1
13
140
6
5
2:1
6.5
140
6
【解释与结论】
①通过实验发现,铁炭质量比对铁吸氧腐蚀速率的影响是。
②分析食盐水浓度对铁吸氧腐蚀速率的影响应对比实验(填实验序号)。
③示数差3cm是指U型管左侧液面上升3cm。U型管内液面向左偏移的原因是。
(3)、【反思与评价】①有同学提出应该再加一组实验,研究铁炭质量比为2:1、食盐水浓度为3.3%时的实验数据,你觉得是否有必要,并说明理由。
②依据上述数据,你认为制作发热贴应选择的原料配比,并说明理由。
五、计算题
-
38. 军事上用氢化锂(LiH)作氢气发生来源。请计算40g氢化锂与足量的水反应生成氢气的质量。(温馨提示:反应的化学方程式为LiH + H2O= LiOH + H2↑)。
-