北京市石景山区2022年中考二模化学试题
试卷更新日期:2022-07-22 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、矿石粉碎 B、石蜡熔化 C、酒精挥发 D、食物腐败2. 空气中体积分数的为21%的气体是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. 为了防止骨质疏松,人体必须摄入的元素是( )A、钙 B、铁 C、锌 D、碘4. 下列生活垃圾属于可回收物的是( )A、菜叶 B、废旧电池 C、废旧报纸 D、一次性餐具5. 下列元素属于非金属元素的是( )A、硅 B、汞 C、金 D、钛6. 下列物质在O2中燃烧时,不会产生CO2的是( )A、木炭 B、氢气 C、一氧化碳 D、蜡烛7. 某些食品的近似pH如下,其中酸性最强的是( )
食品
A.柠檬汁
B.番茄汁
C.牛奶
D.玉米粥
pH
2.4
4.4
6.5
7.8
A、A B、B C、C D、D8. 下列净化水的方法中,净化程度最高的是( )A、吸附 B、沉降 C、过滤 D、蒸馏9. 下列物质由氧分子构成的是( )A、H2O B、O2 C、CO2 D、H2O210. 小苏打在加热时反应:2NaHCO3Na2CO3+H2O+CO2↑,该反应属于( )A、化合反应 B、分解反应 C、复分解反应 D、置换反应11. 下列物质的用途中,利用其化学性质的是( )A、铜用作导线 B、浓硫酸用作干燥剂 C、干冰用作制冷剂 D、小苏打用于治疗胃酸过多症12. “84消毒液”可用于环境等的消毒,主要成分为NaClO,其中氯元素的化合价为( )A、+3 B、+2 C、+1 D、-113. 下列实验操作中,错误的是( )A、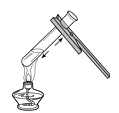 加热液体
B、
加热液体
B、 稀释浓硫酸
C、
稀释浓硫酸
C、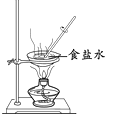 蒸发食盐水
D、
蒸发食盐水
D、 检查装置气密性
14. 下列物质敞口放置于空气中,质量会减小的是( )A、浓盐酸 B、浓硫酸 C、石灰石 D、氢氧化钠15. 如图是元素周期表中钠元素的信息示意图,对图中信息理解错误的是( )
检查装置气密性
14. 下列物质敞口放置于空气中,质量会减小的是( )A、浓盐酸 B、浓硫酸 C、石灰石 D、氢氧化钠15. 如图是元素周期表中钠元素的信息示意图,对图中信息理解错误的是( ) A、质子数为 11 B、元素名称为钠 C、元素符号为 Na D、核外电子数为 22.9916. 将下列金属放入稀盐酸中,不能发生反应的是( )A、铜 B、锌 C、铁 D、镁17. 下列物质的化学式书写正确的是( )A、氧化镁MgO2 B、氧化铝Al2O3 C、氯化锌ZnCl D、硫酸钠NaSO418. 用下图装置测定空气中氧气的含量。下列说法正确的是( )
A、质子数为 11 B、元素名称为钠 C、元素符号为 Na D、核外电子数为 22.9916. 将下列金属放入稀盐酸中,不能发生反应的是( )A、铜 B、锌 C、铁 D、镁17. 下列物质的化学式书写正确的是( )A、氧化镁MgO2 B、氧化铝Al2O3 C、氯化锌ZnCl D、硫酸钠NaSO418. 用下图装置测定空气中氧气的含量。下列说法正确的是( ) A、红磷取用量的多少不影响实验结果 B、将红磷点燃放入瓶内后,再用弹簧夹夹紧乳胶管 C、红磷熄灭后,应立即打开弹簧夹 D、反应后,瓶中剩余的气体主要是氮气19. 关于化学反应“ ”的下列叙述中,错误的是( )A、甲烷具有可燃性 B、反应前后原子个数不变 C、16g甲烷和64g氧气充分反应生成18g水和44g二氧化碳 D、1个甲烷分子与2个氧分子生成2个水分子和1个二氧化碳分子20. 用下图装置探究可燃物燃烧的条件,图1铜片上白磷和图2水中白磷发生燃烧。下列结论错误的是( )
A、红磷取用量的多少不影响实验结果 B、将红磷点燃放入瓶内后,再用弹簧夹夹紧乳胶管 C、红磷熄灭后,应立即打开弹簧夹 D、反应后,瓶中剩余的气体主要是氮气19. 关于化学反应“ ”的下列叙述中,错误的是( )A、甲烷具有可燃性 B、反应前后原子个数不变 C、16g甲烷和64g氧气充分反应生成18g水和44g二氧化碳 D、1个甲烷分子与2个氧分子生成2个水分子和1个二氧化碳分子20. 用下图装置探究可燃物燃烧的条件,图1铜片上白磷和图2水中白磷发生燃烧。下列结论错误的是( ) A、烧杯中热水的作用之一是使白磷达到燃烧所需的温度 B、对比铜片上的白磷、红磷发生的现象,说明可燃物燃烧温度要达到着火点 C、对比铜片上红磷、水中白磷发生的现象,说明可燃物燃烧要与氧气接触 D、对比水中白磷通氧气前后发生的现象,说明可燃物燃烧要与氧气接触
A、烧杯中热水的作用之一是使白磷达到燃烧所需的温度 B、对比铜片上的白磷、红磷发生的现象,说明可燃物燃烧温度要达到着火点 C、对比铜片上红磷、水中白磷发生的现象,说明可燃物燃烧要与氧气接触 D、对比水中白磷通氧气前后发生的现象,说明可燃物燃烧要与氧气接触二、选择题组
-
21. 用水、氯化钠、二氧化碳、蔗糖等物质可以自制“盐汽水”。完成下面小题。(1)、自制的“盐汽水”属于( )A、纯净物 B、化合物 C、混合物 D、盐(2)、自制“盐汽水”的原料中属于有机化合物的是( )A、水 B、氯化钠 C、二氧化碳 D、蔗糖22. 依据溶解度曲线和实验①~④完成下面小题。


实验
①
②
③
④
水的温度/℃
20
20
40
40
硝酸钾质量/g
20
40
25
50
水的质量/g
100
100
100
100
(1)、所得溶液中,溶质与溶剂的质量比为1:2的是( )A、① B、② C、③ D、④(2)、所得溶液属于饱和溶液的是( )A、① B、② C、③ D、④(3)、所得溶液的溶质质量分数为20%的是( )A、① B、② C、③ D、④三、填空题
-
23. 从A或B两题中任选一个作答,若两题均作答,按A计分。
A NaOH的俗称之一是
B Ca(OH)2的俗称之一是
24. 醋是日常生活中常用的调味品,主要通过大米或高粱等谷物经过发酵制成。 (1)、谷物中富含的营养素是____(填序号)。A、糖类 B、油脂 C、蛋白质(2)、醋酸(CH3COOH)中质量分数最大的元素是。(3)、葡萄糖和酒精两种物质的共同点是。25. CO2是人类实现可持续发展必须善加利用的资源。下图是通过清洁能源电解水制取氢气,再将CO2转化为燃料或其他化学品的示意。
(1)、谷物中富含的营养素是____(填序号)。A、糖类 B、油脂 C、蛋白质(2)、醋酸(CH3COOH)中质量分数最大的元素是。(3)、葡萄糖和酒精两种物质的共同点是。25. CO2是人类实现可持续发展必须善加利用的资源。下图是通过清洁能源电解水制取氢气,再将CO2转化为燃料或其他化学品的示意。 (1)、下列发电方式利用清洁能源的是____(填序号)。A、风力发电 B、太阳能光伏发电 C、燃煤发电(2)、电解水制取氢气反应的化学方程式为。(3)、CO2加氢制甲醇微观示意图如下,参与反应的A与B的分子个数比为。
(1)、下列发电方式利用清洁能源的是____(填序号)。A、风力发电 B、太阳能光伏发电 C、燃煤发电(2)、电解水制取氢气反应的化学方程式为。(3)、CO2加氢制甲醇微观示意图如下,参与反应的A与B的分子个数比为。 26. 工业上炼铁的主要原料是铁矿石、焦炭、石灰石、空气,生产过程示意如图。
26. 工业上炼铁的主要原料是铁矿石、焦炭、石灰石、空气,生产过程示意如图。 (1)、石灰石的主要作用是将铁矿石中的杂质转化为炉渣。石灰石的主要成分是。(2)、生成还原性气体CO的原料有。(3)、CO与赤铁矿中Fe2O3反应的化学方程式为。27. 二氧化钛溶胶常用于无机胶黏剂、陶瓷等,其主要工艺流程如下图。
(1)、石灰石的主要作用是将铁矿石中的杂质转化为炉渣。石灰石的主要成分是。(2)、生成还原性气体CO的原料有。(3)、CO与赤铁矿中Fe2O3反应的化学方程式为。27. 二氧化钛溶胶常用于无机胶黏剂、陶瓷等,其主要工艺流程如下图。
已知:反应釜中发生的反应为:。
(1)、反应釜中,反应前后的物质属于氧化物的有。(2)、过滤器中,除去的物质是。(3)、分散釜中,加入x的目的是调节pH为1~2,得到二氧化钛溶胶。x为(填“盐酸”或“NaOH溶液”)。28. 用下图所示仪器配制50g溶质质量分数为6%的NaCl溶液。 (1)、实验中需要称量NaCl固体的质量为g。(2)、量取水的体积时,用到的仪器有胶头滴管和。(3)、实验中的下列操作,需要用到玻璃棒的是____(填序号)。A、称量 B、溶解 C、装瓶贴标签29. 在两个小烧杯中进行氢氧化钠性质的实验。
(1)、实验中需要称量NaCl固体的质量为g。(2)、量取水的体积时,用到的仪器有胶头滴管和。(3)、实验中的下列操作,需要用到玻璃棒的是____(填序号)。A、称量 B、溶解 C、装瓶贴标签29. 在两个小烧杯中进行氢氧化钠性质的实验。 (1)、实验1中,氢氧化钠发生潮解,说明氢氧化钠具有的性质是;久置后氢氧化钠发生变质,用化学方程式表示其原因:。(2)、实验2中,证明氢氧化钠能与盐酸发生反应的现象是。
(1)、实验1中,氢氧化钠发生潮解,说明氢氧化钠具有的性质是;久置后氢氧化钠发生变质,用化学方程式表示其原因:。(2)、实验2中,证明氢氧化钠能与盐酸发生反应的现象是。四、科普阅读题
-
30. 阅读下面科普短文。
贝壳主要由95%左右的CaCO3与5%左右的贝壳素构成,是一种天然的生物资源,拥有非常高的利用价值。
贝壳经过高温煅烧等加工处理后,可用来制作建筑材料、动物和人体所需的钙补充剂。
贝壳具有多级层状结构,拥有良好的吸附性,可用作污水、土壤中重金属的吸附剂。研究人员用贝壳粉和CaCO3粉末分别对某土壤样品(被铅蓄电池污染)中Pb吸附效果进行实验,结果如图。
贝壳经加工可用于涂料,贝壳涂料具有隔热保温功能。研究人员对贝壳涂料的隔热保温功能进行了实验:制作4个相同的纸箱模拟封闭建筑。甲作为对照不涂刷涂料,乙在内壁涂刷涂料,丙在外壁涂刷涂料,丁在内壁和外壁涂刷涂料。干燥后,将68℃500mL的水同时放入四个纸箱中,自然冷却45min,测量水温,结果如下表。
甲
乙
丙
丁
温度/℃
50.7
52
52.5
52.5

贝壳具有广泛应用前景,若能有效利用,必会产生巨大经济和环保生态效益。
(原文作者崔童、赵镇东等,有删改)
依据文章内容回答下列问题。
(1)、贝壳中CaCO3所占比例约为。(2)、在保温领域,贝壳涂料涂刷在(填“内壁”或“外壁”)效果更好。(3)、判断下列说法是否正确(填“对”或“错”)。①贝壳可以用作吸附剂,是因为它具有多级层状结构。。
②贝壳是制作动物和人体所需的钙补充剂的一种原料。。
(4)、根据图实验,得出的结论是。五、综合题
-
31. 根据下图回答问题。
 (1)、实验室用高锰酸钾制取氧气的化学方程式为。(2)、实验室制取二氧化碳时,选用的发生及收集装置分别是;检验二氧化碳已经收集满的方法是。32. 如下图进行实验,点燃酒精灯至木炭红热,将过氧化氢溶液加入平底烧瓶中。
(1)、实验室用高锰酸钾制取氧气的化学方程式为。(2)、实验室制取二氧化碳时,选用的发生及收集装置分别是;检验二氧化碳已经收集满的方法是。32. 如下图进行实验,点燃酒精灯至木炭红热,将过氧化氢溶液加入平底烧瓶中。 (1)、A中发生反应的化学方程式为。(2)、B和C中观察到的现象是。33. 用下图实验(夹持仪器已略去)研究铁的性质。
(1)、A中发生反应的化学方程式为。(2)、B和C中观察到的现象是。33. 用下图实验(夹持仪器已略去)研究铁的性质。 (1)、实验1,点燃酒精灯,一段时间后蜡片熔化,说明铁具有的性质是。(2)、实验2,铁丝在氧气中燃烧反应的化学方程式为。(3)、实验3,观察到的现象是。34. 取3支试管,各放入一个生锈的铁钉,再分别加入5mL不同浓度的硫酸溶液,进行实验,记录如下表。
(1)、实验1,点燃酒精灯,一段时间后蜡片熔化,说明铁具有的性质是。(2)、实验2,铁丝在氧气中燃烧反应的化学方程式为。(3)、实验3,观察到的现象是。34. 取3支试管,各放入一个生锈的铁钉,再分别加入5mL不同浓度的硫酸溶液,进行实验,记录如下表。硫酸溶液
实验条件
实验现象
10%
不加热
30s铁锈脱落,50s出现较明显小气泡,90s溶液发红
10%
酒精灯上加热
10s出现明显气泡,20s铁锈脱落,65s铁锈消失,溶液变黄
20%
酒精灯上加热
5s出现明显气泡,10s铁锈脱落,45s铁锈消失,溶液变黄
(1)、溶液变黄是因为生成了。(2)、用化学方程式表示溶液中出现气泡的原因:。(3)、该实验可以得出的结论是。35. 实验小组的同学探究不同的配制方法对紫色石蕊溶液显色的影响。【查阅资料】石蕊能溶于水或乙醇中。
【进行实验1】分别用某品牌的石蕊1g进行4种方法的石蕊溶液配制。
方法
蒸馏水体积/mL
操作
石蕊溶液
溶液颜色
①
100
搅拌,静置1h,过滤
滤液
紫色
②
100
煮沸后过滤
滤液
紫色
③
100
搅拌,静置24h,过滤
滤液
紫色
④
50
搅拌,静置24h,过滤
滤液加30mL乙醇,再加蒸馏水稀释至100mL
紫色
【解释与结论】
(1)、方法①配制的石蕊溶液中,溶质是。(2)、方法④中,加蒸馏水稀释至100mL时,加入的蒸馏水体积大于20mL。说明分子具有的性质是。(3)、【进行实验2】用4种方法配制的石蕊溶液进行显色实验:向被测溶液中滴加石蕊溶液。被试溶液
方法①
方法②
方法③
方法④
10%盐酸
红
红
红
浅红
饱和二氧化碳溶液
浅红
浅红
浅红
不明显
饱和碳酸钠溶液
蓝
蓝
蓝
浅蓝
澄清石灰水
蓝
蓝
蓝
浅蓝
【解释与结论】
通过实验可得出饱和碳酸钠溶液呈(填“酸性”或“碱性”)。
(4)、向饱和二氧化碳溶液中滴加石蕊溶液呈浅红色,用化学方程式解释其原因:。(5)、进行实验2时,需要控制的相同条件是:取用被测溶液的体积相同、。(6)、【反思与评价】经实验证明,配制方法④的滤渣中还有较多未溶解的石蕊。实验方案是:向滤渣中加入50mL蒸馏水,。
(7)、用方法④配制的石蕊溶液进行显色实验时现象不明显,原因可能是。六、计算题
-
36. 硫酸厂的污水中含有硫酸等物质,可以用氢氧化钙(假设其他物质不与氢氧化钙反应)进行中和处理。请计算:74kg氢氧化钙可以处理硫酸的质量。
-