山东省济宁市邹城市2022年中考二模化学试题
试卷更新日期:2022-07-12 类型:中考模拟
一、单选题
-
1. 化学与生活密切相关,下列有关物质性质与用途的说法错误的是( )A、铵态氮肥与草木灰都是肥料,可混合使用 B、金具有很好的延展性,可压成很薄的片 C、钨的熔点很高,可用于制造灯泡的小丝 D、熟石灰能与酸反应, 可用于改良酸性土壤2. 下列有关实验基本操作,正确的是( )A、
 B、
B、 C、
C、 D、
D、 3. 建立宏观与微观的联系是化学常用的思维方式,下列是对宏观事实的微观解释,错误的是( )A、硫在氧气中燃烧比空气中更剧烈——在氧气中硫接触到氧分子的机会大 B、夏季在校园里闻到阵阵花香——分子在不断地运动 C、电解水生成氢气和氧气——水中含有氢分子和氧分子 D、液氧和氧气都能助燃——同种分子化学性质相同4. 下列指定反应的化学方程式证确的是( )A、硫酸型酸雨的形成:SO2+H2O=H2SO4 B、铁粉溶于稀硫酸:2Fe+3H2SO4=Fe2(SO4)3+H2↑ C、镁粉着火不能用CO2灭火的原因:2Mg+CO22MgO+C D、Na2O2与CO2反应生成纯碱和氧气:Na2O+CO2=Na2CO3+O25. 推理见学习化学的重爱思能方法,下列推理合理的是( )A、中和反应能够生成盐和水,所以能够生成盐和水的反应,一定是中和反应 B、碱性溶液能使酚酞试液变红色,所以能使酚酞试液变红色的溶液显碱性 C、氧化物一定含有氧元素,则含有氧元素的化合物一定是氧化物 D、洗涤剂除油污是利用了乳化的原理,所以汽油除油污也是利用乳化的原理6. 下列实验现象的描述中,正确的是( )A、木炭在氧气中燃烧,生成二氧化碳 B、硫在氧气中燃烧,发出淡蓝色火焰 C、红磷在空气中燃烧产生大量的白雾 D、铁丝在氧气中燃烧,火星四射,生成黑色固体7. 下列依据实验目的所设计的实验操作中,正确的是( )
3. 建立宏观与微观的联系是化学常用的思维方式,下列是对宏观事实的微观解释,错误的是( )A、硫在氧气中燃烧比空气中更剧烈——在氧气中硫接触到氧分子的机会大 B、夏季在校园里闻到阵阵花香——分子在不断地运动 C、电解水生成氢气和氧气——水中含有氢分子和氧分子 D、液氧和氧气都能助燃——同种分子化学性质相同4. 下列指定反应的化学方程式证确的是( )A、硫酸型酸雨的形成:SO2+H2O=H2SO4 B、铁粉溶于稀硫酸:2Fe+3H2SO4=Fe2(SO4)3+H2↑ C、镁粉着火不能用CO2灭火的原因:2Mg+CO22MgO+C D、Na2O2与CO2反应生成纯碱和氧气:Na2O+CO2=Na2CO3+O25. 推理见学习化学的重爱思能方法,下列推理合理的是( )A、中和反应能够生成盐和水,所以能够生成盐和水的反应,一定是中和反应 B、碱性溶液能使酚酞试液变红色,所以能使酚酞试液变红色的溶液显碱性 C、氧化物一定含有氧元素,则含有氧元素的化合物一定是氧化物 D、洗涤剂除油污是利用了乳化的原理,所以汽油除油污也是利用乳化的原理6. 下列实验现象的描述中,正确的是( )A、木炭在氧气中燃烧,生成二氧化碳 B、硫在氧气中燃烧,发出淡蓝色火焰 C、红磷在空气中燃烧产生大量的白雾 D、铁丝在氧气中燃烧,火星四射,生成黑色固体7. 下列依据实验目的所设计的实验操作中,正确的是( )选项
实验目的
实验操作
A
检验NaCl中含有Na2CO3
加水溶解
B
鉴别NaOH和Ca(OH)2溶液
加Na2CO3溶液
C
除去FeSO4溶液中的CuSO4
加适量Zn粉,过滤
D
除去CO2中的CO
通过足量NaOH溶液
A、A B、B C、C D、D8. 现有a、b、c三种物质的溶解度曲线如图所示,下列说法正确的是( ) A、a、b、c三种物质的溶解度由大到小的顺序是a>b>c B、t2℃时,30g a物质加入到50g水中不断搅拌,所得溶液的质量为80g C、t1℃时,将c的饱和溶液升温到t2℃,饱和溶液的质量会减少 D、t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,析出晶体最多的是a物质9. 下列图像能正确反映对应变化关系的是( )A、
A、a、b、c三种物质的溶解度由大到小的顺序是a>b>c B、t2℃时,30g a物质加入到50g水中不断搅拌,所得溶液的质量为80g C、t1℃时,将c的饱和溶液升温到t2℃,饱和溶液的质量会减少 D、t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,析出晶体最多的是a物质9. 下列图像能正确反映对应变化关系的是( )A、 等质量的镁和锌中分别加入等浓度的稀H2SO4至过量
B、
等质量的镁和锌中分别加入等浓度的稀H2SO4至过量
B、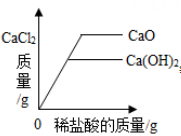 等质量的CaO和Ca(OH)2中分别加入等浓度的稀盐酸至过量
C、
等质量的CaO和Ca(OH)2中分别加入等浓度的稀盐酸至过量
C、 CaCl2和HCl的混合溶液中加入Na2CO3溶液至过量
D、
CaCl2和HCl的混合溶液中加入Na2CO3溶液至过量
D、 AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量
10. 有甲、乙、丙、丁四种无色溶液,它们分别是Na2CO3、BaCl2、HCl、H2SO4溶液中的一种。为区别这四种溶液,现将它们两两混合并得到下面现象:
AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量
10. 有甲、乙、丙、丁四种无色溶液,它们分别是Na2CO3、BaCl2、HCl、H2SO4溶液中的一种。为区别这四种溶液,现将它们两两混合并得到下面现象:溶液
甲+乙
乙+丙
丙+丁
甲+丁
现象
无明显现象
白色沉淀
白色沉淀
无色气体
根据对上述现象的分析,可推知甲、乙、丙、于四种溶液的顺序依次是( )
A、HCl、BaCl2、Na2CO3、H2SO4 B、Na2CO3、BaCl2、H2SO4、HCl C、H2SO4、HCl、Na2CO3、BaCl2 D、HCl、H2SO4、BaCl2、Na2CO3二、填空题
-
11. 糖尿病检验原理之一是将含有葡萄糖(C6H12O6)的尿液与新制Cu(OH)2共热,产生砖红色沉淀,该沉淀为氧化亚铜,请用化学用语填空。(1)、2个铜原子 , 3个氢氧根离子。(2)、铜元素常显0、+1、+2价,氧化亚铜的化学式为。(3)、葡萄糖在人体内缓慢氧化生成CO2和 , 并释放能量。12. 锂被誉为“21世纪的能源金属”,是世界上最轻的金属。“无锂不走天下”,锂电池改变了我们的生活。
 (1)、下列说法正确的是____(填序号)。A、锂离子的相对原子质量是6.941g B、锂原子核外电子数为3 C、锂离子电池放电时,电能转化成化学能(2)、在化学反应中容易(填 “得到”或“失去”电子)。(3)、锂是一种比铁活泼的金属。锂与稀硫酸反应的化学方程式为。13. 在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:(1)、滤渣中一定含有 , 可能含有(填化学式)。(2)、滤液中可能含有的溶质(填化学式)。(3)、用化学方程式表示溶液变为浅绿色的原因。14. 生活中处处蕴含着化学知识。请用所学知识回答下列问题。(1)、日常生活中常用的方法降低水的硬度。(2)、端午节临近,我们包粽子准备了如下食材:糯米、瘦肉、花生、红枣,其中瘦肉富含的营养素主要是。(3)、食品安全是一个永恒的话题。下列说法不科学的是(填序号)。
(1)、下列说法正确的是____(填序号)。A、锂离子的相对原子质量是6.941g B、锂原子核外电子数为3 C、锂离子电池放电时,电能转化成化学能(2)、在化学反应中容易(填 “得到”或“失去”电子)。(3)、锂是一种比铁活泼的金属。锂与稀硫酸反应的化学方程式为。13. 在某次实验课上,小东同学把一包铁粉和镁粉的混合物放入一定量的AgNO3溶液中,使其充分反应后过滤,得到滤渣和浅绿色滤液,据此回答下列问题:(1)、滤渣中一定含有 , 可能含有(填化学式)。(2)、滤液中可能含有的溶质(填化学式)。(3)、用化学方程式表示溶液变为浅绿色的原因。14. 生活中处处蕴含着化学知识。请用所学知识回答下列问题。(1)、日常生活中常用的方法降低水的硬度。(2)、端午节临近,我们包粽子准备了如下食材:糯米、瘦肉、花生、红枣,其中瘦肉富含的营养素主要是。(3)、食品安全是一个永恒的话题。下列说法不科学的是(填序号)。A 霉变的花生、大米蒸煮后仍不可食用
B 不可用亚硝酸钠代替食盐腌制食物
C 使用了食品添加剂的食品对人体都有害
15. 乙醇:俗名酒精,乙醇的分子结构模型如图所示,请回答: (1)、乙醇分子中C、H、O原子个数比为;(2)、乙醇中C、O两元素的质量比为。
(1)、乙醇分子中C、H、O原子个数比为;(2)、乙醇中C、O两元素的质量比为。三、综合题
-
16. 海洋中有丰富的水生物和化学资源。海水晒盐能得到粗盐和苦卤,粗盐中含有多种可溶性杂质(硫酸钠、氯化钙等)和不溶性杂质(泥沙等)。现以粗盐为原料制取精盐,生产过程如图所示,请回答下列问题:
 (1)、操作I和操作Ⅱ的名称是;(2)、加入BaCl2溶液后发生反应的化学方程式为;(3)、向操作Ⅱ后所得溶液中加入过量盐酸,其目的是 , 最后通过蒸发结晶得到较为纯净的氯化钠。17.(1)、 实验室采用下列三种方法制取气体:
(1)、操作I和操作Ⅱ的名称是;(2)、加入BaCl2溶液后发生反应的化学方程式为;(3)、向操作Ⅱ后所得溶液中加入过量盐酸,其目的是 , 最后通过蒸发结晶得到较为纯净的氯化钠。17.(1)、 实验室采用下列三种方法制取气体:制取O2:
制取CO2:……
制取Cl2: MnO2+4HCl (浓) MnCl2+Cl2↑+2H2O
已知: Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
①写出实验室制取CO2的化学方程式。
②下列有A、B、C三种发生装置和D、E两种收集装置,请回答下列问题:

Ⅰ、写出图中仪器II的名称是;
II、用D装置收集Cl2时,Cl2应从管口(填导气管接口处的字母)进入瓶中。
③下列对制取三种气体的分析中错误的是。
A.制取CO2和Cl2的发生装置相同 B.O2、CO2和Cl2都能用向上排空气法收集
C.制取Cl2的反应中MnO2是催化剂 D.用E装置收集O2时,O2应从d管导入
④该小组在制取CO2的时候,发现二氧化碳收集好后,反应仍在发生,所以,他们想设计一个能随时控制反应的发生与停止的装置。你觉得如图I、II、Ⅲ装置中能实现上述意图的是。
 (2)、皮蛋,又称松花蛋,是一种中国特有的食品。某化学小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤液中溶质的成分进行探究。
(2)、皮蛋,又称松花蛋,是一种中国特有的食品。某化学小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤液中溶质的成分进行探究。小组同学讨论后一致认为, 滤液中的溶质定含有 NaOH和。(写化学式)
[提出问题] 滤液中还可能含有哪些溶质呢?
[作出猜想]
小林认为:还含有Na2CO3; 小方认为: 还含有; 小华认为:还含有Ca(OH)2和Na2CO3
[交流讨论1]经过进步讨论,大家认为小华的猜想不合理,原因是。(用化学方程式表示)
[实验探究]
实验操作
实验现象
实验结论
小林:取少量滤液于试管中,滴加足量的稀盐酸
小林的猜想正确
小华:取少量滤液于试管中,滴加几滴酚酞溶液
溶液变红
小林的猜想正确
[交流讨论2]同学们认为,通过小华的实验不足以得出其结论,原因是。
[继续探究]小明也取少量滤液于试管中,滴加少量稀盐酸,却没有看到明显现象。小明对此深感疑心。经老师的指导和大家的认真思考后终于找出了原因,你认为原因是。最后,老师对同学们这种严谨的科学态度给子了充分的肯定。
18. 碳酸氢钠片是一种常用药,能用于治疗胃酸过多,这是因为人体的胃液中含有盐酸,为测定某药片中碳酸氢钠的含量,小金进行了如下实验: (1)、小金按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质量的变化来采集实验数据。同学们认为,测得碳酸氢钠的质量分数会偏大,原因是。(答出一点即可)(2)、为减小实验误差,小金又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实验,采集的实验数据如表:
(1)、小金按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质量的变化来采集实验数据。同学们认为,测得碳酸氢钠的质量分数会偏大,原因是。(答出一点即可)(2)、为减小实验误差,小金又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实验,采集的实验数据如表:实验序号
1
2
3
碳酸氢钠片样品质量/g
3.0
3.0
3.0
反应前总质量/g
193.8
194.6
193.6
反应后总质量/g
192.6
193.6
192.5
①三次实验中生成二氧化碳的平均质量为g;
②请计算药片中碳酸氢钠的质量分数。(写出计算过程)