内蒙古包头市青山区2022年中考一模化学试题
试卷更新日期:2022-07-12 类型:中考模拟
一、单选题
-
1. “绿水青山就是金山银山”,保护环境就是保护我们自己。下列做法值得提倡的是( )A、禁止使用燃煤发电,减少酸雨的形成 B、大量施用化肥、农药,提高农作物产量 C、实验室含酸废水直接倒入下水道 D、减少一次性餐具的使用2. 下表中知识的归纳,完全正确的一组是( )
A.变化
B.组成
①有沉淀出现的变化不一定是化学变化
②酸和碱的反应一定是中和反应
①同种元素组成的物质一定不是化合物
②氯酸钾中含有氧元素,所以它属于氧化物
C.结构
D.性质
①构成物质的微粒有分子、原子、离子
②原子都是由质子、中子、电子构成的
①氧气和一氧化碳都具有还原性
②活性炭净水利用了它的化学性质——吸附性
A、A B、B C、C D、D3. 随着科学的发展,新能源的开发不断取得突破。清华大学研究人员成功研制出一种纳米 纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下图所示(图中微粒恰 好完全反应)。下列说法正确的是( ) A、乙物质中碳元素的化合价为+2 B、反应中甲和丁的质量比为 1:3 C、该反应类型为置换反应 D、反应前后分子的数目不变4. 根据所学的化学知识,判断以下实验方法正确的是( )
A、乙物质中碳元素的化合价为+2 B、反应中甲和丁的质量比为 1:3 C、该反应类型为置换反应 D、反应前后分子的数目不变4. 根据所学的化学知识,判断以下实验方法正确的是( )选项
实验目的
实验操作
A
检验某未知溶液是否含有
加入氯化钡溶液,观察是否有白色沉淀产生
B
除去部分变质的NaOH中的杂质
加水溶解,滴加适量的CaCl2溶液
C
鉴别NH4Cl和尿素【CO(NH2)2)】
分别取少量固体于研钵中,加熟石灰研磨,闻气味
D
分离CaCl2和NaCl的混合溶液
加入适量的碳酸钠溶液,过滤,向滤渣中加适量稀硫酸
A、A B、B C、C D、D5. 黄铜是由铜和锌组成的合金,利用黄铜制造其它物质的过程中,会产生大量的黄铜渣,主要含有Zn、Cu、ZnO、CuO。现有一种利用黄铜渣获取Cu与ZnSO4 , 的实验流程如图,则下列说法正确的是( ) A、酸溶的目的只是为了将Cu析出 B、向滤渣中加入稀盐酸,有气泡产生 C、滤液a中只有ZnSO4、CuSO4两种溶质 D、把图中“过量Zn”换成“过量Fe”,也能达到实验目的6. 在完成实验室制取二氧化碳的实验后,为检测废液中溶质成分,同学们向废液中分别加入四种不同物质并绘制图象,下列图象中不能与其它三个图象得到同一结论的是( )A、
A、酸溶的目的只是为了将Cu析出 B、向滤渣中加入稀盐酸,有气泡产生 C、滤液a中只有ZnSO4、CuSO4两种溶质 D、把图中“过量Zn”换成“过量Fe”,也能达到实验目的6. 在完成实验室制取二氧化碳的实验后,为检测废液中溶质成分,同学们向废液中分别加入四种不同物质并绘制图象,下列图象中不能与其它三个图象得到同一结论的是( )A、 B、
B、 C、
C、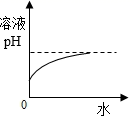 D、
D、
二、填空题
-
7. 回答:(1)、2021 年 12 月国内首条磁浮空轨车辆“兴国号”在武汉下线。
①“兴国号”攻克了长大薄壁铝合金车体激光焊接技术,焊接时用氩气作保护气,氩气的 化学式为。
②下列制造列车使用的材料中,属于合成材料的是。
A.有机玻璃车窗 B.铝合金车体 C.铜导线 D.涤纶座套
③该车辆生产中使用了钕铁硼磁体材料。已知钕(Nd)是一种稀土元素, 钕元素部分信息如图所示,则钕原子的中子数为(取整数)。已知氯化钕的化学式为 NdCl3 , 则氧化钕的化学式为。
 (2)、如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
(2)、如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
①t1℃时,完全溶解 5g 丙物质至少需要水g。
②t2℃时,将 20g 甲加入100g 水中,充分搅拌后所得甲溶液可以 用如图中点(填“a”、“b”、“c”)表示。
③将等质量的甲、丙的饱和溶液从 t2℃降温到 t1℃,对所得溶液的 叙述正确的是。
A.都是饱和溶液 B.溶剂质量:甲<丙
C.溶液质量:甲>丙 D.溶质质量分数:甲=丙
三、综合题
-
8. 如图是实验室制取气体的常用仪器。请根据要求填空:
 (1)、小峰同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择图中的仪器(填序号),其化学方程式为。(2)、小明同学设计了如图所示的实验装置,既可用于制取 CO2 , 又可用于探究 CO2的性质。
(1)、小峰同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择图中的仪器(填序号),其化学方程式为。(2)、小明同学设计了如图所示的实验装置,既可用于制取 CO2 , 又可用于探究 CO2的性质。(说明:1、装置Ⅰ中盛放的药品是石灰石和稀盐酸。2、装置Ⅲ 中在小试管外壁贴有 4 片试纸:其中两端的两片用紫色石蕊溶液润湿, 中间两片用紫色石蕊溶液浸过并晒干)

①实验时,打开 K1关闭 K2可用来制备 CO2。检验Ⅱ中气体 收集满的方法是。
②实验时,关闭 K1打开 K2可用于探究 CO2的性质。实验时Ⅲ中出现的现象是 , 该实验说明 CO2具有的性质是。
9. 已知 A、B、C、D、E 为初中化学中常见的五种不同类别的物质,其中 A 为年产量最高 的金属单质,E 可用于制造玻璃、纺织、造纸等,各种物 质间的反应和转化关系如图所示(“—”表示相连的两种物质之间可发生反应,“→”表示一种物质可以转化为另一种 物质;反应条件、部分反应物和生成物已略去),请写出: (1)、C 可能是(填一种,写化学式)(2)、D 与 E 反应的化学方程式。(3)、B→A 的反应(一定、不一定、一定不)是置换反应。10. 同学们在探究稀硫酸的化学性质时,进行了下列实验。请结合图和资料回答问题。
(1)、C 可能是(填一种,写化学式)(2)、D 与 E 反应的化学方程式。(3)、B→A 的反应(一定、不一定、一定不)是置换反应。10. 同学们在探究稀硫酸的化学性质时,进行了下列实验。请结合图和资料回答问题。
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到 底部有沉淀,上层清液呈红色。为了检验废液中的成分进行了下列探究。
(1)、经过分析讨论,废液缸中的沉淀是(2)、为了探究上层清液中溶质的成分(指示剂除外),设计如下实验方案。请你补充完整。【做出猜想】猜想 1:溶质有 NaCl、HCl
猜想 2:溶质有 NaCl、HCl、H2SO4、Na2SO4
猜想 3:溶质有 NaCl、Na2CO3、Na2SO4
猜想 4:溶质有
【讨论分析】经讨论,大家认为猜想 3 是错误的,理由是
【实验验证】
实验步骤
实验现象
探究结论
猜想4正确
四、计算题
-
11. 某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数, 称取该产品样品 25g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应, 气体完全逸出,得到不饱和 NaCl 溶液。反应过程用精密仪器测 得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。请 回答:
 (1)、该纯碱样品中 Na2CO3的质量分数。(2)、反应后所得溶液中溶质的质量分数。
(1)、该纯碱样品中 Na2CO3的质量分数。(2)、反应后所得溶液中溶质的质量分数。
-