湖南省株洲市醴陵市2022年初中学业水平诊断性测试化学试题
试卷更新日期:2022-07-12 类型:中考模拟
一、单选题
-
1. 下列过程涉及化学变化的是( )A、钢铁冶炼 B、酒精挥发 C、蔗糖溶解 D、玻璃碎裂2. 运用分类法学习和研究物质,能够收到事半功倍的效果。下列物质中属于纯净物的是( )A、木炭 B、空气 C、硬水 D、氧气3. 下列有关水的叙述正确的是( )A、淡水资源是取之不尽的 B、净化水的方法有:沉淀、过滤、吸附、蒸馏 C、肥皂水可以降低水的硬度 D、水分子是由氢元素和氧元素组成的4. 化学让我们欣赏到了溶液的颜色美,下列物质溶于水后形成无色溶液的是( )A、CuSO4 B、KMnO4 C、MgCl2 D、FeSO45. 医疗上高锰酸钾(KMnO4)是防腐消毒药,用于急性皮炎或急性湿疹。KMnO4中锰元素的化合价为( )A、+6 B、+7 C、+4 D、+26. 规范的实验操作是实验成功的关键。下列实验操作正确的是( )A、
 倾倒液体
B、
倾倒液体
B、 稀释浓硫酸
C、
稀释浓硫酸
C、 闻气体气味
D、
闻气体气味
D、 测定溶液酸碱度
7. 化学是人类进步的阶梯。下列说法错误的是( )A、煤炭的脱硫处理可以有效减少酸雨的形成 B、用熟石灰可以改良酸性土壤 C、合成材料用途广泛,其废弃物也不会带来环境污染 D、不断开发新能源是减少碳排放实现碳中和的重要途径8. 下列用粒子观点解释错误的是( )A、酸有相似的化学性质——酸在溶液中都解离出H+ B、压瘪的乒乓球放入热水中重新鼓起——分子体积增大 C、酒香不怕巷子深——分子在不断运动 D、金刚石与石墨的硬度不同-——碳原子的排列方式不同9. 下列实验现象的描述正确的是( )A、铁在氧气中燃烧火星四射,生成黑色的四氧化三铁 B、点燃塑料和羊毛都会产生烧焦羽毛的气味 C、红磷在空气中燃烧时发出蓝色火焰,生成白色固体 D、打开盛有浓盐酸的试剂瓶盖,瓶口会出现大量白雾10. 下列每组中的物质在溶液中能大量共存的是( )A、H2SO4 、BaCl2 、NaOH B、Na2CO3 、Ca(NO3)2 、HCl C、MgCl2 、NaNO3 、 HCl D、CuSO4 、KOH 、 KCl11. 下列物质的俗名或名称与化学式对应的是( )A、烧碱—KOH B、熟石灰—CaO C、氦气—He2 D、小苏打—NaHCO312. 无人机的用途越来越广泛,可以用于航拍、喷洒农药等。制无人机框架宜选用密度小、强度高、硬度较大,化学稳定性好的金属材料,下列材料中最适合做无人机框架的是( )
测定溶液酸碱度
7. 化学是人类进步的阶梯。下列说法错误的是( )A、煤炭的脱硫处理可以有效减少酸雨的形成 B、用熟石灰可以改良酸性土壤 C、合成材料用途广泛,其废弃物也不会带来环境污染 D、不断开发新能源是减少碳排放实现碳中和的重要途径8. 下列用粒子观点解释错误的是( )A、酸有相似的化学性质——酸在溶液中都解离出H+ B、压瘪的乒乓球放入热水中重新鼓起——分子体积增大 C、酒香不怕巷子深——分子在不断运动 D、金刚石与石墨的硬度不同-——碳原子的排列方式不同9. 下列实验现象的描述正确的是( )A、铁在氧气中燃烧火星四射,生成黑色的四氧化三铁 B、点燃塑料和羊毛都会产生烧焦羽毛的气味 C、红磷在空气中燃烧时发出蓝色火焰,生成白色固体 D、打开盛有浓盐酸的试剂瓶盖,瓶口会出现大量白雾10. 下列每组中的物质在溶液中能大量共存的是( )A、H2SO4 、BaCl2 、NaOH B、Na2CO3 、Ca(NO3)2 、HCl C、MgCl2 、NaNO3 、 HCl D、CuSO4 、KOH 、 KCl11. 下列物质的俗名或名称与化学式对应的是( )A、烧碱—KOH B、熟石灰—CaO C、氦气—He2 D、小苏打—NaHCO312. 无人机的用途越来越广泛,可以用于航拍、喷洒农药等。制无人机框架宜选用密度小、强度高、硬度较大,化学稳定性好的金属材料,下列材料中最适合做无人机框架的是( ) A、生铁 B、黄铜 C、铝合金 D、纯铝13. 治疗疟疾的特效药——青蒿素的化学式为C15H22O5 , 下列关于青蒿素的说法错误的是( )A、青蒿素是由碳、氢、氧三种元素组成的有机物 B、青蒿素中共有42个原子 C、青蒿素中碳、氢、氧三种元素的质量比为90:11:40 D、每个青蒿素分子中含有22个氢原子14. “性质决定用途”是化学学科的重要观念,下列用途与性质对应错误的是( )A、气焊、气割时用到氧气——氧气具有氧化性 B、食品包装袋中充入氮气防腐——氮气化学性质不活泼 C、工业上高炉炼铁用到焦炭——碳具有还原性 D、医疗上血液制品的储存与运输用到干冰——二氧化碳不支持燃烧15. 现有X、Y、Z三种金属,把X和Y分别放入稀硫酸中,X溶解并产生气体,Y不反应;把Y和Z分别放入硝酸银溶液中,过一会,Y的表面有银析出,Z的表面没有变化。则三种金属的活动性顺序为( )A、X>Y>Z B、X>Z>Y C、Y>X>Z D、Y>X>Z16. 某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如下图,下列分析正确的是( )
A、生铁 B、黄铜 C、铝合金 D、纯铝13. 治疗疟疾的特效药——青蒿素的化学式为C15H22O5 , 下列关于青蒿素的说法错误的是( )A、青蒿素是由碳、氢、氧三种元素组成的有机物 B、青蒿素中共有42个原子 C、青蒿素中碳、氢、氧三种元素的质量比为90:11:40 D、每个青蒿素分子中含有22个氢原子14. “性质决定用途”是化学学科的重要观念,下列用途与性质对应错误的是( )A、气焊、气割时用到氧气——氧气具有氧化性 B、食品包装袋中充入氮气防腐——氮气化学性质不活泼 C、工业上高炉炼铁用到焦炭——碳具有还原性 D、医疗上血液制品的储存与运输用到干冰——二氧化碳不支持燃烧15. 现有X、Y、Z三种金属,把X和Y分别放入稀硫酸中,X溶解并产生气体,Y不反应;把Y和Z分别放入硝酸银溶液中,过一会,Y的表面有银析出,Z的表面没有变化。则三种金属的活动性顺序为( )A、X>Y>Z B、X>Z>Y C、Y>X>Z D、Y>X>Z16. 某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如下图,下列分析正确的是( ) A、配制过程中出现两处不符合题意 B、实验操作步骤为:计算、称量、量取、蒸发 C、需称量氯化钠的质量为7.0g D、溶液配制好后,将溶液存放在烧杯中,贴上标签即可17. 下列安全措施正确的是( )A、高楼住宅发生火灾时,乘电梯离开 B、炒菜时油锅着火,用锅盖盖灭 C、冬天用炭火取暖时,为防止一氧化碳中毒,在火炉旁放一盆水 D、不小心被蚊虫叮咬,可以涂一些硼酸溶液止痒止痛18. 分析推理是化学学习和研究中常用的思维方法。下列分析推理正确的是( )A、碱溶液的pH>7,所以pH>7的溶液一定是碱溶液 B、向某固体中加入盐酸有气体生成,则该固体可能是碳酸盐 C、酸与碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 D、物质燃烧都会有发光放热的现象,所以发光放热的现象都是燃烧
A、配制过程中出现两处不符合题意 B、实验操作步骤为:计算、称量、量取、蒸发 C、需称量氯化钠的质量为7.0g D、溶液配制好后,将溶液存放在烧杯中,贴上标签即可17. 下列安全措施正确的是( )A、高楼住宅发生火灾时,乘电梯离开 B、炒菜时油锅着火,用锅盖盖灭 C、冬天用炭火取暖时,为防止一氧化碳中毒,在火炉旁放一盆水 D、不小心被蚊虫叮咬,可以涂一些硼酸溶液止痒止痛18. 分析推理是化学学习和研究中常用的思维方法。下列分析推理正确的是( )A、碱溶液的pH>7,所以pH>7的溶液一定是碱溶液 B、向某固体中加入盐酸有气体生成,则该固体可能是碳酸盐 C、酸与碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 D、物质燃烧都会有发光放热的现象,所以发光放热的现象都是燃烧二、多选题
-
19. 甲和乙两种物质的溶解度曲线如图所示,下列分析正确的是( )
 A、甲的溶解度大于乙的溶解度 B、将a1℃的甲和乙的饱和溶液升温到a2℃时仍是饱和溶液 C、a1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液 D、将a2℃时甲的不饱和溶液降温到a1℃,不一定有晶体析出20. 一定条件下,在密闭容器中发生某一反应,测得反应前后各物质的质量如下表所示:
A、甲的溶解度大于乙的溶解度 B、将a1℃的甲和乙的饱和溶液升温到a2℃时仍是饱和溶液 C、a1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液 D、将a2℃时甲的不饱和溶液降温到a1℃,不一定有晶体析出20. 一定条件下,在密闭容器中发生某一反应,测得反应前后各物质的质量如下表所示:物质
甲
乙
丙
丁
反应前物质的质量/g
3.2
16.8
0.8
0.1
反应后物质的质量/g
x
8.4
3.0
1.0
下列说法正确的是( )
A、x=5.3 B、反应中生成丙与丁的质量比为3:1 C、乙一定是化合物 D、该反应属于分解反应三、填空题
-
21. 用化学用语填空:(1)、人体中含量最高的金属元素;(2)、氧化亚铁。22. 下表为元素周期表的一部分,表中数字表示原子序数。
 (1)、1号元素的原子与8号元素的原子相结合形成化合物的化学式可以为 或;(2)、17号元素对应的离子符号为;(3)、12号元素的原子结构示意图为。23. 2400℃时水能分解,其微观过程可用以下示意图表示,请按要求回答下列问题。
(1)、1号元素的原子与8号元素的原子相结合形成化合物的化学式可以为 或;(2)、17号元素对应的离子符号为;(3)、12号元素的原子结构示意图为。23. 2400℃时水能分解,其微观过程可用以下示意图表示,请按要求回答下列问题。 (1)、水分解过程示意图排列的正确顺序是(填标号)。(2)、2400℃时水分解的客观事实说明(填数字序号)。
(1)、水分解过程示意图排列的正确顺序是(填标号)。(2)、2400℃时水分解的客观事实说明(填数字序号)。①通常情况下水的性质稳定 ②水是一种元素 ③化学变化需要一定条件
(3)、2400℃时水分解的化学方程式为。24. 新冠疫情期间突然闹出来的“粮荒”,为世界粮食安全敲响了警钟,近日,袁隆平院士团队研究的海水稻,再次在我国青海高盐碱地区试种(高盐碱地土壤内水分pH超过8.5)。(1)、如果试种成功,将来人们有望吃到西部海水稻大米,大米提供的主要营养素是。(2)、由于海水稻生长在碱性土壤,与普通大米相比钠的含量较高,钠元素是人类所需的元素(填“常量”或“微量”)。(3)、为变废为宝,不断改良这种盐碱地,常在土地中施加(填“硫磺粉”或“熟石灰”)。(4)、水稻等农作物生长期间常施加一些肥料,下列物质属于复合肥料的是(填序号)。a.KNO3
b.CO(NH2)2
c.K2SO4
d.Ca3(PO4)2
25. 用如图实验验证CO2的性质。 (1)、观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是。(2)、观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是。26. 请回答下列问题。(1)、在做“铁丝在氧气中燃烧”实验时,预先要在集气瓶中放一些水,这样做的目的。(2)、要把块状冰糖溶于水,根据你的生活经验,有哪些方法可以加快冰糖溶解。(至少说两种)27. 今年新冠疫情在我国的一些地方爆发,我们要做好个人防护。酒精(C2H5OH)是预防新冠病毒扩散的一种重要的消毒剂。(1)、酒精是(填“可再生”或“不可再生”)资源。(2)、某同学配了一瓶酒精消毒剂,经测定其中酒精分子与水分子的个数比为1:1,此消毒剂中酒精与水的质量比为(最简比)。28. 某种粗盐水中有少量含、K+的杂质,小明用这种粗盐水经过下列实验流程想要制取纯净的氯化钠晶体。
(1)、观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是。(2)、观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是。26. 请回答下列问题。(1)、在做“铁丝在氧气中燃烧”实验时,预先要在集气瓶中放一些水,这样做的目的。(2)、要把块状冰糖溶于水,根据你的生活经验,有哪些方法可以加快冰糖溶解。(至少说两种)27. 今年新冠疫情在我国的一些地方爆发,我们要做好个人防护。酒精(C2H5OH)是预防新冠病毒扩散的一种重要的消毒剂。(1)、酒精是(填“可再生”或“不可再生”)资源。(2)、某同学配了一瓶酒精消毒剂,经测定其中酒精分子与水分子的个数比为1:1,此消毒剂中酒精与水的质量比为(最简比)。28. 某种粗盐水中有少量含、K+的杂质,小明用这种粗盐水经过下列实验流程想要制取纯净的氯化钠晶体。 (1)、固体A的化学式为。(2)、加稍过量盐酸时发生反应的化学方程式为。(3)、若将C溶液蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得晶体仍不是纯净的氯化钠,理由是。29. 牙膏中常用碳酸钙粉末做摩擦剂,利用石灰石(杂质不溶于水和酸)制备纯净碳酸钙的一种方法如下图。
(1)、固体A的化学式为。(2)、加稍过量盐酸时发生反应的化学方程式为。(3)、若将C溶液蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得晶体仍不是纯净的氯化钠,理由是。29. 牙膏中常用碳酸钙粉末做摩擦剂,利用石灰石(杂质不溶于水和酸)制备纯净碳酸钙的一种方法如下图。 (1)、反应①的化学方程式为 , 操作Ⅰ的名称是。(2)、反应②的化学方程式为 , 该反应属于反应(填基本反应类型)。30. 下图是实验室制取气体的常用装置,请回答下列问题。
(1)、反应①的化学方程式为 , 操作Ⅰ的名称是。(2)、反应②的化学方程式为 , 该反应属于反应(填基本反应类型)。30. 下图是实验室制取气体的常用装置,请回答下列问题。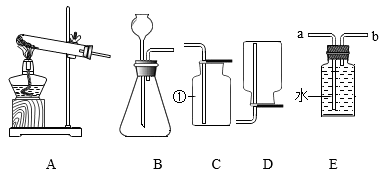 (1)、仪器①的名称是 , 该仪器(填“能”或“不能”)加热。(2)、实验室用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应的化学方程式为 , 若用E装置收集氧气,气体应从导管口 , (填“a”或“b”)进入。(3)、实验室用锌和稀硫酸反应制取氢气,反应的方程式为。(4)、实验室用石灰石与稀盐酸反应制取气体,应选用的发生装置和收集装置是。31. 为加深对酸的主要性质的认识,在学完酸的化学性质后,老师组织同学们进行了如下的实验探究。
(1)、仪器①的名称是 , 该仪器(填“能”或“不能”)加热。(2)、实验室用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应的化学方程式为 , 若用E装置收集氧气,气体应从导管口 , (填“a”或“b”)进入。(3)、实验室用锌和稀硫酸反应制取氢气,反应的方程式为。(4)、实验室用石灰石与稀盐酸反应制取气体,应选用的发生装置和收集装置是。31. 为加深对酸的主要性质的认识,在学完酸的化学性质后,老师组织同学们进行了如下的实验探究。
实验内容:
实验一:按图1所示完成实验。
实验二:往装有生锈铁钉的试管中加入足量的稀盐酸。
实验三:往滴有酚酞的氢氧化钠溶液中加入一定量的稀盐酸。
实验分析:
(1)、实验一中,观察到紫色石蕊溶液变色。(2)、实验二中,观察到溶液由无色变成发黄,一段时间后铁钉表面有气泡产生,请写出相关的化学方程式、。(3)、实验三中,观察到溶液由红色变成无色,由此分析,反应后所得溶液中,溶质成分的可能组合有(不考虑酚酞)、(用化学式表示)。应用与拓展:
(4)、小明在征得老师同意后,继续进行了如下实验,由下述实验可以得出氢氧化钙的性质有:、、。
四、计算题
-
32. 某化学兴趣小组的同学为了测定假黄金(铜锌合金)中锌的质量,取20g假黄金于试管中,取120g稀盐酸,分6次加入,充分反应后,实验数据如下:
实验次序
1
2
3
4
5
6
加入稀盐酸的质量(g)
20
20
20
20
20
20
剩余固体的质量(g)
18.7
17.4
m
14.8
13.5
13.5
请回答:
(1)、表中m=。(2)、20g假黄金中锌的质量为。(3)、所用稀盐酸的质量分数为多少?(写出计算过程)