广东省广州市番禺区2022年中考二模化学试题
试卷更新日期:2022-07-12 类型:中考模拟
一、单选题
-
1. 为有效阻断新型冠状病毒的传播,公众改变了许多生活习惯。下列做法主要涉及化学反应的是( )A、用医用酒精杀菌消毒 B、保持社交距离 C、改变握手拥抱礼节 D、出门配戴口罩2. 浓硫酸是重要的化工原料,生产、储存、运输浓硫酸过程中应张贴的标识是( )A、
 B、
B、 C、
C、 D、
D、 3. 空气质量指数(简称AQI)是依据常规监测的几种空气污染物浓度计算得到的,下列物质计入空气质量评价的污染物监测范畴的是( )A、CO2 B、SO2 C、N2 D、He4. 广州早茶虾饺早点口感鲜香,配料中虾仁富含的营养素是( )A、油脂 B、无机盐 C、糖类 D、蛋白质5. 下列有关水的叙述错误的是( )A、自然界中水的天然循环是水分子不断运动的结果 B、H2O与H2都含有氢分子 C、水在通电的条件下发生分解反应,分子种类发生变化 D、物质溶于水中,溶质的分子(或离子)分散到水分子中形成均一、稳定的混合物6. 在距地面10﹣50km的高空有一层臭氧(O3),它能吸收大部分紫外线,保护地球生物。臭氧与氧气在一定条件下能相互转化,臭氧属于( )A、酸 B、碱 C、单质 D、氧化物7. 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精可有效灭活病毒。现用95%的酒精配制75%的酒精,一般不会用到的仪器是( )A、
3. 空气质量指数(简称AQI)是依据常规监测的几种空气污染物浓度计算得到的,下列物质计入空气质量评价的污染物监测范畴的是( )A、CO2 B、SO2 C、N2 D、He4. 广州早茶虾饺早点口感鲜香,配料中虾仁富含的营养素是( )A、油脂 B、无机盐 C、糖类 D、蛋白质5. 下列有关水的叙述错误的是( )A、自然界中水的天然循环是水分子不断运动的结果 B、H2O与H2都含有氢分子 C、水在通电的条件下发生分解反应,分子种类发生变化 D、物质溶于水中,溶质的分子(或离子)分散到水分子中形成均一、稳定的混合物6. 在距地面10﹣50km的高空有一层臭氧(O3),它能吸收大部分紫外线,保护地球生物。臭氧与氧气在一定条件下能相互转化,臭氧属于( )A、酸 B、碱 C、单质 D、氧化物7. 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精可有效灭活病毒。现用95%的酒精配制75%的酒精,一般不会用到的仪器是( )A、 B、
B、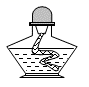 C、
C、 D、
D、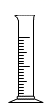 8. 磷肥可以促进作物生长,增强作物的抗寒、抗旱能力。下列化肥属于磷肥的是( )A、K2SO4 B、NH4Cl C、KNO3 D、Ca3 (PO4)29. 牛奶中能促进骨骼生长和牙齿坚固的化学元素是( )A、钠 B、铁 C、钙 D、锌10. 幸福需要辛勤的劳动来创造。下列劳动项目与所涉及的化学知识不相符的是( )
8. 磷肥可以促进作物生长,增强作物的抗寒、抗旱能力。下列化肥属于磷肥的是( )A、K2SO4 B、NH4Cl C、KNO3 D、Ca3 (PO4)29. 牛奶中能促进骨骼生长和牙齿坚固的化学元素是( )A、钠 B、铁 C、钙 D、锌10. 幸福需要辛勤的劳动来创造。下列劳动项目与所涉及的化学知识不相符的是( )选项
劳动项目
化学知识
A
用洗洁精清洗餐具
洗洁精的乳化作用
B
用液化石油气做饭
液化石油气的可燃性
C
用食醋清除水壶内壁的水垢
醋酸能与水垢反应
D
利用活性炭自制简易净水器
活性炭具有还原性
A、A B、B C、C D、D11. 2020年6月23日长征三号乙运载火箭成功发射北斗三号卫星,在火箭的制造中使用了钛和钛合金。钛元素在元素周期表中的相关信息如下图所示。下列说法错误的是( )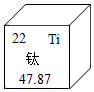 A、钛原子的中子数为22 B、钛元素属于金属元素 C、钛的元素符号是Ti D、钛元素的相对原子质量是47.8712. 盐湖地区人们常采用“夏天晒盐,冬天捞碱”的方法来获取 NaCl 和 Na2CO3。结合溶解度曲线判断,下列说法错误的是( )
A、钛原子的中子数为22 B、钛元素属于金属元素 C、钛的元素符号是Ti D、钛元素的相对原子质量是47.8712. 盐湖地区人们常采用“夏天晒盐,冬天捞碱”的方法来获取 NaCl 和 Na2CO3。结合溶解度曲线判断,下列说法错误的是( ) A、NaCl 的溶解度随温度变化不大 B、44 ℃时 Na2CO3饱和溶液的质量分数为 50% C、“夏天晒盐”的原理是让湖水蒸发结晶得到 NaCl D、“冬天捞碱”的原理是让湖水降温结晶得到 Na2CO313. 下列有关物质的除杂、鉴别所用的操作方法错误的是( )
A、NaCl 的溶解度随温度变化不大 B、44 ℃时 Na2CO3饱和溶液的质量分数为 50% C、“夏天晒盐”的原理是让湖水蒸发结晶得到 NaCl D、“冬天捞碱”的原理是让湖水降温结晶得到 Na2CO313. 下列有关物质的除杂、鉴别所用的操作方法错误的是( )选项
实验目的
操作方法
A
除去粗盐中的泥沙
加水溶解、过滤、洗涤、干燥
B
除去氧气中少量的水蒸气
通过盛有浓硫酸的洗气瓶
C
鉴别空气、氧气、二氧化碳
分别伸入燃着的小木条
D
鉴别氮肥(NH4Cl)和钾肥(KCl)
加熟石灰混合、研磨、闻气味
A、A B、B C、C D、D14. 科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图所示,下列说法错误的是( ) A、该反应的化学反应方程式为:2CO2+4H2O2CH3OH+3O2 B、生成物
A、该反应的化学反应方程式为:2CO2+4H2O2CH3OH+3O2 B、生成物 的化学式为CH3OH,该物质属于有机化合物
C、22g二氧化碳完全反应生成氧气的质量为16g
D、原子的种类和数目在反应前后都没有发生变化
的化学式为CH3OH,该物质属于有机化合物
C、22g二氧化碳完全反应生成氧气的质量为16g
D、原子的种类和数目在反应前后都没有发生变化
二、综合应用题
-
15. 2021年3月,三星堆遗址新出土重要文物500多件,有高2.62米的青铜大立人、高3.95米的青铜神树、象牙等,多属前所未见的稀世之珍。(1)、(一)青铜古称“吉金”是金属冶铸史上最早出现的合金,青铜属于(填“金属”或“合成”)材料,青铜的硬度比纯铜(填“大”或“小”)。(2)、(二)生活中铜制品长期露置在潮湿空气中会锈蚀,生成“铜绿”【化学式为Cu2(OH)2CO3】
【查阅资料】
【工艺流程】为从某锈蚀的铜样品中回收铜并制得硫酸锌,取该铜样品(除含有铜、锌和铜绿外,不含其它物质),进行如下操作:

请回答下列问题:
气体a中含有H2和(填化学式),“铜绿”【化学式为Cu2(OH)2CO3】中铜元素的化合价为。
(3)、操作Ⅰ的名称是 , 该操作中玻璃棒的作用是。(4)、写出②中发生反应的化学方程式:。16. 根据实验图示回答下列问题: (1)、写出图一中仪器a的名称。(2)、实验室用加热高锰酸钾固体的方法制取氧气,选择的发生装置是(填字母序字号),加热时,应使用酒精灯的焰集中加热;检验氧气可用。(3)、实验室可用铜片与浓硝酸在常温下反应制取二氧化氮(NO2)。通常状况下,二氧化氮是红棕色气体,溶于水时与水反应生成硝酸和一氧化氮(NO)。
(1)、写出图一中仪器a的名称。(2)、实验室用加热高锰酸钾固体的方法制取氧气,选择的发生装置是(填字母序字号),加热时,应使用酒精灯的焰集中加热;检验氧气可用。(3)、实验室可用铜片与浓硝酸在常温下反应制取二氧化氮(NO2)。通常状况下,二氧化氮是红棕色气体,溶于水时与水反应生成硝酸和一氧化氮(NO)。①制取NO2的发生装置可用(填字母)。
②收集NO2不用装置E原因是(用化学方程式表示)。
(4)、镁粉在火星上可以扮演地球上煤的角色,通过采用Mg/CO2金属粉末燃烧器可以为采矿车、电站等提供热能,其转化过程如图二:
已知:燃烧器中发生的主要反应为
①热气中一定含有的物质有(写一种即可)。
②通过上述反应,你对燃烧条件的新认识是。
17. 某校九年级“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如下实验,请回答下列问题: (1)、Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)、Ⅰ、如图所示装置进行实验,很快发现澄清的石灰水变浑浊;请写出C与CuO反应的化学方程式;
(2)、实验结束时,应(填写下列操作代号)。①先撤出导管,再熄灭酒精灯 ②先熄灭酒精灯,再撤出导管
(3)、Ⅱ、小组中小敏同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2 , 小组的同学们在老师指导下设计实验进行了验证:
已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
仪器B中所盛试剂为 , 其作用为。
(4)、D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有。(5)、实验前,需检查;点燃酒精灯前,先打开K,通入N2一段时间,其作用为。(6)、将1.44g炭和16.0gCuO在较高温度下反应生成Cu,理论上可生成g CO。(7)、Ⅲ、小组中吴华同学通过查阅资料发现:Cu2O为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。请设计简单实验验证CuO和足量炭反应后所得的红色固体中是否有Cu2O。
18. 为防止全球变暖,我国承诺在2060年要实现“碳中和”。减少化石燃料的使用,开发利用氢能,下图是利用太阳能制氢的示意图 (1)、上图实现了能量之间的相互转化,其中电解水的化学反应方程式为 , 该电解水过程是由电能转化为(填“化学能”或“热能”)。(2)、从微观的角度讲,每2个水分子分解,会产生个氢气分子。(3)、H2与CO2在一定条件下反应,生成甲醇(化学式:CH3OH)和H2O,该化学反应的方程式为: , 反应(填“属于”或“不属于”)置换反应。(4)、甲醇合成时,若碳元素全部来自于二氧化碳,则制取10吨甲醇需要消耗二氧化碳的质量是吨。19. 为探究盐酸的化学性质,某化学小组做了如下实验:
(1)、上图实现了能量之间的相互转化,其中电解水的化学反应方程式为 , 该电解水过程是由电能转化为(填“化学能”或“热能”)。(2)、从微观的角度讲,每2个水分子分解,会产生个氢气分子。(3)、H2与CO2在一定条件下反应,生成甲醇(化学式:CH3OH)和H2O,该化学反应的方程式为: , 反应(填“属于”或“不属于”)置换反应。(4)、甲醇合成时,若碳元素全部来自于二氧化碳,则制取10吨甲醇需要消耗二氧化碳的质量是吨。19. 为探究盐酸的化学性质,某化学小组做了如下实验: (1)、上述反应中有气体生成的是 , 有白色沉淀出现的是;B试管中所发生反应的化学方程式为。(2)、将反应后D和E试管中的废液倒入一洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
(1)、上述反应中有气体生成的是 , 有白色沉淀出现的是;B试管中所发生反应的化学方程式为。(2)、将反应后D和E试管中的废液倒入一洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl
猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl
猜想四:
(3)、【讨论与交流】经讨论,同学们一致认为猜想是错误的。(4)、【实验与结论】实验步骤
实验现象
实验结论
取少量滤液于试管中,滴加适量碳酸钠溶液
无现象
猜想四
成立
取少量滤液于试管中,加适量
(5)、【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在。20. 某兴趣小组查阅资料发现除去泥沙等杂质的粗盐,可能还含有CaCl2、MgCl2、Na2SO4等杂质。他们将该粗盐配成溶液,并对粗盐溶液进行探究和除杂。(1)、配制溶液时,加速粗盐溶解的玻璃仪器是。(2)、(探究过程)
步骤1:向粗盐溶液中加入过量NaOH溶液,未出现明显现象,说明溶液中无杂质,向溶液中继续滴加过量Na2CO3溶液,产生白色沉淀CaCO3固体,反应的化学方程式为。(3)、步骤2:向步骤1的滤液中滴加过量BaCl2溶液,产生白色沉淀,过滤:向滤液中滴加稀盐酸至溶液呈中性即得NaCl溶液。加稀盐酸除去的物质是。(初步结论)杂质成分已确定,且已完全除去。
(4)、(反思交流)小东认为Na2SO4还不能确定是否存在,可向步骤2的沉淀中滴加过量稀盐酸,若观察到的现象,证明粗盐中确实存在Na2SO4。
(5)、小红认为杂质也未完全除去,可按照步骤1和步骤2重新实验,并对调其中两种试剂的位置就能达到除杂目的,这两种试剂为 (填序号)。ANa2CO3溶液、BaCl2溶液 B稀盐酸、BaCl2溶液 CNaOH溶液、NaCO3溶液