北京市昌平区2022年中考二模化学试题
试卷更新日期:2022-07-12 类型:中考模拟
一、单选题
-
1. 空气成分中,体积分数最大的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体2. 决定元素种类的是( )A、中子数 B、质子数 C、核外电子数 D、最外层电子数3. 下列物质可用于鉴别硬水和软水的是( )A、活性炭 B、肥皂水 C、食盐水 D、酒精4. 下列富含维生素的物质是( )A、鸡蛋 B、大米 C、西瓜 D、花生油5. “高钙牛奶”中的钙应理解为( )A、离子 B、原子 C、分子 D、元素6. 地壳中含量最多的元素是( )A、硅 B、氧 C、铁 D、铝7. 下列不属于铁丝在氧气中燃烧现象的是( )A、放出热量 B、产生大量白烟 C、火星四射 D、生成黑色固体8. 下列物质中,属于溶液的是( )A、牛奶 B、豆浆 C、冰水 D、糖水9. 下列物质通常不会损害人体健康的是( )A、一氧化碳 B、黄曲霉素 C、甲醛 D、水10. 下列物质中,能用作氮肥的是( )A、NH4HCO3 B、K2SO4 C、K2CO3 D、Ca(H2PO4)211. 下列图标中,表示“禁止吸烟”的是( )A、
 B、
B、 C、
C、 D、
D、 12. 压瘪的乒乓球放入热水中重新鼓起是因为球内的气体分子( )A、体积增大 B、质量增大 C、间隔增大 D、个数增多13. 下列实验操作中,正确的是( )A、点燃酒精灯
12. 压瘪的乒乓球放入热水中重新鼓起是因为球内的气体分子( )A、体积增大 B、质量增大 C、间隔增大 D、个数增多13. 下列实验操作中,正确的是( )A、点燃酒精灯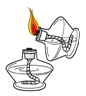 B、稀释浓硫酸
B、稀释浓硫酸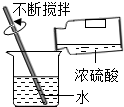 C、读取液体体积
C、读取液体体积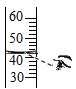 D、称量固体
D、称量固体 14. 中国茶道既是饮茶的艺术,也是生活的艺术。下列泡茶的主要步骤中,属于过滤操作的是( )A、投茶
14. 中国茶道既是饮茶的艺术,也是生活的艺术。下列泡茶的主要步骤中,属于过滤操作的是( )A、投茶 B、冲泡
B、冲泡 C、滤茶
C、滤茶 D、分茶
D、分茶 15. 下列符号能表示2个氯分子的是( )A、Cl2 B、2Cl2 C、2Cl D、2Cl-16. 下列物质的化学式错误的是( )A、生石灰——CaO B、熟石灰——Ca(OH)2 C、纯碱——NaOH D、小苏打——NaHCO317. 下列物质敞口放置于空气中,质量会增加的是( )A、食盐水 B、浓硫酸 C、浓盐酸 D、石灰石18. 下列物质溶于水时,溶液温度明显降低的是( )A、氯化钠 B、硝酸铵 C、浓硫酸 D、氢氧化钠19. “灭火弹”是一种新型灭火器,将其投入火灾现场,迅速释放出超细干粉,覆盖在可燃物表面,火被熄灭。灭火原理是( )A、移走可燃物 B、降低可燃物的着火点 C、隔绝氧气 D、降温至可燃物着火点以下20. 下列物质的用途中,利用其化学性质的是( )A、干冰用于人工降雨 B、天然气用作燃料 C、液氮用作冷冻剂 D、银用于制作导线21. 用如图装置可验证空气中O2的含量。下列说法错误的是( )
15. 下列符号能表示2个氯分子的是( )A、Cl2 B、2Cl2 C、2Cl D、2Cl-16. 下列物质的化学式错误的是( )A、生石灰——CaO B、熟石灰——Ca(OH)2 C、纯碱——NaOH D、小苏打——NaHCO317. 下列物质敞口放置于空气中,质量会增加的是( )A、食盐水 B、浓硫酸 C、浓盐酸 D、石灰石18. 下列物质溶于水时,溶液温度明显降低的是( )A、氯化钠 B、硝酸铵 C、浓硫酸 D、氢氧化钠19. “灭火弹”是一种新型灭火器,将其投入火灾现场,迅速释放出超细干粉,覆盖在可燃物表面,火被熄灭。灭火原理是( )A、移走可燃物 B、降低可燃物的着火点 C、隔绝氧气 D、降温至可燃物着火点以下20. 下列物质的用途中,利用其化学性质的是( )A、干冰用于人工降雨 B、天然气用作燃料 C、液氮用作冷冻剂 D、银用于制作导线21. 用如图装置可验证空气中O2的含量。下列说法错误的是( )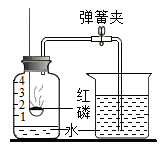 A、实验前一定要检查装置的气密性 B、该实验所用的红磷不可用木炭代替 C、待反应装置冷却至室温打开弹簧夹 D、集气瓶中水面最终上升至2处,证明了空气中氧气含量22. 碳在自然界的循环过程如图所示。下列说法中,错误的是( )
A、实验前一定要检查装置的气密性 B、该实验所用的红磷不可用木炭代替 C、待反应装置冷却至室温打开弹簧夹 D、集气瓶中水面最终上升至2处,证明了空气中氧气含量22. 碳在自然界的循环过程如图所示。下列说法中,错误的是( )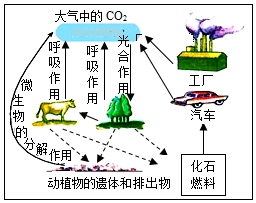 A、氧元素未参与该循环过程 B、绿色植物的光合作用可吸收CO2 C、控制化石燃料的使用可减少碳排放 D、动植物遗体被微生物分解可产生CO223. 天宫课堂中太空“冰球”实际上是在微重力环境下过饱和乙酸钠(CH3COONa)溶液结晶析出的过程。乙酸钠的溶解度如下表所示。下列说法正确的是( )
A、氧元素未参与该循环过程 B、绿色植物的光合作用可吸收CO2 C、控制化石燃料的使用可减少碳排放 D、动植物遗体被微生物分解可产生CO223. 天宫课堂中太空“冰球”实际上是在微重力环境下过饱和乙酸钠(CH3COONa)溶液结晶析出的过程。乙酸钠的溶解度如下表所示。下列说法正确的是( )温度/℃
21.5
26
30
34.5
40.5
49.5
50.5
溶解度/g
20.01
32.62
35.04
38.07
42.1
47.03
66.34
A、26℃时,100g乙酸钠饱和溶液中溶质质量为32.62g B、30℃时,100g乙酸钠饱和溶液的溶质质量分数为35.04% C、30℃时,将40g乙酸钠放入100g水中得到140g溶液 D、40.5℃时,100g水最多溶解42.1g乙酸钠二、选择题组
-
24. Tc(中文名“锝”)是一种医用放射性元素,在核医学诊断中具有多种功能。锝元素在元素周期表中的信息如下图。完成下面小题。(1)、下列关于锝元素的说法中,错误的是( )
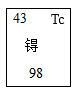 A、元素名称为锝 B、元素符号是Tc C、原子序数为43 D、相对原子质量为98g(2)、锝原子的核外电子数是( )A、43 B、55 C、98 D、141
A、元素名称为锝 B、元素符号是Tc C、原子序数为43 D、相对原子质量为98g(2)、锝原子的核外电子数是( )A、43 B、55 C、98 D、141三、填空题
-
25. 2021年5月,我国首辆火星车“祝融号”成功着陆。“祝融号”火星车的车身选用高强韧性的新型铝基碳化硅复合材料。
 (1)、碳化硅(SiC)中Si元素属于(填“金属”或“非金属”)元素。(2)、碳化硅属于____(填序号)。A、混合物 B、纯净物 C、化合物26. 我国冶炼金属的历史悠久。
(1)、碳化硅(SiC)中Si元素属于(填“金属”或“非金属”)元素。(2)、碳化硅属于____(填序号)。A、混合物 B、纯净物 C、化合物26. 我国冶炼金属的历史悠久。 (1)、后母戊鼎是由青铜制作,青铜属于(填“金属”或“合金”)。(2)、用CO高温还原法从赤铁矿石(主要成分为Fe2O3)中冶炼铁的化学方程式为。(3)、电解法冶炼铝的反应为2Al2O34Al+3O2↑,该反应中,化合价降低的元素是 , 该反应属于基本类型中的反应。27. 用如图实验装置验证水的组成。
(1)、后母戊鼎是由青铜制作,青铜属于(填“金属”或“合金”)。(2)、用CO高温还原法从赤铁矿石(主要成分为Fe2O3)中冶炼铁的化学方程式为。(3)、电解法冶炼铝的反应为2Al2O34Al+3O2↑,该反应中,化合价降低的元素是 , 该反应属于基本类型中的反应。27. 用如图实验装置验证水的组成。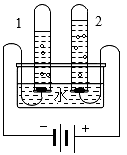 (1)、电解水发生反应的化学方程式为。(2)、实验得到“关于水的组成”的结论是。28. 农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。
(1)、电解水发生反应的化学方程式为。(2)、实验得到“关于水的组成”的结论是。28. 农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。 (1)、实验操作顺序为。(2)、②中需称量NaCl的质量为。29. 用下图实验验证可燃物燃烧的条件。已知:白磷的着火点为40℃,红磷的着火点为240℃,热水温度约为80℃。
(1)、实验操作顺序为。(2)、②中需称量NaCl的质量为。29. 用下图实验验证可燃物燃烧的条件。已知:白磷的着火点为40℃,红磷的着火点为240℃,热水温度约为80℃。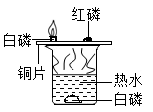 (1)、白磷燃烧的化学方程式为。(2)、对比铜片上和水中的白磷,得出可燃物燃烧的条件是。30. 用如图装置研究Na2CO3的性质。
(1)、白磷燃烧的化学方程式为。(2)、对比铜片上和水中的白磷,得出可燃物燃烧的条件是。30. 用如图装置研究Na2CO3的性质。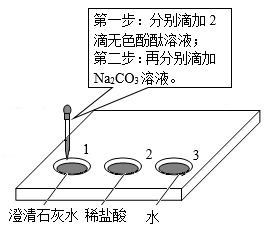 (1)、第一步后,溶液为无色的孔穴有(填孔穴序号)。(2)、第二步后,孔穴1中发生反应的化学方程式为。(3)、第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显(填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是。
(1)、第一步后,溶液为无色的孔穴有(填孔穴序号)。(2)、第二步后,孔穴1中发生反应的化学方程式为。(3)、第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显(填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是。四、科普阅读题
-
31. 阅读下面科普短文。
酿酒在中国由来已久,葡萄酒中含有丰富的有机物、颜色鲜艳、口感丰富,深受人们喜爱。红葡萄酒酿造工艺流程如下:采摘→破碎→发酵→压榨→陈化→倒桶→澄清→装瓶
葡萄的种植与采摘可影响葡萄酒的口感、色泽等。新鲜的红葡萄进入酿酒厂首先会经过粉碎处理。粉碎的葡萄皮、果肉、汁液混合放入发酵容器,加入酵母进行发酵。葡萄汁中的多糖在酵母作用下水解为葡萄糖(C6H12O6),葡萄糖在酵母的作用下生成酒精等物质。温度、pH等会影响酿酒酵母的生长,因此也会影响葡萄酒发酵的效果。图1为不同温度下酿酒酵母的生长曲线,其中OD600nm值越大反映出酿酒酵母的浓度也越大。

表1
浸渍时间/天
酒精度/(V/V%)
色度
4
12.4
4.9
5
12.3
5.8
7
12.4
5.4
9
12.5
5.2
葡萄酒的色泽来自葡萄皮中的花色苷和单宁类物质,会受到浸渍发酵时间的影响。表1为浸渍发酵温度26~28℃,不同浸渍时间某赤霞珠葡萄酒色度与酒精度的关系。
不锈钢罐、水泥槽、木桶等可被当作发酵容器。发酵结束后的葡萄酒再经过压榨、陈化、倒桶、澄清、装瓶等操作就能得到可口的红葡萄酒。
依据文章内容回答下列问题。
(1)、葡萄糖(C6H12O6)由种元素组成。(2)、请补全葡萄糖在酵母的作用下分解为乙醇的化学方程式:C6H12O62C2H5OH+2↑。(3)、根据图1可以得出在相同时间内,温度与酿酒酵母浓度的关系是。(4)、判断下列说法是否正确(正确的画√,错误的画×)。①采摘、破碎、发酵、压榨四个流程只发生了物理变化。
②根据表1可知,发酵时间越长葡萄酒色度越大。
32. 2022年北京冬奥会上氢能的应用十分广泛,以下是获得氢气的一种方法,其工业流程如下。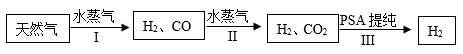 (1)、I中反应的微观示意图如下,在方框中补全另一种产物的微粒图示。
(1)、I中反应的微观示意图如下,在方框中补全另一种产物的微粒图示。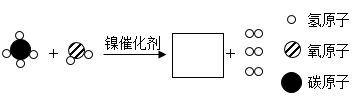 (2)、Ⅲ中PSA提纯也称为变压吸附,利用吸附剂(活性炭、分子筛等)的多孔性结构提纯气体,发生的变化属于(填“物理”或“化学”)变化。(3)、以上流程获得氢气的原料是。33. 印制电板制造业是电子信息产业的基础,从其废液(主要成分是CuCl2)中获得产品CuSO4的工业流程如下。
(2)、Ⅲ中PSA提纯也称为变压吸附,利用吸附剂(活性炭、分子筛等)的多孔性结构提纯气体,发生的变化属于(填“物理”或“化学”)变化。(3)、以上流程获得氢气的原料是。33. 印制电板制造业是电子信息产业的基础,从其废液(主要成分是CuCl2)中获得产品CuSO4的工业流程如下。已知:Cu(OH)2难溶于水。
 (1)、产品CuSO4属于____(填序号)。A、酸 B、碱 C、盐 D、氧化物(2)、反应池中发生反应的类型属于复分解反应,写出该反应的化学方程式。(3)、煅烧炉中发生的反应为:Cu(OH)2CuO+H2O,酸浸槽加入的酸溶液X为。34. 根据下图回答问题。
(1)、产品CuSO4属于____(填序号)。A、酸 B、碱 C、盐 D、氧化物(2)、反应池中发生反应的类型属于复分解反应,写出该反应的化学方程式。(3)、煅烧炉中发生的反应为:Cu(OH)2CuO+H2O,酸浸槽加入的酸溶液X为。34. 根据下图回答问题。 (1)、仪器a的名称是。(2)、加热高锰酸钾制取氧气的化学方程式为。(3)、收集氧气的装置是C或(填序号)。35. 用如图装置验证CO2的性质。
(1)、仪器a的名称是。(2)、加热高锰酸钾制取氧气的化学方程式为。(3)、收集氧气的装置是C或(填序号)。35. 用如图装置验证CO2的性质。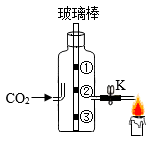 (1)、实验室制取CO2的化学方程式为。(2)、打开K,观察到蜡烛熄灭,得到的结论是。(3)、瓶中玻璃棒上①③为湿润的石蕊滤纸条,②为干燥的石蕊滤纸条。该实验的目的是。36. 利用如图装置(气密性已检验)验证Fe的化学性质。
(1)、实验室制取CO2的化学方程式为。(2)、打开K,观察到蜡烛熄灭,得到的结论是。(3)、瓶中玻璃棒上①③为湿润的石蕊滤纸条,②为干燥的石蕊滤纸条。该实验的目的是。36. 利用如图装置(气密性已检验)验证Fe的化学性质。 (1)、将稀H2SO4加入试管中,可观察到的现象是 , 发生反应的化学方程式为。(2)、继续向试管中注入CuSO4溶液,观察到Fe片表面产生红色固体,原因是。37. 目前市场上主流的“茶垢清洁剂”的主要成分为过碳酸钠(2Na2CO3·3H2O2),热水溶解后,能迅速产生活性气体,快速清洁茶具上附着的茶垢。
(1)、将稀H2SO4加入试管中,可观察到的现象是 , 发生反应的化学方程式为。(2)、继续向试管中注入CuSO4溶液,观察到Fe片表面产生红色固体,原因是。37. 目前市场上主流的“茶垢清洁剂”的主要成分为过碳酸钠(2Na2CO3·3H2O2),热水溶解后,能迅速产生活性气体,快速清洁茶具上附着的茶垢。【查阅资料】
过碳酸钠俗称固体双氧水,外观为白色结晶或结晶性粉末,易溶于水,水溶液中含有Na2CO3和H2O2。
I.探究“茶垢清洁剂”遇热水产生气体的成分
【进行实验】
向盛有适量“茶垢清洁剂”的大试管中加入足量热水,观察到有大量无色气泡产生。
(1)、【解释与结论】证明产生气体是氧气的实验方法为。
(2)、H2O2反应生成氧气的化学方程式为。(3)、Ⅱ.探究制备过碳酸钠的最佳条件【进行实验】取6.0g35%H2O2溶液加入烧杯中,加入稳定剂15mL;边搅拌,边加入3.5gN2CO3固体,搅拌下使过碳酸钠完全析出,分析产品质量。分别在不同温度下进行4次实验,结果见下表。
序号
t/℃
活性氧百分含量/%
产率/%
①
5~10
13.94
85.49
②
10~15
14.02
85.78
③
15~20
15.05
88.38
④
20~25
14.46
83.01
【解释与结论】
以上实验的目的是。
(4)、比较实验③和④发现温度越高而过碳酸钠的产率越低,其原因可能是。(5)、【反思与评价】欲进一步证明过碳酸钠溶液中含有碳酸盐,所需试剂是。
(6)、若要继续探究制作过碳酸钠的最佳原料比(35%H2O2溶液与Na2CO3的质量比),除应用相同的实验仪器和操作步骤外,还需其他相同的条件是。五、计算题
-
38. 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。CO2加氢制甲醇的总反应可表示为:CO2+3H2CH3OH+H2O,若制得甲醇16t,计算减少CO2的质量(写出计算过程及结果)。
-