浙教版科学八上1.6物质的分离
试卷更新日期:2022-07-11 类型:同步测试
一、单选题
-
1. 河水净化制自来水的主要步骤如下图所示, 有关说法错误的是( )
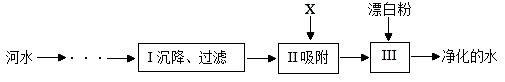 A、步骤Ⅰ可除去难溶性杂质 B、X 试剂可以是活性炭 C、步骤Ⅲ可杀菌、消毒 D、“净化的水”为纯净水2. 正确规范的实验操作非常重要,下列操作规范的是( )A、称量
A、步骤Ⅰ可除去难溶性杂质 B、X 试剂可以是活性炭 C、步骤Ⅲ可杀菌、消毒 D、“净化的水”为纯净水2. 正确规范的实验操作非常重要,下列操作规范的是( )A、称量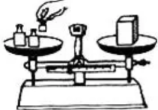 B、溶解
B、溶解 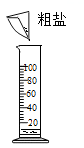 C、过滤
C、过滤 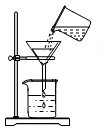 D、蒸发结晶
D、蒸发结晶 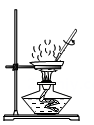 3. 口罩可阻挡粉尘、飞沫、病毒等进入口鼻,从而保护人体。这一作用相当于物质分离方法中的( )A、沉淀 B、过滤 C、蒸馏 D、结晶4. 下列关于玻璃棒在实验操作中的用途完全正确的是( )
3. 口罩可阻挡粉尘、飞沫、病毒等进入口鼻,从而保护人体。这一作用相当于物质分离方法中的( )A、沉淀 B、过滤 C、蒸馏 D、结晶4. 下列关于玻璃棒在实验操作中的用途完全正确的是( )①在溶解固体时,使用玻璃棒搅拌是为了加速固体物质的溶解
②在过滤时,沿玻璃棒倾倒待过滤的液体,玻璃棒具有引流的作用
③在浓缩蒸发液体时,使用玻璃棒搅拌是为了使液体均匀受热,防止液体等溅出
A、仅①② B、仅①③ C、仅②③ D、全部5. 在野外和灾区,可用下列步骤将河水转化成饮用水:①化学沉降(用明矾);②消毒杀菌(漂白粉);③自然沉降;④加热煮沸。以上处理过程最合理的顺序是( )
A、③②①④ B、③①②④ C、③①④② D、①③②④6. 如图所示为三种实验操作,下列说法正确的是( ) A、进行如图甲所示的过滤操作,可从食盐溶液中获得食盐固体 B、进行如图乙所示的蒸发操作,当蒸发皿中出现较多固体时停止加热 C、进行如图丙所示的蒸馏操作,冷凝管管进出水的方向是a进b出 D、在粗盐提纯实验中,需要用到图示甲、乙、丙三种操作7. 预防感染新冠肺炎,口罩成了不可或缺的利器。医用防护口罩通常有三层,其层状结构及对外在物质的防护作用如图所示。医用防护口罩起防护作用的主要原理是( )
A、进行如图甲所示的过滤操作,可从食盐溶液中获得食盐固体 B、进行如图乙所示的蒸发操作,当蒸发皿中出现较多固体时停止加热 C、进行如图丙所示的蒸馏操作,冷凝管管进出水的方向是a进b出 D、在粗盐提纯实验中,需要用到图示甲、乙、丙三种操作7. 预防感染新冠肺炎,口罩成了不可或缺的利器。医用防护口罩通常有三层,其层状结构及对外在物质的防护作用如图所示。医用防护口罩起防护作用的主要原理是( ) A、杀菌 B、消毒 C、过滤 D、干燥8. 一杯60 ℃、100克不饱和的硝酸钾溶液,逐渐恒温蒸发水时溶液质量的变化如下表所示:由上表可知蒸发水时析出了晶体的是( )
A、杀菌 B、消毒 C、过滤 D、干燥8. 一杯60 ℃、100克不饱和的硝酸钾溶液,逐渐恒温蒸发水时溶液质量的变化如下表所示:由上表可知蒸发水时析出了晶体的是( )实验次数 1 2 3 蒸发水的质量/克 2 2 2 剩余溶液的质量/克 98 96 93 A、第1次 B、第2次 C、第3次 D、都没有晶体析出9. 下列有关水和溶液的说法正确的是( )A、溶液是均一、稳定的溶质均匀分散在溶剂中且静止不动 B、天然水经沉降、过滤、活性炭吸附后得到的水是纯净水 C、将植物油溶解于水可形成溶液 D、配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数10. 水是生命之源。城市生活用水经自来水厂净化处理的过程如图。下列说法错误的是( ) A、通过反应沉淀池、过滤池除去水中不溶性杂质 B、自来水厂投入明矾进行消毒 C、吸附池内常用活性炭吸附色素和异味 D、自然界中的水都不是纯水11. 运用概念分类有助于我们对知识进一步理解和掌握。下列选项中的分类不完整的是( )A、
A、通过反应沉淀池、过滤池除去水中不溶性杂质 B、自来水厂投入明矾进行消毒 C、吸附池内常用活性炭吸附色素和异味 D、自然界中的水都不是纯水11. 运用概念分类有助于我们对知识进一步理解和掌握。下列选项中的分类不完整的是( )A、 B、
B、 C、
C、 D、
D、 12. 测定粗盐纯度,需经过称量、溶解、过滤、蒸发结晶下列操作规范的是( )A、
12. 测定粗盐纯度,需经过称量、溶解、过滤、蒸发结晶下列操作规范的是( )A、 称量
B、
称量
B、 溶解
C、
溶解
C、 过滤
D、
过滤
D、 蒸发结晶
13. 对于下列各图的相关叙述,正确的是( )
蒸发结晶
13. 对于下列各图的相关叙述,正确的是( )
 A、如图甲,在探究飞机获得升力与机翼形状关系的实验中,当风吹向机翼模型时弹簧秤甲 示数减小。 B、如图乙,在制备硫酸铜晶体的实验中,实验原理与“夏天晒盐”原理相同。 C、如图丙,可以用活性炭吸附海水中的杂质,再过滤煮沸后,即可饮用。 D、如图丁,在蒸馏实验中,冷凝水的流向为从上往下。14. 下列实验操作中玻璃棒的作用与其他三组不同的是( )A、配制蔗糖溶液
A、如图甲,在探究飞机获得升力与机翼形状关系的实验中,当风吹向机翼模型时弹簧秤甲 示数减小。 B、如图乙,在制备硫酸铜晶体的实验中,实验原理与“夏天晒盐”原理相同。 C、如图丙,可以用活性炭吸附海水中的杂质,再过滤煮沸后,即可饮用。 D、如图丁,在蒸馏实验中,冷凝水的流向为从上往下。14. 下列实验操作中玻璃棒的作用与其他三组不同的是( )A、配制蔗糖溶液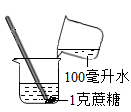 B、过滤泥水
B、过滤泥水 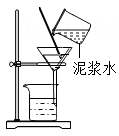 C、获取氯化钠晶体
C、获取氯化钠晶体 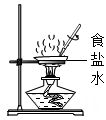 D、配制 10%的食盐水
D、配制 10%的食盐水  15. 20℃时,四个实验小组分别取不同质量的食盐,逐渐加入到各盛有 50g 水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量溶液的质量。记录数据如下表:
15. 20℃时,四个实验小组分别取不同质量的食盐,逐渐加入到各盛有 50g 水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量溶液的质量。记录数据如下表:实验小组
第一组
第二组
第三组
第四组
水的质量/克
50
50
50
50
食盐的质量/克
15
20
25
30
溶液质量/克
65
68
m
68
下列说法错误的是( )
A、 表格中 m 值为 68 B、0℃时,50 克水中最多可溶 18 克食盐 C、相同温度下,把水的质量增加到 100 克,食盐在水里的溶解度增大 D、用蒸发溶剂结晶的方法可以重新获得溶解了的食盐16. 宋代《开宝本草》中记载了硝酸钾晶体的提纯方法,“……所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”。其中没有涉及到的实验方法是( )A、溶解 B、蒸发 C、蒸馏 D、结晶17. 小柯同学在实验室做了粗盐提纯的实验,再用提纯得到的精盐配置10%的氯化钠溶液50g,下列说法错误的是( ) A、这两个实验的正确操作顺序是①④⑤②③① B、②的操作中若发现指针左偏应继续加砝码或向右调节游码 C、③的操作会使得到的氯化钠溶液溶质质量分数比10%小一些 D、⑤的操作中玻璃棒的作用是搅拌防止局部温度过高,造成液体飞溅18. 《本草纲目》中“黄连”条目下记载:“吐血不止,去黄连一两,捣碎,加鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是( )A、加热 B、称量 C、过滤 D、蒸发结晶19. 下列有关水和溶液的说法正确的是( )A、溶液是均一、稳定的溶质均匀分散在溶剂中且静止不动 B、天然水经沉降、过滤、活性炭吸附后得到的水是纯净水 C、通过洗洁精的乳化作用,可将植物油溶解于水形成溶液 D、配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数20. 下列实验操作中错误的是( )A、取用固体药品
A、这两个实验的正确操作顺序是①④⑤②③① B、②的操作中若发现指针左偏应继续加砝码或向右调节游码 C、③的操作会使得到的氯化钠溶液溶质质量分数比10%小一些 D、⑤的操作中玻璃棒的作用是搅拌防止局部温度过高,造成液体飞溅18. 《本草纲目》中“黄连”条目下记载:“吐血不止,去黄连一两,捣碎,加鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是( )A、加热 B、称量 C、过滤 D、蒸发结晶19. 下列有关水和溶液的说法正确的是( )A、溶液是均一、稳定的溶质均匀分散在溶剂中且静止不动 B、天然水经沉降、过滤、活性炭吸附后得到的水是纯净水 C、通过洗洁精的乳化作用,可将植物油溶解于水形成溶液 D、配制好的溶液装瓶时不慎洒出少量,不会影响溶液溶质质量分数20. 下列实验操作中错误的是( )A、取用固体药品 B、倾倒液体药品
B、倾倒液体药品  C、过滤泥浆水
C、过滤泥浆水  D、蒸发食盐水
D、蒸发食盐水 
二、实验探究题
-
21. 某兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50克20%的氯化钠溶液。请回答下列有关问题:
实验一:以下是同学们做粗盐提纯实验的操作示意图。

a.图C中玻璃棒的作用是。
b.图D为过滤装置,其漏斗中滤纸的放置方向应为(填序号)。
实验二:用提纯后得到的精盐配制了氯化钠溶液,经检测,溶质质量分数偏小,其原因可能有(填序号)。
A.氯化钠固体仍然不纯
B.用量筒量取水时,仰视读数
C.配制好的溶液装瓶时,有少量溶液洒出
22. 海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,某兴趣小组同学按甲图中的步骤将粗盐进行提纯。

 (1)、甲图中的操作①为乙图中的(填字母),操作②为过滤,若两次过滤后滤液仍浑浊,原因可能是。(写出一种)(2)、利用提纯出的精盐配制100克12%的食盐溶液,必须用到的仪器是 。A、烧杯 B、10mL量筒 C、100mL量筒 D、漏斗(3)、若(2)中配制的食盐溶液的溶质质量分数大于12%,则可能的原因是 。A、称量食盐时,砝码放左盘,食盐放右盘 B、将称量好的食盐倒入烧杯时,有食盐固体洒落烧杯外 C、将量好的水倒入烧杯时,有少量水溅出 D、量取液体时,俯视读数23. 粗盐是含有较多可溶性杂质(如氯化镁和氯化钙等)和不溶性杂质(如泥沙等)的氯化钠。为提纯粗盐,同学们经过了①蒸发结晶;②溶解;③过滤;④计算产率等步骤。(1)、实验过程中,合理的操作步骤为 (填序号)。(2)、实验③中玻璃棒的作用是。(3)、实验结束后,4个小组分别计算了精盐产率,老师的评价是:第1组结果偏高,于是各组分别讨论了第1组的误差,所找原因合理的是( )
(1)、甲图中的操作①为乙图中的(填字母),操作②为过滤,若两次过滤后滤液仍浑浊,原因可能是。(写出一种)(2)、利用提纯出的精盐配制100克12%的食盐溶液,必须用到的仪器是 。A、烧杯 B、10mL量筒 C、100mL量筒 D、漏斗(3)、若(2)中配制的食盐溶液的溶质质量分数大于12%,则可能的原因是 。A、称量食盐时,砝码放左盘,食盐放右盘 B、将称量好的食盐倒入烧杯时,有食盐固体洒落烧杯外 C、将量好的水倒入烧杯时,有少量水溅出 D、量取液体时,俯视读数23. 粗盐是含有较多可溶性杂质(如氯化镁和氯化钙等)和不溶性杂质(如泥沙等)的氯化钠。为提纯粗盐,同学们经过了①蒸发结晶;②溶解;③过滤;④计算产率等步骤。(1)、实验过程中,合理的操作步骤为 (填序号)。(2)、实验③中玻璃棒的作用是。(3)、实验结束后,4个小组分别计算了精盐产率,老师的评价是:第1组结果偏高,于是各组分别讨论了第1组的误差,所找原因合理的是( )组别
1
2
3
4
精盐产率
91%
69%
73%
75%
A、蒸发结晶时有少量液体飞溅出去。 B、没有蒸发干,精盐中仍然有水分。 C、烧杯里的食盐未溶解完就开始过滤。24. 小明在将粗盐提纯后, 再配制了溶质质量分数为 0.9%的生理盐水, 请你帮助他完成下 列实验过程。(1)、实验过程包括、过滤、蒸发结晶、洗涤烘干、计算、称量、溶解、装瓶等环节。(2)、在过滤环节需要对圆形滤纸作折叠处理 (虚线表示沿此线折叠) ,右图中正确 的折叠步骤依次为。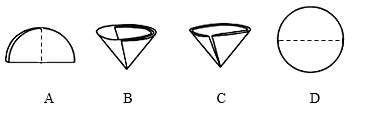 (3)、在过滤时玻璃棒的作用是。(4)、如果要配制 200 克生理盐水, 则在称量环节需要定量称取精盐的质量为克。25. 已知该粗盐中的主要杂质是泥沙。某同学在实验室做粗盐提纯的操作步骤如下:
(3)、在过滤时玻璃棒的作用是。(4)、如果要配制 200 克生理盐水, 则在称量环节需要定量称取精盐的质量为克。25. 已知该粗盐中的主要杂质是泥沙。某同学在实验室做粗盐提纯的操作步骤如下:步骤1:用天平称取5克粗盐,用药匙将粗盐逐渐加入盛有20mL水的烧杯里,边加边用玻璃棒搅拌,直到粗盐完全溶解为止。玻璃棒在这里搅拌的目的是。
步骤2:将步骤1得到混合物进行过滤,过滤操作中用到的玻璃仪器有: , 过滤后留在滤纸上的主要物质是(填“泥沙”“食盐”)。
步骤3:将所得的澄清溶液倒入蒸发皿,进行蒸发结晶。
三、填空题
-
26. 氯化钠和硝酸钾两种物质的溶解度随温度的变化见下表:
温度/℃
溶解度/g
0
20
40
60
80
100
氯化钠
35.7
36
36.6
37.3
38.4
39.8
硝酸钾
13.3
31.6
63.9
110
169
246
(1)、从氯化钠溶液中得到氯化钠固体应采用的方法是。(2)、20℃时,向100g水中加入50g硝酸钾,充分溶解后形成的溶液是硝酸钾的 (填“饱和”或“不饱和”)溶液。再将温度升高到60℃时,溶液的质量为克。27. 水是生命之源,保护水资源人人有责。(1)、发源于天台里石门水库的北干渠,长72.3公里,主要解决天台县大部分及三门县部分农田用水问题。北干渠工程影响水循环途径中的环节是 。(2)、如图是水厂净化水的过程,则水厂生产自来水时使用的净水方法有 。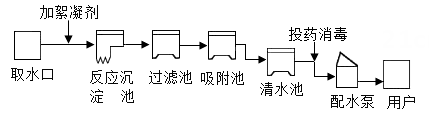 A、沉淀 B、过滤 C、煮沸 D、蒸馏 E、吸附28. A物质的溶解度如下表所示,某同学利用A物质进行了图甲实验。
A、沉淀 B、过滤 C、煮沸 D、蒸馏 E、吸附28. A物质的溶解度如下表所示,某同学利用A物质进行了图甲实验。
温度(℃)
20
50
溶解度/g
30
110
(1)、①~④杯溶液中,是该温度下A物质的饱和溶液的是:。(填序号)(2)、④中溶液的溶质质量分数是。(3)、像A这种溶解度受温度影响较大的固体物质,一般用的方法获得晶体。29. 右图为 A 、B 两种固体物质的溶解度曲线, 请结合图形回答下列 问题。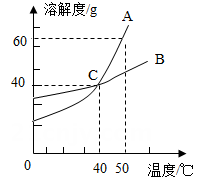 (1)、交点C表示的意义是:在℃时,A、B两种物质的溶解度相等;(2)、50℃时,A的饱和溶液中溶质与溶剂的质量比为;(3)、如果在大量的A中含有少量杂质B,要提纯A,可先将样品配制成溶液,再采取(选填“蒸发溶剂”或“冷却热饱和溶液”)结晶的方法获得更高纯度的A。30. 如图是进行粗盐提纯实验的步骤图,请回答:
(1)、交点C表示的意义是:在℃时,A、B两种物质的溶解度相等;(2)、50℃时,A的饱和溶液中溶质与溶剂的质量比为;(3)、如果在大量的A中含有少量杂质B,要提纯A,可先将样品配制成溶液,再采取(选填“蒸发溶剂”或“冷却热饱和溶液”)结晶的方法获得更高纯度的A。30. 如图是进行粗盐提纯实验的步骤图,请回答: (1)、操作Ⅲ、IV、V中都用到的玻璃仪器是玻璃棒,该仪器在操作IV中的作用是。(2)、粗盐提纯实验步骤较多、操作烦琐,可以缩短粗盐提纯实验时间的正确操作是 。A、研碎粗盐 B、溶解时多加一倍的水 C、过滤时玻璃棒紧靠一层滤纸处 D、蒸发时不要用玻璃棒搅拌散热(3)、各小组的产率及评价如下:
(1)、操作Ⅲ、IV、V中都用到的玻璃仪器是玻璃棒,该仪器在操作IV中的作用是。(2)、粗盐提纯实验步骤较多、操作烦琐,可以缩短粗盐提纯实验时间的正确操作是 。A、研碎粗盐 B、溶解时多加一倍的水 C、过滤时玻璃棒紧靠一层滤纸处 D、蒸发时不要用玻璃棒搅拌散热(3)、各小组的产率及评价如下:组别
1
2
3
4
产率
75%
83%
83%
72%
老师对产率的评价
偏低
偏高
偏高
偏低
下列各组同学对造成产率偏高或偏低的原因分析,正确的是 。
A、第1组:烧杯里的食盐末溶解完就开始过滤 B、第2组:蒸发时,有固体物质飞溅 C、第3组:滤液浑浊就开始蒸发 D、第4组:蒸发后,精盐中还有水分31. 死海因其高盐度出名,美国科学家对其十分好奇,做了一个实验:(如图)他们将一件黑色礼服用钢丝固定,放入死海中,两年后取出,发现衣服表面挂满了白色盐晶。经检测,晶体中的成分主要包含氯化钠、氯化钙、氯化钾等。 (1)、黑色礼服上的白色盐晶,在这两年中经历的最主要过程 。A、凝固 B、蒸馏 C、结晶 D、升华(2)、死海中盐类的质量分数始终保持在25%左右不再升高,试分析原因。32. 学习科学以后,我们对水有了更全面的认识。关于“水”回答下列问题:
(1)、黑色礼服上的白色盐晶,在这两年中经历的最主要过程 。A、凝固 B、蒸馏 C、结晶 D、升华(2)、死海中盐类的质量分数始终保持在25%左右不再升高,试分析原因。32. 学习科学以后,我们对水有了更全面的认识。关于“水”回答下列问题: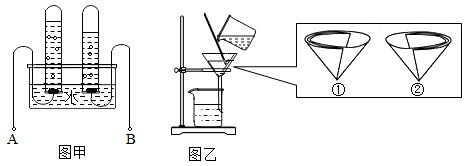 (1)、将少量①菜油、②醋、③蔗糖、④胡椒粉、⑤味精粉、⑥面粉分别加入水中振荡,其中形成乳浊液。(填序号)(2)、下图甲为电解水的装置图,图中 A 端接的是电源的极。(填“正”或“负”)(3)、将浑浊的河水用下图乙所示的装置进行净化,净化后得到的清澈的水是(填“纯净物”或“混合物”)。在该装置中,其漏斗中滤纸的放置方向应为(填序号)。33. 小明同学得到了如下关于A、B的两种固体物质的溶解度表:
(1)、将少量①菜油、②醋、③蔗糖、④胡椒粉、⑤味精粉、⑥面粉分别加入水中振荡,其中形成乳浊液。(填序号)(2)、下图甲为电解水的装置图,图中 A 端接的是电源的极。(填“正”或“负”)(3)、将浑浊的河水用下图乙所示的装置进行净化,净化后得到的清澈的水是(填“纯净物”或“混合物”)。在该装置中,其漏斗中滤纸的放置方向应为(填序号)。33. 小明同学得到了如下关于A、B的两种固体物质的溶解度表:温度(℃)
0
10
20
30
40
溶解度(g)
A
35
35.5
36
36.5
37
B
6
10
18
36.5
50
(1)、若将B物质从溶液中结晶析出,宜采用的方法是:。(2)、10℃,将10克B物质加入到90克水中时,溶质质量分数(计算结果保留一位小数)。34. 实验课上,小明进行粗盐提纯实验,根据要求回答下列问题。(1)、图甲为过滤装置,其漏斗中滤纸的放置方向应为(填序号) (2)、图乙物品中可以替代滤纸进行过滤实验的是。(3)、在粗盐溶解步骤中需要控制水的用量不宜过多的原因有 (填字母)。A、节约实验时间 B、保证固体混合物全部溶解 C、节约能源35. 温州产盐历史悠久,常用粗盐提纯的方法(如图所示)得到精盐。
(2)、图乙物品中可以替代滤纸进行过滤实验的是。(3)、在粗盐溶解步骤中需要控制水的用量不宜过多的原因有 (填字母)。A、节约实验时间 B、保证固体混合物全部溶解 C、节约能源35. 温州产盐历史悠久,常用粗盐提纯的方法(如图所示)得到精盐。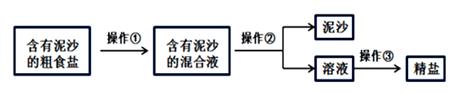 (1)、实验流程中的操作②是。(2)、如果过滤后所得滤液依旧浑浊,可能原因是。(3)、以上实验得到的精盐存在少量氯化镁,从物质分类角度看,精盐属于(选填“纯净物”或“混合物”)
(1)、实验流程中的操作②是。(2)、如果过滤后所得滤液依旧浑浊,可能原因是。(3)、以上实验得到的精盐存在少量氯化镁,从物质分类角度看,精盐属于(选填“纯净物”或“混合物”)四、解答题
-
36. 水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
 (1)、自来水生产过程中用到了活性炭,利用其性,可以除去水中的色素和异味。(2)、流入过滤池中的混合物属于(填“溶液”、“悬浊液”或“乳浊液”)。(3)、过氧乙酸是一种常用的消毒剂,现要配制500克溶质质量分数为5%的过氧乙酸溶液,需要溶质质量分数为25%的过氧乙酸溶液多少克?需要加水多少克?37. 第十七届西博会“舞动的水滴展”在西湖水面上举行。展览主角五个“大水滴"代表浙江五水共治,呼吁珍惜水资源,热爱自然。
(1)、自来水生产过程中用到了活性炭,利用其性,可以除去水中的色素和异味。(2)、流入过滤池中的混合物属于(填“溶液”、“悬浊液”或“乳浊液”)。(3)、过氧乙酸是一种常用的消毒剂,现要配制500克溶质质量分数为5%的过氧乙酸溶液,需要溶质质量分数为25%的过氧乙酸溶液多少克?需要加水多少克?37. 第十七届西博会“舞动的水滴展”在西湖水面上举行。展览主角五个“大水滴"代表浙江五水共治,呼吁珍惜水资源,热爱自然。 (1)、大水滴漂浮在水面上时,它受到浮力(选填“大于”“等于”小于")它的重力。五水共治的一项重要工作是“保供水”,虽然杭州是江南水乡代表城市之米,但是杭州也缺水。你觉得杭州缺水的原因可能是 (请写出一点)。(2)、”治污水”是五水共治的另一项重要工作。为了防止水体污染,你认为下列措施中可行的是 。A、不任意排放生活污水 B、禁止使用农药和化肥 C、及时拧紧水龙头 D、牲畜粪便适当处理后再施用(3)、水的循环利用是“抓节水”的一个重要举措。下列几个步骤可将河水转化为饮用水:
(1)、大水滴漂浮在水面上时,它受到浮力(选填“大于”“等于”小于")它的重力。五水共治的一项重要工作是“保供水”,虽然杭州是江南水乡代表城市之米,但是杭州也缺水。你觉得杭州缺水的原因可能是 (请写出一点)。(2)、”治污水”是五水共治的另一项重要工作。为了防止水体污染,你认为下列措施中可行的是 。A、不任意排放生活污水 B、禁止使用农药和化肥 C、及时拧紧水龙头 D、牲畜粪便适当处理后再施用(3)、水的循环利用是“抓节水”的一个重要举措。下列几个步骤可将河水转化为饮用水:①化学沉降(用明矾)②消毒杀菌(用漂白粉)③自然沉降④加热煮沸。
以上处理过程最合理的顺序是。
38. 我国有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱,那里的人们冬天捞碱、夏天晒盐。下表是氯化钠、纯碱在不同温度下的溶解度,请结合内容回答下列问题。温度/℃
0
10
20
40
60
80
溶解
度/g
氯化钠
35.7
35.8
36.0
36.6
37.3
38.4
纯碱
7.1
12.5
21.5
38.8
46.0
43.9
(1)、由溶解表可知,氯化钠与纯碱的溶解度恰好相等时的温度范围是_____________A、0℃~10℃ B、10℃~20℃ C、20℃~ 40℃ D、40℃~60℃(2)、长期在液面以外的咸菜表面会出现白色晶体,这晶体的形成与(填“冬天捞碱”或“夏天晒盐”)的原理一致。(3)、生活中纯碱既可用于洗衣又能发面。现要配制纯碱溶液,取48克纯碱溶于100克60℃的水中,所得溶液的溶质质量分数为多少(保留一位小数)?39. 盐场经过长时间日晒会长出形状各异的“盐花”(主要成分为食盐)。盐花属于粗盐,下图是粗盐提纯的部分实验操作。 (1)、一定质量粗盐提纯实验的正确操作顺序为。(填字母)(2)、盐池中食盐的质量分数始终保持在25%左右不再升高,试分析原因。(3)、提纯的精盐可用于一定质量分数食盐溶液的配置。现需要配置质量分数为10%的食盐溶液100克,理论上需要25%的盐池溶液多少克?(写出计算过程)40. 如图所示为有关食盐的两个实验。
(1)、一定质量粗盐提纯实验的正确操作顺序为。(填字母)(2)、盐池中食盐的质量分数始终保持在25%左右不再升高,试分析原因。(3)、提纯的精盐可用于一定质量分数食盐溶液的配置。现需要配置质量分数为10%的食盐溶液100克,理论上需要25%的盐池溶液多少克?(写出计算过程)40. 如图所示为有关食盐的两个实验。 (1)、实验一:粗盐(所含杂质不溶于水)提纯并测定产率实验。
(1)、实验一:粗盐(所含杂质不溶于水)提纯并测定产率实验。a.单一粗盐提纯实验的正确操作顺序为;
b.某同学所测得的产率与其他同学比较明显偏低,下列哪些情况可能会导致产率明显偏低:(选填字母)。
A.溶解时将粗盐一次全部倒入水中,立即过滤
B.过滤时滤纸破损
C.蒸发时有一些液体、固体溅出
D.提纯后的精盐尚未完全干燥就称其质量
(2)、实验二:用提纯得到的精盐配制50克14%的氯化钠溶液a.步骤如下:①计算;②称量和量取;③溶解;④装瓶;
b.经检测,所配制的氯化钠溶液中溶质的质量分数偏小,其原因可能是 ▲ ;
A.量取水读数时俯视B.称量时砝码与药品位置放反
C.盛装溶液的试剂瓶用蒸馏水润洗D.配制结束后,不小心碰洒一部分溶液
c.配制完成的氯化钠溶液B的浓度为8%,质量为40g,请通过计算说明需向溶液B中加入浓度为多少、质量为多少的氯化钠溶液才能配制成溶液 A。(请在溶液 B 的基础上配制,假设加入的氯化钠溶液不饱和)