浙教版科学八上1.5物质的溶解同步练习(2)
试卷更新日期:2022-07-11 类型:同步测试
一、单选题
-
1. 如图所示为蒸发氯化钠溶液的实验过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,作出的判断不正确的是( )
 A、在①→②过程中,氯化钠的质量分数不断增大 B、在②→③过程中,氯化钠的溶解度保持不变 C、在③→④过程中,氯化钠的质量分数不断减小 D、在②→④过程中,氯化钠的质量分数先不变后增大2. 某温度下,在100g溶质质量分数为30%的某物质的饱和溶液中,加入6g该物质和10g水充分搅拌后,所得溶液中溶质的质量分数是( )A、34% B、30% C、31% D、15%3. 某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是( )A、30% B、×100% C、26.5% D、×100%4. 物质的溶解性受很多因素的影响,下列会影响固体物质溶解性的一组是( )
A、在①→②过程中,氯化钠的质量分数不断增大 B、在②→③过程中,氯化钠的溶解度保持不变 C、在③→④过程中,氯化钠的质量分数不断减小 D、在②→④过程中,氯化钠的质量分数先不变后增大2. 某温度下,在100g溶质质量分数为30%的某物质的饱和溶液中,加入6g该物质和10g水充分搅拌后,所得溶液中溶质的质量分数是( )A、34% B、30% C、31% D、15%3. 某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是( )A、30% B、×100% C、26.5% D、×100%4. 物质的溶解性受很多因素的影响,下列会影响固体物质溶解性的一组是( )①溶质的性质 ②溶剂的性质 ③温度 ④压强
A、① B、①② C、①②③ D、①②③④5. 一杯60 ℃、100克不饱和的硝酸钾溶液,逐渐恒温蒸发水时溶液质量的变化如下表所示:由上表可知蒸发水时析出了晶体的是( )实验次数 1 2 3 蒸发水的质量/克 2 2 2 剩余溶液的质量/克 98 96 93 A、第1次 B、第2次 C、第3次 D、都没有晶体析出6. 20℃时,有X、Y、Z三瓶质量相等的硝酸钾饱和溶液,若将X溶液降温到10℃,将Y溶液加热蒸发掉5g水,使之成为高温下的不饱和溶液,从Z的溶液中取出一半,则此时,X、Y、Z三瓶溶液中溶质质量分数的关系是( )A、Y>X>Z B、Y>Z>X C、Z>Y>X D、X>Y>Z7. 如图为甲、乙、丙三种物质的溶解度曲线。下列说法正确的是( ) A、a的溶解度最大,c的溶解度最小 B、t1℃时a、c两种溶液溶质的质量分数相等 C、t2℃时30g物质a加入到50g水中不断搅拌,形成80g溶液 D、升温能使c的不饱和溶液变为饱和溶液8. 科学研究中常用图象来表示两个量(x,y)之间的关系,以使研究的问题变得直观明了。下列两个量之间的关系不符合如图所示的是( )
A、a的溶解度最大,c的溶解度最小 B、t1℃时a、c两种溶液溶质的质量分数相等 C、t2℃时30g物质a加入到50g水中不断搅拌,形成80g溶液 D、升温能使c的不饱和溶液变为饱和溶液8. 科学研究中常用图象来表示两个量(x,y)之间的关系,以使研究的问题变得直观明了。下列两个量之间的关系不符合如图所示的是( ) A、一定浓度溶液中,溶质质量与溶液质量的关系 B、物体受到浮力与排开液体质量的关系 C、固体的溶解度与温度的关系 D、物体受到的浮力与其排开液体体积的关系9. 硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示。则下列说法正确的是( )
A、一定浓度溶液中,溶质质量与溶液质量的关系 B、物体受到浮力与排开液体质量的关系 C、固体的溶解度与温度的关系 D、物体受到的浮力与其排开液体体积的关系9. 硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示。则下列说法正确的是( )温度/℃
10
30
50
70
90
溶解度/g
27.7
39.3
49.0
54.1
51.1
A、硫酸镁的溶解度随温度升高而增大 B、10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 C、70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大 D、50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:10010. 20℃时,四个实验小组分别取不同质量的食盐,逐渐加入到各盛有 50g 水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量溶液的质量。记录数据如下表:实验小组
第一组
第二组
第三组
第四组
水的质量/克
50
50
50
50
食盐的质量/克
15
20
25
30
溶液质量/克
65
68
m
68
下列说法错误的是( )
A、 表格中 m 值为 68 B、0℃时,50 克水中最多可溶 18 克食盐 C、相同温度下,把水的质量增加到 100 克,食盐在水里的溶解度增大 D、用蒸发溶剂结晶的方法可以重新获得溶解了的食盐11. 20℃时,要将硝酸钾不饱和溶液转化为饱和溶液,科学兴趣小组同学分别用两种方法①恒温蒸发水分②降低温度。 实验过程中,硝酸钾溶解度的变化情况分别是( )A、①不变、②不变 B、①变大、②变小 C、①不变、②变小 D、①不变、②变大12. 在温度60℃时,一只盛有不饱和蔗糖水的水槽中放着一只乒乓球,乒乓球处于漂浮状态。而后,温度降低到20℃。其中一定没有发生变化的是( )A、乒乓球所受到的浮力 B、乒乓球露出液面的体积 C、蔗糖的溶解度 D、溶液中溶质质量分数13. 科学拓展课上,小明自制了一个“天气瓶”,他在一个封闭玻璃瓶内放入一定量溶有樟脑的乙醇(已知樟脑在乙醇中的溶解度随温度的升高而增大)。如图为该“天气瓶”在三种不同气温下的状况,下列说法正确的是( ) A、三种状况下的溶液都已达到饱和 B、三种状况下溶液中的溶质质量都相等 C、三种状况下的溶质质量分数都相等 D、三种状况下显示气温最低的是丙14. 某同学在20 ℃(已知硝酸钾—KNO3的溶解度:20 ℃时为31.6克,50 ℃时为85.5克)时进行了如下实验,得到相应的溶液①~⑤,下列说法正确的是( )
A、三种状况下的溶液都已达到饱和 B、三种状况下溶液中的溶质质量都相等 C、三种状况下的溶质质量分数都相等 D、三种状况下显示气温最低的是丙14. 某同学在20 ℃(已知硝酸钾—KNO3的溶解度:20 ℃时为31.6克,50 ℃时为85.5克)时进行了如下实验,得到相应的溶液①~⑤,下列说法正确的是( ) A、保持温度不变,若在④中加入5.5克硝酸钾固体可得到饱和溶液 B、②③⑤中溶质的质量分数相等 C、①③④均为饱和溶液 D、④→⑤可析出53.9克硝酸钾晶体15. t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法错误的是( )
A、保持温度不变,若在④中加入5.5克硝酸钾固体可得到饱和溶液 B、②③⑤中溶质的质量分数相等 C、①③④均为饱和溶液 D、④→⑤可析出53.9克硝酸钾晶体15. t℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量之间的关系如图所示。下列说法错误的是( )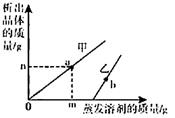 A、蒸发溶剂前甲是饱和溶液 B、b点对应的乙溶液是饱和溶液 C、t℃时,乙的溶解度更大 D、a点时,甲溶液的质量分数为16. 下表是由不同温度时硝酸钾的溶解度,有关说法正确的是( )
A、蒸发溶剂前甲是饱和溶液 B、b点对应的乙溶液是饱和溶液 C、t℃时,乙的溶解度更大 D、a点时,甲溶液的质量分数为16. 下表是由不同温度时硝酸钾的溶解度,有关说法正确的是( )温度/℃
0
20
40
60
80
100
溶解度/克
13.3
31.6
63.9
110
169
246
A、20℃时,100克水中溶解的硝酸钾越多,溶解度就越大 B、40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克 C、100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多
D、0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小17. 农业上常用饱和食盐水选种。在室温保持不变的情况下,饱和食盐水露置在空气中一段时间后,有少量固体析出。对此过程的描述,下列图像正确的是( )A、 B、
B、 C、
C、 D、
D、 18. 氢氧化钙的溶解度随温度升高而降低。如图是有关澄清石灰水的实验操作及变化情况。下列说法正确的是( )
18. 氢氧化钙的溶解度随温度升高而降低。如图是有关澄清石灰水的实验操作及变化情况。下列说法正确的是( ) A、操作Ⅰ可能是降温 B、操作Ⅰ一定是加溶质 C、①与②的溶质质量一定不相等 D、②与③的溶解度一定相等19. 已知(1)20℃时,溶解度在10克以上的物质称为易溶物质,溶解度在1-10克的物质为可溶物质,溶解度在0.01-1克为微溶物质,溶解度小于0.01克的物质为难溶物质。
A、操作Ⅰ可能是降温 B、操作Ⅰ一定是加溶质 C、①与②的溶质质量一定不相等 D、②与③的溶解度一定相等19. 已知(1)20℃时,溶解度在10克以上的物质称为易溶物质,溶解度在1-10克的物质为可溶物质,溶解度在0.01-1克为微溶物质,溶解度小于0.01克的物质为难溶物质。
(2)20℃时几种物质的溶解度如表:
下列说法正确的是( )物质名称 氯化钠 氢氧化钙 氯酸钾 硝酸钾 溶解度(克) 36.0 0.165 7.4 31.6 A、20℃时氯酸钾是易溶物质 B、20℃时氢氧化钙是难溶物质 C、20℃时的氯化钠溶解度比硝酸钾大 D、20℃时硝酸钾饱和溶液的溶质质量分数为31.6%20. 20℃时,10克水中最多可溶解5克A物质,50℃时,15克B物质溶于50克水中恰好饱和,A与B的溶解度( )A、 A=B B、A<B C、A>B D、无法比较二、填空题
-
21. 下表是甲物质在不同温度时溶解度按下图步骤进行操作:
温度/℃
10
20
30
40
溶解度/g
10.0
18.0
36.0
56.0
 (1)、在A一E的溶液中,溶质质量分数最大的是(填字母)。(2)、要使E中未溶的甲物质全部溶解,至少需要加入30℃的水克。22. A、B是不含结晶水的两种固体物质,溶解度表格如下,请回答下列问题
(1)、在A一E的溶液中,溶质质量分数最大的是(填字母)。(2)、要使E中未溶的甲物质全部溶解,至少需要加入30℃的水克。22. A、B是不含结晶水的两种固体物质,溶解度表格如下,请回答下列问题温度(℃)
0
t1
t2
A物质溶解度(克)
10
15
20
B物质溶解度(克)
20
15
11
(1)、温度为(填“t1℃”或“t2℃”)时,A、B溶解度相等。(2)、t2℃时,A的饱和溶液中溶质A的质量分数为(精确至 0.1%)。(3)、t2℃时,A和B的饱和溶液降温至t1℃。其中有晶体析出的是。23. 配制一定质量的硝酸钾溶液,将一木块漂浮于50℃时的硝酸钾饱和溶液中,当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图变化。 (1)、由此推测出温度的改变是(填“升温”或“降温”)。(2)、同时观察到烧杯底部硝酸钾晶体(填“增多”“不变”或“减少”)。(3)、导致木块浸入液体体积增大的原因是。24. 如图所示,在小试管中加入的浓硫酸,则观察到U型管中的液面(填“a升高b降低”或“a降低b升高”),集中瓶中观察到的现象是。
(1)、由此推测出温度的改变是(填“升温”或“降温”)。(2)、同时观察到烧杯底部硝酸钾晶体(填“增多”“不变”或“减少”)。(3)、导致木块浸入液体体积增大的原因是。24. 如图所示,在小试管中加入的浓硫酸,则观察到U型管中的液面(填“a升高b降低”或“a降低b升高”),集中瓶中观察到的现象是。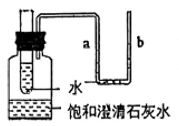 25. 硝酸钾在不同温度时的溶解度如图所示:
25. 硝酸钾在不同温度时的溶解度如图所示:温度(℃)
0
10
20
30
40
50
60
70
硝酸钾
13.3
20.9
31.6
45.8
63.9
85.5
110
138
(1)、从表中可知硝酸钾溶解度与温度的关系为。(2)、30℃时,将50克硝酸钾放在100克水中,充分溶解后所得溶液的质量是。26. 硝酸钾和氯化钾的溶解度曲线如图所示: (1)、t3 ℃时,氯化钾的溶解度为g。(2)、将t3 ℃时硝酸钾的饱和溶液163.9 g稀释成质量分数为20.0%的硝酸钾溶液,需加水g。(3)、现有t3 ℃时硝酸钾的饱和溶液m1 g和氯化钾的饱和溶液m2 g。不考虑水的蒸发,下列说法正确的是 (填字母标号)。A、t3 ℃时硝酸钾的饱和溶液比氯化钾饱和溶液溶质的质量分数大 B、分别降温到t2 ℃,两溶液中溶质的质量分数相等 C、分别降温到t2 ℃,氯化钾饱和溶液析出的溶质更多 D、不同温度下,硝酸钾溶解度可能大于、小于或等于氯化钾的溶解度27. 实验室需配制一定质量分数的硝酸钾溶液(1)、查阅硝酸钾的溶解度。已知20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质的质量分数最大为% (计算结果保留整数)。(2)、称量硝酸钾固体质量。应分别在天平左右两盘放上纸片,调节平衡后, (填字母)。A、先移动游码到所需位置,再添加硝酸钾直到天平平衡 B、先添加所需的硝酸钾,再移动游码直到天平 平衡28. 现有一木块漂浮于 40℃的 KNO3 饱和溶液中,当温度改变时(不考虑由此引起的木块和溶液的体积变化),木块排开液体的体积 V 排随时间 t 发生了如图所示的变化。
(1)、t3 ℃时,氯化钾的溶解度为g。(2)、将t3 ℃时硝酸钾的饱和溶液163.9 g稀释成质量分数为20.0%的硝酸钾溶液,需加水g。(3)、现有t3 ℃时硝酸钾的饱和溶液m1 g和氯化钾的饱和溶液m2 g。不考虑水的蒸发,下列说法正确的是 (填字母标号)。A、t3 ℃时硝酸钾的饱和溶液比氯化钾饱和溶液溶质的质量分数大 B、分别降温到t2 ℃,两溶液中溶质的质量分数相等 C、分别降温到t2 ℃,氯化钾饱和溶液析出的溶质更多 D、不同温度下,硝酸钾溶解度可能大于、小于或等于氯化钾的溶解度27. 实验室需配制一定质量分数的硝酸钾溶液(1)、查阅硝酸钾的溶解度。已知20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质的质量分数最大为% (计算结果保留整数)。(2)、称量硝酸钾固体质量。应分别在天平左右两盘放上纸片,调节平衡后, (填字母)。A、先移动游码到所需位置,再添加硝酸钾直到天平平衡 B、先添加所需的硝酸钾,再移动游码直到天平 平衡28. 现有一木块漂浮于 40℃的 KNO3 饱和溶液中,当温度改变时(不考虑由此引起的木块和溶液的体积变化),木块排开液体的体积 V 排随时间 t 发生了如图所示的变化。 (1)、由此推断出温度的改变方式是(填“升 温”或“降温”)。(2)、在温度改变的过程中,如右上图中 A、B 两点对应的木块受到的浮力大小关系为FAFB(填“>、”“<”或“=”)。29. 生活中处处有科学,请填写以下的科学知识:(1)、夏季雷雨前鱼会纷纷游到水面上来,这是因为气压了,使得氧气在水中的溶解度下降。(选填“升高”或“降低”)。(2)、用冰来冷却海鲜食品或用来保鲜时,通常冰块应放在食品的(选填“上部”或“下部”)。(3)、衣服上有油脂等脏物时,用水洗是洗不掉的,这是因为油脂在水中的能力比较弱。(4)、烹煮牛肉汤时,为了解汤的咸味是否适宜,取锅中少量汤品尝即可,这是因为溶液具有性。30. 如图是a、b、c三种物质的溶解度曲线,请据图回答:
(1)、由此推断出温度的改变方式是(填“升 温”或“降温”)。(2)、在温度改变的过程中,如右上图中 A、B 两点对应的木块受到的浮力大小关系为FAFB(填“>、”“<”或“=”)。29. 生活中处处有科学,请填写以下的科学知识:(1)、夏季雷雨前鱼会纷纷游到水面上来,这是因为气压了,使得氧气在水中的溶解度下降。(选填“升高”或“降低”)。(2)、用冰来冷却海鲜食品或用来保鲜时,通常冰块应放在食品的(选填“上部”或“下部”)。(3)、衣服上有油脂等脏物时,用水洗是洗不掉的,这是因为油脂在水中的能力比较弱。(4)、烹煮牛肉汤时,为了解汤的咸味是否适宜,取锅中少量汤品尝即可,这是因为溶液具有性。30. 如图是a、b、c三种物质的溶解度曲线,请据图回答: (1)、t2℃时,将50克a物质加入到50克水中并充分搅拌,形成溶液的质量为g;(2)、P点的含义是。(3)、将t2℃时a、b、c三种物质的饱和溶液降低温度到t1℃时,这三种溶液中溶质质量分数的大小由大到小顺序是 (填序号)。
(1)、t2℃时,将50克a物质加入到50克水中并充分搅拌,形成溶液的质量为g;(2)、P点的含义是。(3)、将t2℃时a、b、c三种物质的饱和溶液降低温度到t1℃时,这三种溶液中溶质质量分数的大小由大到小顺序是 (填序号)。三、实验探究题
-
31. 配制一定溶质质量分数的氯化钠溶液是初中化学的基础实验之一。请回答下列问题:(1)、现欲配制一瓶75g溶质质量分数为10%的氯化钠溶液,请用图中的序号表示配制溶液的正确操作顺序。
 (2)、认真观察,图中某步骤错误,若不进行改正,其他操作步骤正确,则所配制溶液的溶质的质量分数(填“大于”、“小于”或“等于”)10%。(3)、实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,问需要15%的氯化钠溶液克才可配得120克5%的氯化钠溶液。(4)、t℃时某氯化钠溶液400克,在温度不变的情况下,第一次蒸发20克水,析出晶体4克;第二次又蒸发20克水,析出晶体6克。则t℃时硝酸钠的溶解度为克。32. 小红在学习了物质的溶解这一专题后,对“气体在液体中溶解能力的强弱与气压的关系”进行了研究。小红用20 mL一次性注射器吸取10 mL某碳酸饮料(饮料中溶解有二氧化碳气体),并用胶头封闭注射器针孔,进行了如图所示的实验。
(2)、认真观察,图中某步骤错误,若不进行改正,其他操作步骤正确,则所配制溶液的溶质的质量分数(填“大于”、“小于”或“等于”)10%。(3)、实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,问需要15%的氯化钠溶液克才可配得120克5%的氯化钠溶液。(4)、t℃时某氯化钠溶液400克,在温度不变的情况下,第一次蒸发20克水,析出晶体4克;第二次又蒸发20克水,析出晶体6克。则t℃时硝酸钠的溶解度为克。32. 小红在学习了物质的溶解这一专题后,对“气体在液体中溶解能力的强弱与气压的关系”进行了研究。小红用20 mL一次性注射器吸取10 mL某碳酸饮料(饮料中溶解有二氧化碳气体),并用胶头封闭注射器针孔,进行了如图所示的实验。 (1)、图中,小红向外拉注射器,根据生活经验小红可以观察到什么现象?。(2)、该实验装置的优点是。(3)、气体的溶解度还受温度等因素的影响,请解释“一些工厂向河里排放热水,会造成河里的鱼因缺氧而死亡”的原因:。33. R是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组的同学进行了如图2所示实验。
(1)、图中,小红向外拉注射器,根据生活经验小红可以观察到什么现象?。(2)、该实验装置的优点是。(3)、气体的溶解度还受温度等因素的影响,请解释“一些工厂向河里排放热水,会造成河里的鱼因缺氧而死亡”的原因:。33. R是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组的同学进行了如图2所示实验。 (1)、t2℃时,硝酸钾的溶解度为g。(2)、现需要使用①的溶液配制200克10% 的R的稀溶液,需要g①的溶液。(3)、根据以上信息可推出R是(写名称)。(4)、关于图2中烧杯内的物质,以下几种说法正确的有。
(1)、t2℃时,硝酸钾的溶解度为g。(2)、现需要使用①的溶液配制200克10% 的R的稀溶液,需要g①的溶液。(3)、根据以上信息可推出R是(写名称)。(4)、关于图2中烧杯内的物质,以下几种说法正确的有。A.①和②的溶液中,溶质质量相等
B.若使③中的固体溶解,可采用加水或升温的方法
C.①、②、③中,只有③中上层清液是饱和溶液
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
34. 在实验室,小阳分别用甲盐的晶体配制了溶质质量分数为5%的A溶液和30%的B溶液,但忘了贴标签。请你运用所学的科学原理,设计一个简单的实验来判别这两瓶溶液。请写出简要的实验方案和明确的判别依据。有下列仪器、物品供选择:量筒、天平、小烧杯、酒精灯、三角架、石棉网、漏斗、玻璃棒、滤纸、温度计、甲盐的晶体。(实验室的温度为30℃,30℃甲盐的溶解度为50g)方案: ▲ 。
判别依据: ▲ 。
35. 烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。溶液的温度/℃
75
65
50
35
20
析出固体M的质量/g
0
0
2.0
4.5
8.4
若不考虑水蒸发对实验的影响.请回答下列问题。
(1)、65℃时,该溶液是否为饱和溶液?(填“是”、“否”或“无法判断”);(2)、分析表格可知,M溶解度和温度的关系是;(3)、将40℃时接近饱和的M溶液变成饱和溶液.下列方法中一定能达到目的的有(填序号)。①升温;②降温;③加溶质M;④加水;⑤加另一种固体N;⑥恒温蒸发水;⑦与40℃时M的饱和溶液混合
(4)、20℃时,用固体粉末M和水配制100g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码盒)、烧杯、药匙、量筒(100 mL)、玻璃棒、。四、解答题
-
36. 图1为甲、乙(均不含结晶水)两种固体物质在水中的溶解度曲线。
 (1)、t1℃时,甲的溶解度 乙的溶解度(填“大于”或“小于”或“等于”)。(2)、t2℃时,100g水中溶解 g乙物质恰好达到饱和。(3)、某同学在t1℃时开始如图2实验,得到相应的溶液A、B、C。在溶液A、B、C中,属于饱和溶液的是 ;在溶液C中再加入25g甲后,充分搅拌,恢复到t1℃,所得溶液的质量为 。37. 工业上常用碳酸镁矿石(主要成分是难溶于水的碳酸镁.杂质不溶于水也不与酸反应)与稀硫酸反应来制备硫酸镁。硫酸镁在不同温度时的溶解度如表所示。制备流程如图。
(1)、t1℃时,甲的溶解度 乙的溶解度(填“大于”或“小于”或“等于”)。(2)、t2℃时,100g水中溶解 g乙物质恰好达到饱和。(3)、某同学在t1℃时开始如图2实验,得到相应的溶液A、B、C。在溶液A、B、C中,属于饱和溶液的是 ;在溶液C中再加入25g甲后,充分搅拌,恢复到t1℃,所得溶液的质量为 。37. 工业上常用碳酸镁矿石(主要成分是难溶于水的碳酸镁.杂质不溶于水也不与酸反应)与稀硫酸反应来制备硫酸镁。硫酸镁在不同温度时的溶解度如表所示。制备流程如图。温度(℃)
60
80
90
100
硫酸镁溶解度(克)
54.6
55.8
52.9
50.4
 (1)、用150千克溶质质量分数为98%的浓硫酸配制9.8%的稀硫酸,需要水千克。(2)、小煦将除去杂质后的滤液加热至90℃,得到硫酸镁浓溶液,继续加热,观察到晶体快速析出。其原因可能是 。38. 你见过冬天能自发热,夏天能自制冷的罐装饮料吗,如图是“玛吉克牌”一摇冰功能饮料,根据所给资料回答:
(1)、用150千克溶质质量分数为98%的浓硫酸配制9.8%的稀硫酸,需要水千克。(2)、小煦将除去杂质后的滤液加热至90℃,得到硫酸镁浓溶液,继续加热,观察到晶体快速析出。其原因可能是 。38. 你见过冬天能自发热,夏天能自制冷的罐装饮料吗,如图是“玛吉克牌”一摇冰功能饮料,根据所给资料回答: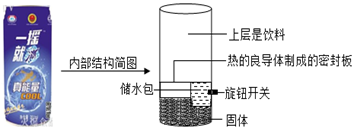 (1)、“一摇冰”饮料在炎热的夏天解渴,其罐底的固体可能是 。A、氢氧化钠 B、硝酸铵 C、氯化钠(2)、我们在喝碳酸饮料(含有二氧化碳气体)后,常出现打嗝现象,是由于气体的溶解度随温度升高而。(3)、已知罐体底部水溶液的溶质质量分数为60%,若要将100克该溶液稀释为20%的稀溶液,则需加水多少克?39. 某工厂在装配一件设备时,不小心把一个精密空心小球掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来。已知该小球的密度为1.6g/cm3 , 有人提出往小洞中倒入某种溶液使小球浮起。现有两种物质的溶解度数据(注:溶液体积可认为近似等于水的体积):
(1)、“一摇冰”饮料在炎热的夏天解渴,其罐底的固体可能是 。A、氢氧化钠 B、硝酸铵 C、氯化钠(2)、我们在喝碳酸饮料(含有二氧化碳气体)后,常出现打嗝现象,是由于气体的溶解度随温度升高而。(3)、已知罐体底部水溶液的溶质质量分数为60%,若要将100克该溶液稀释为20%的稀溶液,则需加水多少克?39. 某工厂在装配一件设备时,不小心把一个精密空心小球掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来。已知该小球的密度为1.6g/cm3 , 有人提出往小洞中倒入某种溶液使小球浮起。现有两种物质的溶解度数据(注:溶液体积可认为近似等于水的体积):物质溶解度/g
20℃
40℃
60℃
80℃
100℃
硝酸钾
31.6
64.0
110.0
169.0
246.0
氯化钾
34.0
40.0
45.0
51.1
56.7
(1)、理论上可用上表中物质配制成溶液倒入小洞中使小球浮起。(2)、配制的溶液温度至少应保持℃以上。在以上计算所得的最低温度时,该饱和溶液溶质的质量分数是。(精确到0.1%)(3)、小球取出后,擦干,用天平称得其质量为8.0g。若把此球投入水中,则静止时所受浮力为多大?40. 下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。温度/℃
0
10
20
30
40
溶解度/克
13.3
20.9
31.6
45.8
63.9
 (1)、10℃时,100克水中最多可溶解硝酸钾的质量为克。(2)、20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为。(3)、如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
(1)、10℃时,100克水中最多可溶解硝酸钾的质量为克。(2)、20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为。(3)、如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)五、综合说理题
-
41. 一木块漂浮于30℃的硝酸钾饱和溶液中,当温度改变时(不考虑由此引起的木块和溶液体积的变化),请描述可能发生的现象并解释原因。
