上海市黄埔区2022届高三下学期二模化学试题
试卷更新日期:2022-07-08 类型:高考模拟
一、单选题
-
1. 对抗疫情离不开化学。下列抗疫物资中,主要成分属于无机物的是( )A、医用酒精
 B、塑料护目镜
B、塑料护目镜 C、漂粉精
C、漂粉精 D、医用橡胶手套
D、医用橡胶手套 2. 下列物质中,其主要成分不属于烃的是( )A、汽油 B、甘油 C、煤油 D、柴油3. 下列物质中既含有氯离子又含有氯分子的是( )A、氯水 B、液氯 C、次氯酸 D、氯化钠4. 已知某水稻田的土壤带负电,使用含氮量相同的下列化肥时,肥效最差的是( )A、 B、 C、 D、(尿素)5. 用下图装置吸收中学常见的某种气体,上层溶液变红。有关该气体的描述错误的是( )
2. 下列物质中,其主要成分不属于烃的是( )A、汽油 B、甘油 C、煤油 D、柴油3. 下列物质中既含有氯离子又含有氯分子的是( )A、氯水 B、液氯 C、次氯酸 D、氯化钠4. 已知某水稻田的土壤带负电,使用含氮量相同的下列化肥时,肥效最差的是( )A、 B、 C、 D、(尿素)5. 用下图装置吸收中学常见的某种气体,上层溶液变红。有关该气体的描述错误的是( ) A、具有刺激性气味 B、可用作制冷剂 C、属于碱 D、含有极性键6. 在实验室采用如图装置制备气体,合理的是( )
A、具有刺激性气味 B、可用作制冷剂 C、属于碱 D、含有极性键6. 在实验室采用如图装置制备气体,合理的是( )化学试剂
制备的气体
装置
A
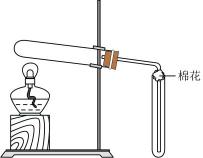
B
C
D
A、A B、B C、C D、D7. 中科院科学家发现,在水滑石表面可发生:。关于该过程的说法正确的是( )A、属于固氮过程 B、化学能一部分转化成了热能 C、反应物的总能量高于生成物的总能量 D、证明氮的非金属性大于氧8. 四氯乙烯是一种衣物干洗剂,以下不是它的性质( )A、易挥发 B、所有原子共平面 C、易溶于水 D、能发生加成反应9. 医疗上用作 X 射线透视肠胃的内服药“钡餐”的物质是( )A、BaCO3 B、Ba(OH)2 C、BaCl2 D、BaSO410. 2022年北京冬奥会火炬“飞扬”用氢气为燃料,耐高温碳纤维材料为外壳,铝合金为点火段材料,辅以可调节火焰颜色的“配方”。下列说法错误的是( ) A、氢气作燃料对环境友好无污染 B、碳纤维不属于有机材料 C、铝合金密度小、易燃 D、含钠元素的“配方”可使火焰呈黄色11. 室温下,1体积的水能溶解约40体积的SO2。用试管收集SO2后进行如下实验。对实验现象的分析正确的是( )
A、氢气作燃料对环境友好无污染 B、碳纤维不属于有机材料 C、铝合金密度小、易燃 D、含钠元素的“配方”可使火焰呈黄色11. 室温下,1体积的水能溶解约40体积的SO2。用试管收集SO2后进行如下实验。对实验现象的分析正确的是( )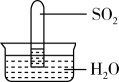 A、试管内液面上升,证明SO2与水发生了反应 B、试管中剩余少量气体,是因为SO2的溶解已达饱和 C、取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO2+H2O⇌H2SO3、H2SO3⇌H++、⇌H++ D、取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO2挥发12. 用已知浓度的溶液测定浓硫酸试剂中含量的主要操作中,不需要用到的仪器为( )A、
A、试管内液面上升,证明SO2与水发生了反应 B、试管中剩余少量气体,是因为SO2的溶解已达饱和 C、取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO2+H2O⇌H2SO3、H2SO3⇌H++、⇌H++ D、取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO2挥发12. 用已知浓度的溶液测定浓硫酸试剂中含量的主要操作中,不需要用到的仪器为( )A、 B、
B、 C、
C、 D、
D、 13. 下列溶液一定呈中性的是( )A、的溶液 B、等物质的量的强酸和强碱反应得到的溶液 C、c(H+)=c(OH-)的溶液 D、紫色石蕊试液不变色的溶液14. 84消毒液(含)与洁厕灵(含浓盐酸)不能混用,会发生反应产生有毒的气体,该反应中( )A、为还原剂 B、仅体现酸性 C、既是氧化产物也是还原产物 D、是还原产物15. 下列过程吸收热量的是( )A、大理石受热分解 B、食物腐败 C、铝热反应 D、浓硫酸稀释16. 用洗涤剂洗涤容器内附着的物质,合理的是( )
13. 下列溶液一定呈中性的是( )A、的溶液 B、等物质的量的强酸和强碱反应得到的溶液 C、c(H+)=c(OH-)的溶液 D、紫色石蕊试液不变色的溶液14. 84消毒液(含)与洁厕灵(含浓盐酸)不能混用,会发生反应产生有毒的气体,该反应中( )A、为还原剂 B、仅体现酸性 C、既是氧化产物也是还原产物 D、是还原产物15. 下列过程吸收热量的是( )A、大理石受热分解 B、食物腐败 C、铝热反应 D、浓硫酸稀释16. 用洗涤剂洗涤容器内附着的物质,合理的是( )A
B
C
D
附着物质
银镜
石蜡
食盐
硫磺
洗涤剂
氨水
蒸馏水
酒精
二硫化碳
A、A B、B C、C D、D17. 利用如图装置进行实验(U形管为耐压试管),开始时,a、b两处液面相平,密封好,放置一段时间。下列说法错误的是( ) A、铁丝的腐蚀速率: B、一段时间后,a管液面高于b管液面 C、a管溶液的增大,b管溶液的减小 D、a、b两管中发生相同的电极反应为18. 工业制硫酸的适宜条件不包括( )A、矿石粉碎成粉末可加快反应速率 B、原料气进入转化器之前需净化处理 C、SO2转化为SO3时用铁触媒作催化剂 D、用98.3%的浓硫酸吸收SO319. 为检验某久置过氧化钠样品的成分,学习小组依次进行了有关实验。实验中涉及反应的离子方程式正确的是( )A、将过氧化钠样品完全溶于水,产生气泡:Na2O2+H2O=2Na++2OH-+O2↑ B、向溶液中滴加BaCl2溶液,产生白色沉淀:CO+Ba2+=BaCO3↓ C、向沉淀中滴加稀醋酸,产生气体:BaCO3+2H+=Ba2++CO2↑+H2O D、将气体通入足量澄清石灰水,出现浑浊现象:CO2+Ca2++OH-=CaCO3↓+H2O20. 常温下,用如图1所示装置,分别向溶液和溶液中逐滴滴加的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是( )
A、铁丝的腐蚀速率: B、一段时间后,a管液面高于b管液面 C、a管溶液的增大,b管溶液的减小 D、a、b两管中发生相同的电极反应为18. 工业制硫酸的适宜条件不包括( )A、矿石粉碎成粉末可加快反应速率 B、原料气进入转化器之前需净化处理 C、SO2转化为SO3时用铁触媒作催化剂 D、用98.3%的浓硫酸吸收SO319. 为检验某久置过氧化钠样品的成分,学习小组依次进行了有关实验。实验中涉及反应的离子方程式正确的是( )A、将过氧化钠样品完全溶于水,产生气泡:Na2O2+H2O=2Na++2OH-+O2↑ B、向溶液中滴加BaCl2溶液,产生白色沉淀:CO+Ba2+=BaCO3↓ C、向沉淀中滴加稀醋酸,产生气体:BaCO3+2H+=Ba2++CO2↑+H2O D、将气体通入足量澄清石灰水,出现浑浊现象:CO2+Ca2++OH-=CaCO3↓+H2O20. 常温下,用如图1所示装置,分别向溶液和溶液中逐滴滴加的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是( ) A、X曲线为溶液的滴定曲线 B、b点溶液的pH大于c点溶液的pH C、c点的溶液中: D、a、d两点水的电离程度:a>d
A、X曲线为溶液的滴定曲线 B、b点溶液的pH大于c点溶液的pH C、c点的溶液中: D、a、d两点水的电离程度:a>d二、非选择题
-
21. 氮化镓是智能手机的快速充电器中使用的一种半导体材料,可通过单质与氨气在高温下反应可制得。镓在周期表中的位置如图。
Al
P
Ga
As
(1)、配平反应:;其中氧化剂的电子式。(2)、N原子的电子排布式为。Ga原子核外未成对电子数为个。(3)、氢化物的热稳定性:(填“>”、“<”或“=”)。(4)、Ga分别与N、P、形成化合物的晶体结构与金刚石相似,其熔点如下表所示:
晶体中含有的化学键类型为。从结构的角度分析、推测的熔点范围 , 理由是。物质
熔点/℃
1700
x
1238
22. 在温度保持不变的情况下,将一定量的充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小且整个操作过程物质均为气态)。(已知:) (1)、对注射器的移动轨迹判断正确的是____。A、 B、 C、 D、(2)、判断下面的说法是否符合题意?(在□中画“×”或“√”)
(1)、对注射器的移动轨迹判断正确的是____。A、 B、 C、 D、(2)、判断下面的说法是否符合题意?(在□中画“×”或“√”)A.d点:
B.c点与a点相比,增大,减小
C.若注射器隔热,没有能量损失,会导致反应温度发生变化,则b、c两点的平衡常数
D.若在注射器中对反应进行完全相同的操作,最后能得到相似的透光率变化趋势图像
在100℃时,将的气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表数据。
时间/s
0
20
40
60
80
100
0.40
0.26
0.00
0.05
0.08
0.08
0.08
(3)、比较、的大小。(4)、20~40s内,的平均反应速率为。(5)、100℃时,容器中物质的量的变化曲线如图。其他条件不变,请画出80℃时物质的量的变化曲线。 23. 以芳香族化合物A和有机物D为原料,制备有机物M和高聚物N的合成路线如图:
23. 以芳香族化合物A和有机物D为原料,制备有机物M和高聚物N的合成路线如图: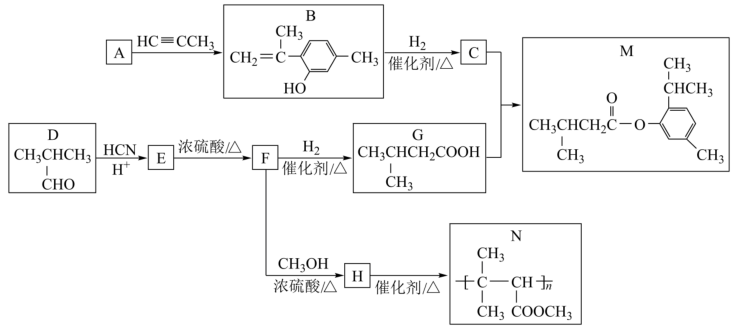
已知:I.符合原子经济学原理
II.

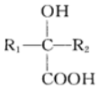 (R1、R2表示氢原子或烃基)(1)、D的官能团名称。(2)、的反应类型 , 生成M的反应条件。(3)、E的结构简式为。(4)、H生成N的化学方程式为。(5)、写出满足下列条件的B的一种同分异构体的结构简式。
(R1、R2表示氢原子或烃基)(1)、D的官能团名称。(2)、的反应类型 , 生成M的反应条件。(3)、E的结构简式为。(4)、H生成N的化学方程式为。(5)、写出满足下列条件的B的一种同分异构体的结构简式。①能发生银镜反应 ②苯环上连有三个取代基 ③苯环上的一卤代物有两种
(6)、参照上述合成路线和信息,以丙烯为原料(无机试剂任选),设计制备 的合成路线。 24. 利用氯碱工业中的固体废物盐泥[主要成分为、、 , 还含有少量、、、等]与废酸反应制备 , 既处理了三废,又有经济效益。其主要流程如下:
的合成路线。 24. 利用氯碱工业中的固体废物盐泥[主要成分为、、 , 还含有少量、、、等]与废酸反应制备 , 既处理了三废,又有经济效益。其主要流程如下:
已知:
①部分离子沉淀完全的
沉淀物
8.96
3.20
4.70
11.12
②三种化合物的溶解度(S)随温度变化的曲线
 (1)、 实验室模拟该流程,不会涉及的操作____。A、
(1)、 实验室模拟该流程,不会涉及的操作____。A、 B、
B、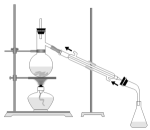 C、
C、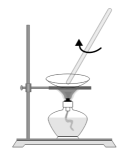 D、
D、
加入可调节 , 且一种离子会被氧化。充分反应后再趁热过滤。
(2)、以上操作利用了的性和性,且不引入新的杂质离子;趁热过滤的目的是;沉淀A的主要成分是、、。(3)、检验滤液B中是否含有的实验方法。(4)、从沉淀B中获得晶体的实验步骤依次为①向沉淀B中加入足量(填化学式);②、;④过滤、洗涤得产品。(5)、若测定晶体中结晶水的含量,需要的定量仪器有。