广东省名校2021-2022学年高三下学期3月开学测试化学试题
试卷更新日期:2022-07-04 类型:开学考试
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11-16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1. 中国年中国味。下列新春文化的主要材料不属于天然有机高分子的是( )A、皮影戏-驴皮皮影
 B、内画-水晶瓶
B、内画-水晶瓶  C、年画-木刻板
C、年画-木刻板  D、窗花-纸花
D、窗花-纸花  2. 化学与生产、生活、科技、环境等关系密切。下列说法错误的是( )A、汽车尾气催化转化器可有效减少CO2的排放,实现“碳中和” B、春雨如雾,雾是一种气溶胶,光束透过大雾可观察到丁达尔效应 C、稀土永磁材料是电子技术通讯中的重要材料,稀土元素均为金属元素 D、“深海勇士”号潜水艇使用的锂离子电池是一种二次电池3. 实验室通过制氯气来获得漂白液,下列装置(夹持装置略)中不必使用的是( )A、
2. 化学与生产、生活、科技、环境等关系密切。下列说法错误的是( )A、汽车尾气催化转化器可有效减少CO2的排放,实现“碳中和” B、春雨如雾,雾是一种气溶胶,光束透过大雾可观察到丁达尔效应 C、稀土永磁材料是电子技术通讯中的重要材料,稀土元素均为金属元素 D、“深海勇士”号潜水艇使用的锂离子电池是一种二次电池3. 实验室通过制氯气来获得漂白液,下列装置(夹持装置略)中不必使用的是( )A、 B、
B、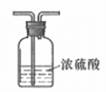 C、
C、 D、
D、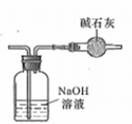 4. NA为阿伏加德罗常数的值。下列叙述正确的是( )A、pH=1的HCl溶液中,含HCl分子的数目为NA B、0.3mol的NO2与足量的H2O完全反应时产生2.24LNO气体 C、6.4g环状S8(
4. NA为阿伏加德罗常数的值。下列叙述正确的是( )A、pH=1的HCl溶液中,含HCl分子的数目为NA B、0.3mol的NO2与足量的H2O完全反应时产生2.24LNO气体 C、6.4g环状S8(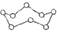 )分子中含有的S—S键数为0.2 NA
D、1LpH=4的0.1mol·L-1K2Cr2O7溶液中所含Cr2O72-数为0.1 NA
5. 能源和环境是人类关注的两大热点。下列说法正确的是( )A、发展火电有利于尽早实现“碳中和、碳达峰”目标 B、南水北调可以优化水资源配置和促进区域协调发展 C、普及氢能、生物质能等二次能源有利于改善环境 D、石油裂解的主要目的是提高汽油的产量6. 一种天然产物具有抗肿瘤、镇痉等生物活性,其结构筒式如下图。下列关于该天然产物
)分子中含有的S—S键数为0.2 NA
D、1LpH=4的0.1mol·L-1K2Cr2O7溶液中所含Cr2O72-数为0.1 NA
5. 能源和环境是人类关注的两大热点。下列说法正确的是( )A、发展火电有利于尽早实现“碳中和、碳达峰”目标 B、南水北调可以优化水资源配置和促进区域协调发展 C、普及氢能、生物质能等二次能源有利于改善环境 D、石油裂解的主要目的是提高汽油的产量6. 一种天然产物具有抗肿瘤、镇痉等生物活性,其结构筒式如下图。下列关于该天然产物的说法正确的是( )
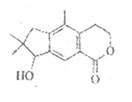 A、分子中的所有碳原子可能共平面 B、1mol该物质水解最多消耗1mol NaOH C、与Cl2发生取代反应生成的一氯代物有9种 D、既能与溴水反应,又能使酸性KMnO4溶液褪色7. 中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理如右图所示。下列说法不正确的是( )
A、分子中的所有碳原子可能共平面 B、1mol该物质水解最多消耗1mol NaOH C、与Cl2发生取代反应生成的一氯代物有9种 D、既能与溴水反应,又能使酸性KMnO4溶液褪色7. 中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理如右图所示。下列说法不正确的是( )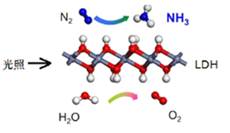 A、上述合成氨的过程属于氮的固定 B、该过程中,LDH降低了反应的活化能 C、该过程有极性键、非极性键的断裂和生成 D、高温高压的条件有利于提高氨的产率8. 下列实验对应的反应方程式书写正确的是( )A、吸有NO2的注射器,堵住针头增大容积红棕色先变浅后变深:2NO2(g) N2O4(g) B、用白醋除水垢:CaCO3+2H+=CO2↑+ H2O + Ca2+ C、电解MgCl2溶液制镁:2Cl-+Mg2+ Mg + Cl2↑ D、Al2(SO4)溶液中加入足量Ba(OH)2溶液
A、上述合成氨的过程属于氮的固定 B、该过程中,LDH降低了反应的活化能 C、该过程有极性键、非极性键的断裂和生成 D、高温高压的条件有利于提高氨的产率8. 下列实验对应的反应方程式书写正确的是( )A、吸有NO2的注射器,堵住针头增大容积红棕色先变浅后变深:2NO2(g) N2O4(g) B、用白醋除水垢:CaCO3+2H+=CO2↑+ H2O + Ca2+ C、电解MgCl2溶液制镁:2Cl-+Mg2+ Mg + Cl2↑ D、Al2(SO4)溶液中加入足量Ba(OH)2溶液Al3++ SO42-+ Ba2-+ 3OH-=Al(OH)3↓+BaSO4↓
9. 近日,武汉大学肖巍教授研究了一种电化学分解甲烷源( ESM)的方法,实现了以节能、无排放和无水的方式生产氢气,反应机理如下图所示。下列说法正确的是( ) A、Ni电极连接电源的负极 B、反应过程中,需要不断补充CO C、理论上每生产11.2 L H2 , 电路中转移2 mol e - D、Ni—YSZ电极的电极反应为CH4 + 2O 2- = CO2 + 2H210. 下列“类比”或“对比”不合理的是( )A、Mg在CO2中点燃反应生成MgO和C,则Ca在CO2中点燃反应生成CaO和C B、NaClO溶液与CO2反应生成NaHCO3和HClO,而Ca(ClO)2溶液与少量CO2反应生成CaCO3和HClO C、Na3N与盐酸反应生成NaCl和NH4Cl,则Mg3N2与盐酸反应生成MgCl2和NH4Cl D、NaOH溶液与少量AgNO3溶液反应生成Ag2O和NaNO3 , 则氨水与少量AgNO3溶液反应最终生成Ag2O和NH4NO311. 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大Z原子最外层电子数是电子层数的3倍。下列说法正确的是( )
A、Ni电极连接电源的负极 B、反应过程中,需要不断补充CO C、理论上每生产11.2 L H2 , 电路中转移2 mol e - D、Ni—YSZ电极的电极反应为CH4 + 2O 2- = CO2 + 2H210. 下列“类比”或“对比”不合理的是( )A、Mg在CO2中点燃反应生成MgO和C,则Ca在CO2中点燃反应生成CaO和C B、NaClO溶液与CO2反应生成NaHCO3和HClO,而Ca(ClO)2溶液与少量CO2反应生成CaCO3和HClO C、Na3N与盐酸反应生成NaCl和NH4Cl,则Mg3N2与盐酸反应生成MgCl2和NH4Cl D、NaOH溶液与少量AgNO3溶液反应生成Ag2O和NaNO3 , 则氨水与少量AgNO3溶液反应最终生成Ag2O和NH4NO311. 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大Z原子最外层电子数是电子层数的3倍。下列说法正确的是( ) A、Z的氢化物只含极性键 B、原子半径:M>W>X>Y>Z C、Z的氢化物沸点一定比X的氢化物的沸点高 D、已知H3WO3的电离反应:H3WO3+H2O H++W(OH)4- , Ka=5.81× 10-10 , 可判断H3WO3是一元弱酸12. 下列化学用语使用正确的是( )A、SiO2的结构式:O-Si=O B、H2O2的电子式:
A、Z的氢化物只含极性键 B、原子半径:M>W>X>Y>Z C、Z的氢化物沸点一定比X的氢化物的沸点高 D、已知H3WO3的电离反应:H3WO3+H2O H++W(OH)4- , Ka=5.81× 10-10 , 可判断H3WO3是一元弱酸12. 下列化学用语使用正确的是( )A、SiO2的结构式:O-Si=O B、H2O2的电子式: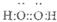 C、BaSO4的电离方程式:BaSO4=SO42-+ Ba2+
D、12C与14C互为同素异形体
13. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
C、BaSO4的电离方程式:BaSO4=SO42-+ Ba2+
D、12C与14C互为同素异形体
13. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )粒子组
判断和分析
A
Na+、Al3+、Cl-、NH3·H2O
不能大量共存,因发生反应:
Al3++4NH3·H2O = AlO +4NH +2H2O
B
H+、K+、S2O 、SO
不能大量共存,因发生反应:
2H++ S2O =S↓+SO2↑+H2O
C
Na+、Fe3+、SO 、H2O2
能大量共存,粒子间不反应
D
H++ Na+、Cl-、MnO
能大量共存,粒子间不反应
A、A B、B C、C D、D14. 现代工业开发了用“NH3—NH4Cl水溶液”浸出氧化锌烟灰(主要成分为ZnO、Pb、CuO和As2O3)制取高纯锌的工艺流程如下图所示: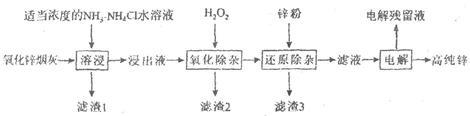
已知:①浸出液中含[Zn(NH3)4]2+、[Cu(NH3)4]2+、AsCl52- , 且存在[M(NH3)4]2+ M 2++ 4NH3(M为Cu或Zn);②“氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去。
下列有关说法错误的是( )
A、ZnO +2NH3·H2O + 2NH4+=[Zn(NH3)4] 2++3H2O B、为提高反应速率,“溶浸”过程的温度越高越好 C、“滤渣3”的主要成分为Cu、Zn D、“电解残留液”可返回“溶浸”过程循环利用15. 已知常温下CH3COOH、NH3·H2O的电离常数近似相等。下列实验操作能达到相应实验目的的是( )选项
实验操作
实验目的
A
向乙二醇中滴加过量酸性高锰酸钾溶液
制备乙二酸
B
向食盐水中通入过量的CO2
除去食盐水中的少量BaCl2
C
将石蜡油蒸汽通过炽热的碎瓷片,再将生成的气体通入溴水中
证明石蜡油的分解产物含不饱和烃
D
常温下,用pH计分别测定等体积1.0 mol·L-1
CH3COONH4溶液和0.1mol·L-1CH3COONH4溶液的pH
探究浓度对水解平衡的影响
A、A B、B C、C D、D16. 用0.1000 mol·L -1盐酸滴定20.00 mL Na2A溶液,溶液中H2A、HA-、A2-分布分数δ随pH变化曲线及滴定曲线如图。下列说法正确的是[如A2-分布分数:δ(A2-)=]( )
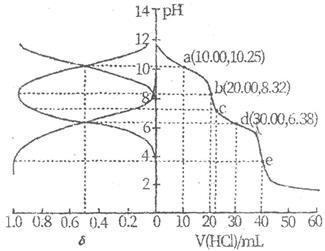 A、H2A的Kal为10-8.32 B、c点:c(HA-)>c(A2-)>c(H2A) C、第一次突变,可选甲基橙作指示剂 D、c(Na2A)=0.100 0 mol·L-1
A、H2A的Kal为10-8.32 B、c点:c(HA-)>c(A2-)>c(H2A) C、第一次突变,可选甲基橙作指示剂 D、c(Na2A)=0.100 0 mol·L-1二、非选择题:共56分。第17~19题为必考题,考生都必须作答,第20~21题为选考题,考生根据要求作答。
-
17. 某化学兴趣小组探究FeCl3溶液和Na2SO3溶液的反应情况。请回答相关问题。(1)、简述用FeCl3晶体配制FeCl3溶液的方法:;Na2SO3溶液用(填瓶塞材质)细口瓶保存。(2)、[实验1]分别将100 mL 1.0 mol·L-1的FeCl3溶液和Na2SO3溶液装入两个烧杯中,按下图进行实验,观察到电流汁指针发生偏转。

请写出左侧烧杯中的电极反应式。
盐桥中的阳离子向(填“左侧”或“右侧”)烧杯中迁移。
(3)、[实验2]在试管1中加入2 mL 1.0 mol·L-1Na2SO3溶液,然后滴加两滴1.0 mol·L-1 FeCl3溶液,溶液中立刻变成红褐色。对试管l进行加热至沸腾,产生红褐色沉淀。取出几漓混合液,加K3[Fe(CN)6]溶液,无蓝色沉淀出现。整个过程中来观察到明显的气泡产生。[实验3]在试管2中加入5 mol 1.0 mol·L-1 FeCl3溶液,然后再滴加l mL 1.0 mol·L-1 Na2SO3溶液,溶液立刻变成红褐色。取出几滴混合液,加K3[Fe(CN)6】溶液,产生蓝色沉淀。
实验3中生成蓝色沉淀的离子方程式为。
请设计实验证明SO 被氧化。
(4)、(反思与研讨]资料显示:H2SO3的Kal=1.7×10-2 Ka2=6.0 × 10-8;Fe(OH)3的Ksp=4 × 10-38;
反应2Fe3++ SO + H2O 2Fe2++SO + 2H+的平衡常数K= 1020.6。
反应2Fe3++ 3SO +6H2O 2Fe(OH)3↓+ 3H2SO3的平衡常数K的数量级为。由此可判断FeCl3溶液和Na2SO3溶液发生(填“互促水解”或“氧化还原”)反应的趋势更大。
18. 铼(Re)是熔点和沸点较高的金属单质之一,用于制造高效能喷射引擎和火箭引擎。钼酸锂(Li2MoO4)的外观为白色结晶粉末,用于电极材料、金属陶瓷的制作。从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉和制钼酸锂的流程如下图所示。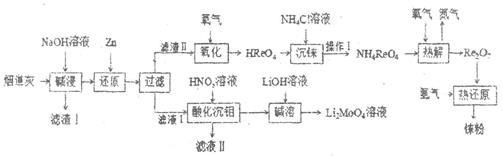
已知:
Ⅰ.Re2O7是酸性氧化物,过铼酸(HReO4)是易溶于水的一元强酸,但不具有强氧化性。
Ⅱ.过铼酸铵(NH4ReO4)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)、“碱浸”时,Re2O7和MoO3分别与NaOH发生以下反应(填写化学方程式)、MoO3+2NaOH=NaMoO4+H2O,则“滤渣I”的主要成分为(填化学式)。(2)、“还原”时,Zn被氧化成ZnO2 2- , 铼的化合物被还原生成难溶的2ReO2·2H2O,该反应的离子方程式为。(3)、“沉铼”时,加入热NH4Cl溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净NH4ReO4晶体,“操作I”包括、、洗涤、干燥。(4)、“热解”时,发生反应的化学方程式为。(5)、“酸化沉钼”过程溶液pH和反应时间对钼酸的析出有很大影响,根据图2中数据判断最佳的“酸化沉钼”条件:反应时间为min、pH为。 (6)、电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图3所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为g。19. 甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义。(1)、一种重要的工业制备甲醇的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H。
(6)、电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如图3所示。电解时,若维持电流强度为0.5A(相当于每秒通过5×10-6mol电子),电解90min,理论上消耗MoS2的质量为g。19. 甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义。(1)、一种重要的工业制备甲醇的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H。已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H1=-40.9kJ·mol-1
②CO(g)+2H2O(g) CH3OH(g) △H2=-90.4kJ·mol-1
试计算制备反应的△H=。
(2)、对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),v正=k正p(CO2)·p3(H2),v逆=k逆·p(CH3OH)·p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。
在540K下,按初始投料比n(CO2):n(H2)=3:l、n(CO2):n(H2)=1:1、n(CO2):n(H2)=1:3,得到不同压强条件下H2的平衡转化率关系图:

①比较a、b、c各曲线所表示的投料比大小顺序为(用字母表示)。
②点N在线b上,计算540K的压强平衡常数Kp=(用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻p(CO2)=0.2MPa,p(CH3OH)=p(H2O)=0.1MPa,
p(H2)=0.4MPa,此时v正:v逆=。
(3)、甲醇催化可制取丙烯,反应为:3CH3OH(g) C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如下图中曲线a所示,已知Arrhenius经验公式为R lnk= (Ea为活化能,k为速率常数,R和C为常数)

①该反应的活化能Ea=kJ·mol-1。
②当使用更高效催化剂时,在图中画出R lnk与 关系的示意图。
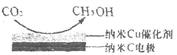
(4)、在饱和KHCO3电解液中,电解活化的CO2也可以制备CH3OH,其原理如下图所示,则阴极的电极反应式为。
三、(二)选考题:共14分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。
-
20. [选修3:物质结构与性质】(1)、据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)
为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
①基态锌原子的电子排布式为 , 原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为。
②Cd与Zn同族,价电子数相同,若配离子[Cd(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=。
③碲和硫同主族,TeO32-的空间构型为 , 写出一个与TeO32-互为等电子体的分子。
(2)、石墨烯是一种二维碳纳米材料,具有优异的光学、力学、电学特性,在材料学、微纳加工、能源、生物医学和药物传递方面具有重要应用前景。1 mol石墨烯含六元环的数目为;石墨烯中部分碳原子被氧化后,其平面结构将发生改变,转化为氧化石墨烯(如下图4),氧化石墨烯中键角α(填“>”、“<”或“=”)键角β,原因是。
 (3)、立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图5所示,B原子填在由N原子构成的(填“四面体”、“八两体”或“立方体”)空隙中。若晶胞边长为a pm,B原子半径为b pm,N原子半径为c pm,则该晶胞的空间利用率为(列出计算式),氮硼原子间的最短距离为 pm。21. [选修5:有机化学基础]某药物中间体I的合成路线如图所示:
(3)、立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图5所示,B原子填在由N原子构成的(填“四面体”、“八两体”或“立方体”)空隙中。若晶胞边长为a pm,B原子半径为b pm,N原子半径为c pm,则该晶胞的空间利用率为(列出计算式),氮硼原子间的最短距离为 pm。21. [选修5:有机化学基础]某药物中间体I的合成路线如图所示: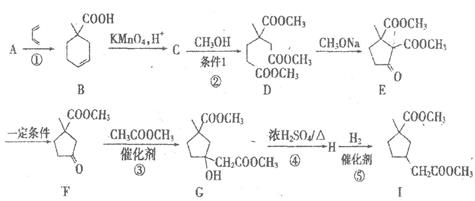
已知:
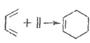
回答下列问题:
(1)、A的结构简式为;H的官能团名称为。(2)、反应②中的化学方程式为。(3)、反应⑤的化学反应类型为。(4)、同时满足下列条件的F的同分异构体的数目为。①分子结构中含六元碳环、甲基和酮羰基;②既能发生水解反应,又能发生银镜反应写出其中核磁共振氢谱有4组峰,峰面积比为4:4:3:1的结构简式。
(5)、参照上述合成路线和信息,以 和
和  为原料(无机试剂任选),设计三步制备
为原料(无机试剂任选),设计三步制备
 的合成路线。
的合成路线。